5 fiches de cours interactives
|
|
|
|
|
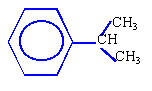
le carbocation isopropyle le plus stable se forme
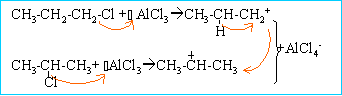
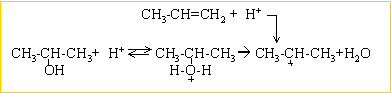
réaction de Friedel et Crafts
l'intermédiaire réactionnel est le carbocation isopropyle :
elle conduit à la fixation d'une chaine latérale sur le benzène
|
corrigé
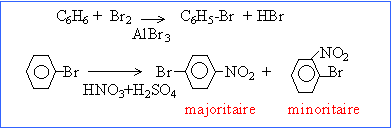
formation du bromobenzène puis du dérivé nitré
le substituant Br est donneur d'électrons; il oriente en ortho et para la seconde substitution
la position ortho est défavorisée pour des raisons d'encombrement stérique.
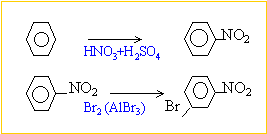
formation du nitrobenzène puis du dérivé bromé
le site de fixation du second substituant dépend du substituant déja fixé:
NO2 déja fixé oriente en méta
|
|
|
|
|
|
|
A est un triméthylbenzène
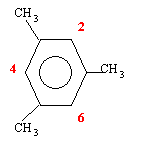
les 3 positions 2,4,6 sont équivalentes et donnent le même dérivé mononitré.
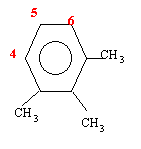
une substitution sur les carbones 4 et 6 donne le même produit mononitré.
une substitution sur le carbone 5 donne un second isomère mononitré
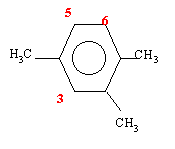
les carbones 3, 5, 6 sont tous différents et on obtient 3 isomères mononitrés.
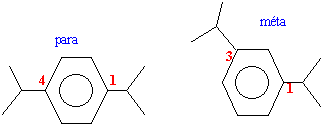
Par contre le groupe ter-butyle est très encombrant et seuls les dérivés disubstitués en para et méta sont obtenus aisément.
|
- On fait agir de l'éthylène sur du benzène en présence de AlCl3 sous la pression atmosphérique. Le produit A obtenu est déshydrogéné vers 500°C en présence de vapeur d'eau. Par polymérisation en présence de catalyseur de Ziegler et Natta on obtient une macromolécule C. Identifier A,B,C.
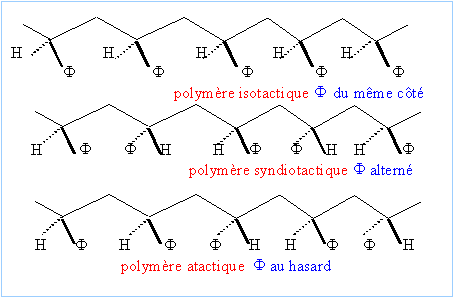
Avec d'autres catalyseurs on obtient d'autres polymères D et E différant de C par la position des groupes phényles. Comparer les structures de C,D,E.
corrigé
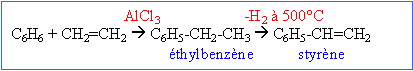
polymérisation du styrène en présence des catalyseurs de Ziegler et Natta donne le polystyrène
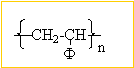
C, D, E sont des polystyrènes qui diffèrent par la répartition du groupe phényl le long de la chaîne carbonée.