|
Capes 95 . |
|||||||||||||||||||||
| .
. |
|||||||||||||||||||||
|
|||||||||||||||||||||
|
L'américium 241 ( Z=95) est un émetteur a de période 458 années. On réalise un mélange d'américium et de bérylium 9, et on obtient un flux de neutrons par deux réactions successives. X* est un nucléide instable. La source ainsi obtenue émettant 107 neutrons par seconde, est placée au centre d'une sphère de polypropylène. Par des tiroirs on peut introduire des échantillons à irradier dans le flux de neutrons. Ce bloc d'irradiation offre l'intérêt de pouvoir séjourner en permanence dans la salle de manipulations sans danger pour les utilisateurs, car la source émet peu de rayons g. En outre il n'estpas nécessaire de renouveller réguliérement la source.
corrigé |
|||||||||||||||||||||
|
La particule a est un noyau d'hélium. La période radioactive ou demi vie t½ est le temps au bout duquel la moitié de l'échantillon initial a disparu. L''atome d'américium posséde 95 électrons, 95 protons, 241-95 = 146 neutrons.
lors d'un désintégration radioactive, il y a : - conservation du nombre total de nucléons : 241 = 4+237 - conservation du nombre de charges : 95 = 2+93 - conservation de la quantité de mouvement -
conservation de l'énergie
énergie libérée : DE =0,0072 * 931,5 = 6,71 MeV. énergie au repos de la particule a, la plus légère : 4,0015*931,5 = 3 727 meV. l'énergie libérée étant faible devant les énergies au repos des particules, les expressions non relativistes de l'énergie et de la quantité de mouvement sont utilisables : DE = ½ m1 v1² + ½ m2v2² (1) l'indice 1 conserne la particule a, l'indice 2 le noyau de Np. conservation de la quantité de mouvement :
v1 = m2v2 / m1=237,048 v2 / 4,015 =59,04 v2. repport dans (1) 6,71 * 1,6 10-13 = 10,736 10-13 J 10,736 10-13 = ½ [ m1 *59,04² v2² + m2v2²] mettre les masses en kg m1 = 4,015 *1,67 10-27 = 6,7 10-27 kg m2 = 237,048 *1,67 10-27 = 395,87 10-27 kg 2*10,736 10-13 = 10-27 v2²[ 6,7 *59,04² + 395,87]=2,37 10-23 v2² v2² = 9,06 1010 d'où v2 = 3 105 m/s. v1 = 1,77 107 m/s. conservation du nombre total de nucléons: 9 +4 =A donne A=13 conservation de la charge : 4+2 = Z donne Z=6 X est l'élément carbone. Le rayonnement g est un rayonnemnt électromagnétique, d'énergie très importante, de l'ordre du MeV. La période de l'américium est très longue ; le bérylium 9 est un noyau stable. Il n'est pas utile de renouveller régulièrement la source.
|
|||||||||||||||||||||
|
L'aluminium issu de l'industrie chimique peut contenir des impuretés en quantité très faible comme le sodium, le cuivre ou le manganèse. Pour vérifier la pureté d'un échantillon d'aluminium on l'irradie par un flux neutronique. Les éléments qu'il contient subissent des réactions nucléaires conduisant à la création d'isotopes instables. L'identification des isotopes ansi formés est faite par l'analyse de leur spectre de rayons g et permet de connaître la nature des éléments initialement présents dans l'échantillon tout en effectuant leur dosage. On s'interessera plus précisément à la présence du sodium 23 dans l'échantillon.
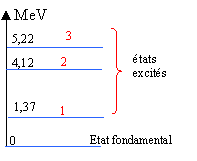 données : 1 u = 1,66 10-27 kg = 931,5 mev/c². c= 3 108 m/s ; e = 1,6 10-19 C ; masse d'une particule a : 4,0015 u ; h= 6,62 10-34 J/s ; corrigé Il s'agit d'un isotope: le nombre de protons n'a pas changé et le nombre de neutrons a changé
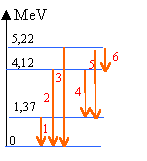
l'antineutrino est une particule de charge nulle et de masse nulle. Le retour d'un niveau excité à un niveau moins excité ( de moindre énergie) ou au niveau fondamental se traduit par l'émission d'un photon g.
six photons peuvent être émis E = hn. énergie en joule et fréquence en Hz 1MeV = 1,6 10-13 J ; h = 6,6 10-34 J/s
|