|
. . |
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
prťparation du nickel |
On ťtudie les rťactions : 2C + O2 --> 2 CO (1) et 2 Ni + O2 --> 2 NiO (2)
corrigť |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
DH01=2 DH0(CO)-2 DH0(C)-DH0(O2)= -221 kJ mol-1. DH02=2 DH0(NiO)-2 DH0(Ni)-DH0(O2)= -488,6 kJ mol-1. DS01=2 S0(CO)-2 S0(C)-S0(O2)= 178,8 J mol-1. DS02=2 S0(NiO)-2 S0(Ni)-S0(O2)= -188,8 J mol-1. DG0=DH0-TDS0 DG01 = -221 000 -178,8 T DG02= -488 600 + 188,8 T 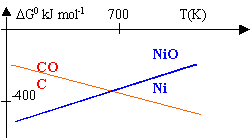
En ťgalisant ces 2 derniŤres expressions on trouve l'intersection des droites ŗ T=728 K. Il est donc possible de rťduire NiO par le carbone au dessus de cette tempťrature, en vue de prťparer le nickel. NiO + C --> Ni + CO A 1000 K, DG0=DG01 - DG02 = -105 J mol-1. DG0 =-RT lnK donc K=2,3 105, rťaction totale
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
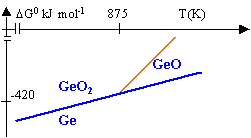
dismutation de GeO |
On ťtudie les rťactions : 2Ge + O2 --> 2 GeO (1) et 2 GeO + O2 --> 2 GeO2 (2)
corrigť |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
DH01=2 DH0(GeO)-2 DH0(Ge)-DH0(O2)= -510 kJ mol-1. DH02=2 DH0(GeO2)-2 DH0(GeO)-DH0(O2)= -594 kJ mol-1. DS01=2 S0(GeO)-2 S0(Ge)-S0(O2)= -101 J mol-1. DS02=2 S0(GeO2)-2 S0(GeO)-S0(O2)= -197 J mol-1. DG0=DH0-TDS0 DG01 = -510 000 +101 T DG02= -594 000 + 197 T
2 GeO --> GeO2 + Ge (3) DH03= DH0(GeO2)+ DH0(Ge)-2DH0(GeO)= -42 kJ mol-1. DS03= S0(GeO2)-2 S0(GeO)+S0(Ge)= -48 J mol-1. DG03 = -42 000 + 48 T DG03 est
nťgatif tant que T< 875 K. La constante de la
rťaction est supťrieure ŗ 1 et la
dismutation se produit ŗ une tempťrature
infťrieure ŗ 875 K.
DH04= DH0(GeO2)- DH0(Ge)-DH0(O2 )= -552 kJ mol-1. DS04= S0(GeO2)- S0(O2)-S0(Ge)= -149 J mol-1. DG04 = -552 000 + 149 T point triple ( coexistence des 3 espŤces) : 875 K et DG0 = -464 kJ Avant 875 K la rťaction (4 )a lieu; au dela les
rťactions (1) et (2) ont lieu . ŗ 800 K l'oxydation donne GeO2; ŗ 950 K l'oxydation donne GeO et GeO2.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
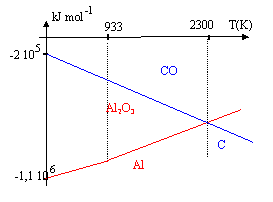
La poudre d'aluminium brŻle trŤs facilement ; la rťaction est exothermique.
corrigť 4/3 Al + O2 = 2/3 Al2O3.(1) sur l'intervalle [250 K, 933 K] : DH01= 2/3 DH0(Al2O3)- 4/3DH0(Al)-DH0(O2 )= -1116 kJ mol-1. DS01= 2/3S0(Al2O3)- S0(O2)-4/3S0(Al)= 34-205-37,3 = -208,3 J K-1 mol-1. DG01 = -1 116 000 + 208,3 T. sur l'intervalle [933 K, 2500 K] DH01= 2/3 DH0(Al2O3)- 4/3[DH0(Al)+ Dfusion Hį(Al)]-DH0(O2 ) DH01= -1116 -4/3* 10,9 = -1130,5 kJ mol-1. entropie de changement d'ťtat ŗ 933 K : S= Dfusion Hį(Al) / Tfusion = -10900 / 933= 11,7 J K-1 mol-1. DS01= 2/3S0(Al2O3)- S0(O2)-4/3[S0(Al)+11,7]= 34-205-53 = -224 J K-1 mol-1. DG01 = -1 130 500 + 224 T. 2C+O2 = 2CO (2) DH02=2 DH0(CO)-2 DH0(C)-DH0(O2)= -220 kJ mol-1. DS02=2 S0(CO)-2 S0(C)-S0(O2)= 177 JK-1 mol-1. DG0=DH0-T DS0 DG02= -220 000 - 177 T Le cabone peut rťduire l'alumine si l'enthalpie libre de la rťaction suivante est nťgative : 3C+ Al2O3 = CO + 2Al obtenue ŗ partir de 1,5 *(2) -1,5 (1) DG0= 1,5(DG02 - DG01) pour trouver la tempťrature ŗ partir de laquelle cette rťduction est possible , ťcrire que DG0 =0 soit DG02= DG01; -1 130 500 + 224 T= -220 000 -177 T T= 910500/ 401 = 2270 K. tempťrature trop ťlevťe pour que cette mťthode soit bon marchť ; la prťparation de l'aluminium se fait par ťlectrolyse.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
A diverses tempťratures T, on relŤve les valeurs correspondantes des enthalpies libres standard DrG0 (DrHG0 et DrSG0 seront considťrťes indťpendantes de T ) relatives aux rťactions d'obtention des oxydes de cuivre (I) et (II) : Cu2O (rťaction 1) et CuO (rťaction 2). ( les rťactions ne font intervenir qu'une mole de dioxygŤne ).
corrigť Quand la tempťrature augmente de T=500 K, DrG01 augmente de 70 kJ/mol : DrG01 = 70/500 T + constante = 0,14 T + constante constante = -230 -0,14*800 = -230 -112 = - 342 kJ/mol DrG01 = 0,14 T -342. Quand la tempťrature augmente de T=500 K, DrG02 augmente de 90 kJ/mol : DrG02 = 90/500 T + constante = 0,18 T + constante constante = -170 -0,18*800 = -170 -1442 = - 314 kJ/mol DrG02 = 0,18 T -314. le signe positif des pentes des droites obtenues indique des rťactions endothermiques. valeurs respectives de DrH į et DrSį pour les rťactions (1) et (2). DrG0 = DrH į -TDrS0 par identification : DrH0 1 = -342 kJ/mol ; DrS0 1 = 0,14 kJ K-1 mol-1. par identification : DrH0 2 = -314 kJ/mol ; DrS0 2 = 0,18 kJ K-1 mol-1. 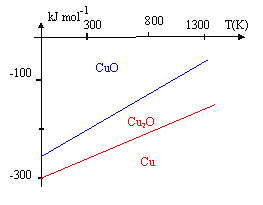
4Cu+O2 =2 Cu2O (1) 2 Cu + O2 = 2 CuO (2) Ĺ (2)- Ĺ (1) donne : Cu2O = Cu + CuO (3) DrG03 =Ĺ(DrG02 -DrG01 )= 0,18T-314 -(0,14 T-342) DrG03 = 0,04 T +28 . L'ťtude thermodynamique de l'oxydation du cuivre montre que la coexistence, ŗ l'ťquilibre, entre le cuivre et l'oxyde de cuivre (II) est impossible. L'oxyde en contact avec le mťtal est Cu2O. Ce dernier peut Ítre oxydť ŗ son tour en CuO par le dioxygŤne. D'un point de vue cinťtique, l'oxydation du cuivre par O2 sec en CuO via Cu2O est trŤs lente. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Rťduction de la chromite: La chromite est oxydťe, en milieu alcalin, en chromate de potassium et oxyde ferrique. Le chromate de potassium est sťparť par dissolution dans l’eau puis prťcipitť sous forme de dichromate de potassium qui est rťduit par le carbone en oxyde de chrome (III) Cr2O3 qu’il s’agit de rťduire en chrome mťtallique.
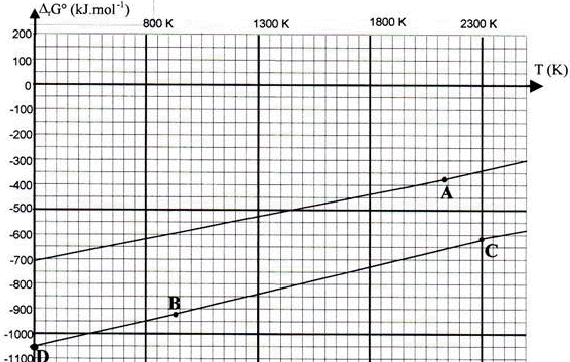 Ce diagramme reprťsente l’enthalpie libre
standard de formation des oxydes pour une mole de
dioxygŤne en fonction de la tempťrature.
corrigť Cr2O3 (s)+ 3H2 (g)= 2 Cr (s)+ 3H2O(g) D H= 3 DfHį (H2O) - DfHį (Cr2O3) = -3* 242 +1140 = 414 kJ mol-1. D S = 3 Sį (H2O) + 2Sį(Cr)- Sį (Cr2O3)-3Sį(H2)= 3*189 + 2*24-3*131-81 = 141 J K-1 mol-1. D G= D H-T D S = 414000-1300*141 = 230700 J mol-1. DG positif; donc rťaction endothermique favorisťe par une ťlťvation de tempťrature. ln K= - D G / ( RT) = -230700 / (8,31*1300) = -21,35 K= 5,3 10-10 donc rťaction spontanťe en sens inverse ( de droite ŗ gauche). 4/3 Al + O2 = 2/3 Al2O3 4/3 Cr + O2 = 2/3 Cr2O3 Al , le plus rťducteur, est situť en dessous de la droite CD la droite du bas correspond ŗ Al2O3 / Al. A : fusion du chrome ŗ 2130 K B : fusion aluminium ŗ 933 K C : fusion alumine. pente du segment DB : - DS de la rťaction 4/3 Al + O2 = 2/3 Al2O3 D S = 2/3S( Al2O3 )- 4/3S( Al)-S(O2) = 2/3*51-4/3*28-205=34-37,3-205= -208,3 J K-1 mol-1 - DS = 208,3 J K-1 mol-1 . pente du segment BC : entropie de changement d'ťtat ŗ 933 K : S= Dfusion Hį(Al) / Tfusion = -11000 / 933= 11,8 J K-1 mol-1. DS0= 2/3S0(Al2O3)- S0(O2)-4/3[S0(Al)+11,8]= 34-205-53 = -224 J K-1 mol-1. - DS = 224 J K-1 mol-1 . Cr2O3 (s)+ 2Al(l) = 2Cr (s)+ Al2O3(s) D H = D (Al2O3)-DH ( Cr2O3) - 2Dfusion Hį(Al)= -1676+1140-22 = -558 kJ mol-1 D S = S( Al2O3 ) + 2 S (Cr) - S( Cr2O3 )-2[ S( Al)+ Dfusion Hį(Al) / Tfusion] D S = 51+2*24-81-2(28 +11,8)= -61,6 J K-1 mol-1 D G= D H-T D S = -558000 + 61,6*1300 = -477900 J mol-1 ln K = 477900 / (8,31*1300) = 44.3 K= 1,7 10 24 K est trŤs grand, donc rťaction spontanťe, totale dans le sens direct. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|