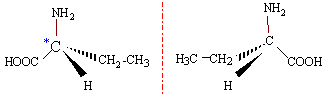|
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitķs adaptķes Ó vos centres d’intķrĻts.
|
||
|
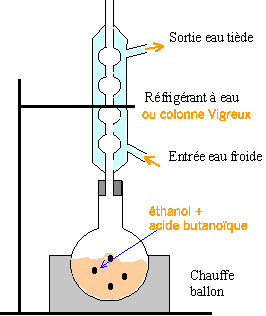
Je dķtermine la formule brute de A : formule brute CxHyOz avec x, y, z entiers 12x / 54,6 = 0,88 d'o∙ x = 4 y / 9,1 = 0,88 d'o∙ y = 8 16 z / 36,3 = 0,88 d'o∙ z =2. A est soluble dans l'eau. Sa solution fait virer le bleu de bromothymol au jaune. La chaŅne carbonķe de A est linķaire. il s'agit d'un acide carboxylique ( le BBT devient jaune) Ó chaine linķaire comptant 4 atomes de carbone. CH3-CH2-CH2-CO2H acide butano’que.
CH3-CH2OH +
CH3-CH2-CH2-CO2H
ķquilibre avec
CH3-CH2-CH2-CO2-CH2-CH3
+H2O Le chauffage Ó reflux permet d'accķlķrer la rķaction en travaillant Ó tempķrature moyenne en ķvitant les pertes de matiĶre.
On considĶre la formule B :
CH3-CH2-CH(NH2)-COOH. Le carbone porteur du groupe amino NH2 est asymķtrique : il possĶde 4 substituants diffķrents. la molķcule est chirale, non superposable Ó son image dans un miroir. elle possĶde deux isomĶres optiques ou ķnantiomĶres.
La molķcule A, sans carbone asymķtrique ne possĶde pas cette particularitķ. |
||
|
|
||
|
|