|
|
|
|
|
|
- L'iode intervient dans le métabolisme de la
glande thyroide. L'iode 127 (
12753I) est stable alors que l'iode
131 est émetteur b+
et l'iode 124 est émetteur b-.
Données : m(iode 131) = 130,87697 u ; m(proton)= 1,007270023 u ; m(neutron) = 1,008665842 u ; c=3 108 m/s ; 1u = 1,66054 10-27 kg ; 1 eV= 1,602 10-19 J.
Quelle est l'énergie de liaison (MeV) du noyau d'iode 131 ?
11 ; 170 ; 110 ; 1705 ; 1103 ; 17. - Le cobalt 60 utilisé en radiothérapie
est un émetteur b-
dont le schéma de désintégration est
donné ci dessous :
Ni*: noyau de nickel excité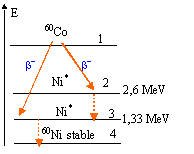
Données : h= 6,62 10-34 Js.
Quelle est la longueur d'onde (m) de l'émission qui se produit lors de la transition du niveau 3 au niveau 4 ?
1,65 10-12 ; 9,32 10-7 ; 1,65 10-6 ; 9,32 10-13 ; 3,22 10-9 ; 3,22 10-13.
corrigé
53 protons et 131-53 = 78 neutrons
défaut de masse : 53*1,007270023 + 78*1,008665842-130,87697 = 1,184427 u
1,184427*1,66 10-27 = 1,9659 10-27 kg.
énergie : Dmc² = 1,9659 10-27 *(3 108)² = 1,77 10-10 J
1,77 10-10 / 1,6 10-19 = 1,106 109 eV = 1106 MeV.
E=hc/l soit l = E/(hc)
E = 1,33 MeV = 1,33 106 eV = 1,33 106 *1,6 10-19 J= 2,128 10-13 J
l = 2,128 10-13/ (6,62 10-34 * 3 108) = 9,33 10-13 m.
- Une radiation rouge a pour longueur d'onde dans le
vide l =656,3 nm. Pour cette
radiation, l'indice du verre est n=1,612. c=3
108 m/s.
- Quelle est sa fréquence (Hz) ?
197 ; 4,57 1014 ; 2,19 10-15 ; 1,52 109 ; 4,57 1011 ; 2,19 1014.
- Quelle est la célérité (m/s) de cette radiation dans le verre ?
3 108 ; 4,84 108 ; 2,52 108 ; 1,86 108 ; 1,47 108 ; 2,25 108 ; - Sur une canalisation en acier dans laquelle circule
de l'eau, on provoque un choc. Un capteur situé
à une distance d, détecte deux signaux
sonores, brefs, séparés par une
durée égale à 1,8 s ;
célérité du son dans l'acier : 5
km/s; célérité du son dans l'eau 1,5
km/s.
- Quelle est la distance d(m)
3,87 ; 51 ; 3857 ; 1,94 ; 0,51 ; 194. - Le quartz d'une montre A, parfaitement
réglée, vibre à la fréquence
f0 = 32768 Hz. Une autre montre à
quartz B, identique à A, retarde de 2 s par
semaine par rapport à A
- Quel est l'écart de fréquence (Hz) de vibration des deux quartz ?
1 ; 10 ; 3,3 10-6 ; 7 ; 0,1 ; 0,7.
corrigé
f= c/l = 3 108 / 656,3 10-9 = 4,57 1014 Hz.
indice n = 3 108 / célérité dans le verre
célérité dans le verre = 3 108 / n = 3 108 /1,612 = 1,86 108 m/s.
dans l'eau, la durée du parcours de l'onde est : t1 = d/ve = d/1500 s
dans l'acier, la durée du parcours de l'onde est : t2 = d/va = d/5000 s
t = t1 - t2 =d( 1/1500-1/5000) = 4,66 10-4 d.
d =t / 4,66 10-4 = 1,8 / 4,66 10-4 =3862 m.
période T0 = 1/32768 = 3,0517578 10-5 s.
pour que la montre affiche une seconde il faut amplifier, multiplier T0 par 32768.
retard : 2/7 = 0,2857 s /jour ; 0,2857 / 24 = 0,0119 s/heure; 0,0119 / 3600 = 3,307 10-6 s à chaque seconde.
en tenant compte du coefficient d'amplification on trouve la période T :
T = T0+3,307 10-6 / 32768 =T0+10-10 = 3,0517678 10-5 s.
puis la fréquence f = 1/T = 32767,9 Hz soit un écart de 0,1 Hz.
- Une bobine idéale d'inductance L= 1,5 mH est
branchée en série avec une
résistance R= 100 ohms et un
générateur de tension continue, de fem E=9
V. A t=0, l'interrupteur est fermé.
- Quelle est la valeur de la constante de temps t du circuit ( seconde) ?
1,5 10-5 ; 0,15 ; 66,7 ; 150 ; 6670 ; 3,87 10-2.
- Que vaut la tension (V) aux bornes de la bobine à t= 5t.
9 ; 5,7 ; 3,3 ; 4,5 ; 2,1 ; 0
- Que vaut l'intensité du courant (mA) à t= 1 ms.
11,1 ; 21 ; 90 ; 57 ; 0 ; 45. - Un circuit oscillant non amorti, comporte une bobine
d'inductance L=0,1 H et un condensateur de
capacité C=2,2 mF. Le
condensateur est initialement chargé sous une
tension de 12 V.
- Quelle est l'énergie maximale (J) emmagasinée par la bobine ?
1,32 10-4 ; 3,17 10-4 ; 1,6 10-4 ; 0,6 ; 0,8 10-4 ; 2,1 10-3 .
- Quelle est l'intensité (A) maximale du courant dans le circuit ?
0,2 ; 5,6 10-2 ; 1,6 10-3 ; 4 10-2 ; 0,45 ; 5,7 10-3 .
corrigé
constante de temps t = L/R = 1,5 10-3 /100 = 1,5 10-5 s.
après une durée supérieure à 5t, le régime permanent est établi et la tension aux bornes de la bobine est égale à zéro si sa résistance est nulle.
à t = 10-3 s, valeur supérieure à 5t, le régime permanent est établi et l'intensité vaut : i = E/R = 9/100 = 0,09 A = 90 mA.
l'énergie maximale stockée par le condensateur se retrouve dans la bobine si la résistance du dipôle est nulle .
E = ½Cu² = 0,5 *2,2 10-6 *12² = 1,584 10-4 J.
intensité maximale : E=½Li² soit i² = 2E/L =2*1,584 10-4 / 0,1 = 3,168 10-3 soit I = 0,056 A.
- Une boule de bois de rayon 6,4 cm tombe verticalement
dans l'air. La force de résistance due à
l'air est de la forme
fr = -r0 S Cx v²
Données : masse volumique du bois :rb =620 kg/m3 ; Cx=0,45; S section de la boule.masse volumique de l'air :r0 =1,21 kg/m3 ;
- Quelle est la valeur de la vitesse limite (m/s) atteinte par la boule ?
4,4 ; 19,1 ; 25,1 ; 13,7 ; 34,2 ; 43,7 - Un satellite de type SPOT a une trajectoire
circulaire surplombant les poles terrestres. Il s'agit
d'un satellite dit à défilement,
destiné à fournir des images de tout le
globe terrestre. La période de passage au dessus
d'un même lieu est égale à 26 jours
solaires moyens et correspond à la durée de
369 révolutions du satellite.
Données : rayon de la terre RT= 6380 km ; masse de la terre MT= 5,98 1024 kg ; constante de gravitation G= 6,67 10-11 Nm² kg-2 ; durée du jour solaire moyen : 86400 s.
- Quelle est la période (s) de révolution du satellite ?
6088 ; 1,23 106 ; 11,1 ; 9 ; 3044 ; 12176.
- Quelle est l'altitude (km) du satellite ?
65698 ; 830 ; 7210 ; 35800 ; 27600 ; 4220. - Dans un manuel d'apprentissage du tennis on peut lire
le conseil suivant concernant le service "Frappez la
balle devant vous de façon à donner
à la balle une vitesse en dessous de la direction
horizontale ". Un tennisman frappe la balle à une
hauteur h=2,4 m . Le vecteur vitesse de la balle
dirigé vers le bas, fait un angle a=10°
avec l'horizontale et a une valeur v0=30
m/s.
- Quelle est la vitesse (m/s) de la balle en touchant le sol ?
29,2 ; 47 ; 58 ; 34,3 ; 30,8 ; 41,7. - Dans un bâtiment public, un lustre assimilable
a un pendule simple, oscille régulièrement.
La durée de 10 oscillations est de 49,2 s.
- Quelle est la longueur( m) du câble auquel est suspendu le lustre ?
6 ; 7,7 ; 37,7 ; 12,2 ; 4,3 ; 8,6. - Un oscillateur élastique horizontal est
constitué d'un solide de masse m=256 get d'un
ressort hélicoïdal à spires non
jointives de raideur k= 78 N/m.
- Quelle est la période propre (s) de l'oscillateur ?
11,38 ; 3,47 ; 0,02 ; 1,91 ; 0,71 ; 0,36.
Quelle est la valeur (rad) de la phase à l'origine ?
p/4 ; p ; 3p/2 ; p/2 ; 0 ; 3p/4.
- Quelle est la valeur de la vitesse (m/s) lorsque l'élongation est x=0,5 cm ?
2,2 10-2 ; 0,34 ; 0,26 ; 8,7 10-2 ; 0,12 ; 0,17. - Un athlète a parcouru un 100 m en 10,5s. On
modèlise sa course e considérant 2 phases :
il accélère uniformément pendant les
15 premièrs mètres de course, qu'il
parcourt ensuite à vitesse constante de 10 m/s
jusqu'à l'arrivée.
- Quelle est la valeur de l'accélération moyenne (m/s²) pendant la phase de démarrage ?
0,95 ; 0,12 ; 9,5 ; 5 ; 6,7 ; 4,3.
corrigé
lorsque la vitesse limite est atteinte le mouvement est rectiligne uniforme. La valeur du poids de la boule est égale à la valeur de la force de frottement.
volume de la boule = 4/3 pr3 ;
masse = volume * masse volumique du bois =4/3 pr3 rb ; poids = 4/3 pr3 rb g
frottement = r0 S Cx v²lim ; avec S = pr2.
4/3 pr3 rb g = r0 pr2 Cx v²lim d'où 4/3 r rb g = r0 Cx v²lim et v²lim =4r rb g /(3r0 Cx )
v²lim = 4*6,4 10-2 *620*9,8 / (3*1,21*0,45)=952 soit vlim = 30,8 m/s.
période : 26*24*3600 / 369 = 6088 s.
3ème loi de Kepler : T² / r3 = 4p² / (GM)
4p² / (GM) =4*3,14² / (6,67 10-11 *5,98 1024) = 9,88 10-14.
r3 = T² / 9,88 10-14 = 6088² /9,88 10-14 = 0,375 1021 soit r = 0,721 107 m = 7210 km
il faut retrancher le rayon de la terre h = 7210-6380 = 830 km.
théorème de l'énergie cinétique : seul le poids travaille (mgh)
½mv²-½mv0² = mgh soit v² = v0² +2gh = 900 + 2*9,8*2,4 = 947 et v = 30,78 m/s.
période T= 4,92 s. Or T = 2p racine carrée (l/g)
T² = 4p² l/g soit l = T²g/ (4p² ) = 4,92² *9,8 / (4*3,14²) = 6 m.
T = 2p racine carrée (m/k) = 6,28 [0,256 / 78]½ = 0,36 s.
x(t) = 0,02 cos (wt) avec w = 2p/T = 6,28 / 0,36 = 17,44 rad/s.
la phase initiale est nulle.
à quelle date t, l'élongation vaut-elle 0,005 m ?
0,005 = 0,02 cos( 17,44 t) soit cos(17,44t)= 0,005/0,02 = 0,25 = cos( 1,318 ) ( angle en radian)
t = 1,318 / 17,44 = 0,07555 s.
la vitesse est la dérivée de x(t) par rapport au temps : v(t) = 0,02 w (-1) sin( wt)
|v(t)| = 0,02*17,44 sin (1,318) = 0,02*17,44 * 0,9682 = 0,34 m/s.
durée du mouvement rectiligne uniforme : (100-15) / 10 = 8,5 s
durée de la phase de démarrage Dt =10,5/8,5 = 2s
variation de la vitesse au cours du démarrage : D v = 10 m/s
accélération moyenne a = D v /Dt = 10/2 = 5 m/s².
- Le taux d'avancement final, d'un volume
v0=100 mL de solution d'acide
méthanoïque (HCOOH) de concentration initiale
c0=0,1 mol/L est 0,04. Quel est le pH de la
solution ?
1,6 ; 1,4 ; 2,4 ; 3,4 ; 4,4 ; 3. - A la date t=0, on introduit dans un bécher un
volume v=30 mL d'une solution aqueuse contenant des ions
peroxodisulfate S2O82-,
de concentration c=0,1 mol/L et un volume v'=40 mL d'une
solution aqueuse contenant des ions iodures I-
de concentration c=0,1 mol/L. La réaction est
lente ; il se forme du diiode et des ions sulfates
SO42-. Le dosage du diiode
formé au cours du temps fournit les mesures
suivantes :
- Quel est l'ordre de grandeur de la vitesse volumique de la réaction à l'instant initial (mol L-1 s-1)t(s) 0 20 40 60 80 100 120 200 nI2 10-4 mol 0 4,4 7,7 10,7 12,6 14,2 15,8 18,2
3,6 10-4 ; 1,8 10-4 ;7,2 10-4 ;9,2 10-4 ; 8,3 10-4 ; 1,2 10-3.
- Quel est le temps de demi-réaction ? (s)
30 ; 120 ; 200 ; 55 ; 90 ; 250. - On mesure la résistance à 25°C
d'une solution aqueuse d'acide propanoïque de
concentration c0=3 10-3 mol/L. On
trouve R= 12 kW. Les plaques
de la cellule de conductimètrie ont une surface de
1,1 cm² et sont distantes de 1 cm. l(CH3-CH2-COO-)
= 3,6 10-3 ; l(H3O+)
= 3,5 10-2 Sm²mol-1.
- Quelle est la valeur de la constante d'acidité Ka de cet acide ?
2,2 10-2 ; 6,3 10-10 ; 4,5 10-7 ; 7,6 10-3 ; 1,3 10-3 ; 8,9 10-2 .
corrigé
[H3O+]= t c0 = 0,04*0,1 = 4 10-3 mol/L
pH = -log(4 10-3 ) = 2,4.
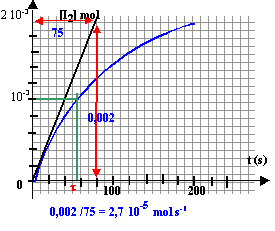
v0 = 1/V dnI2/dt = 1/((30+40) 10-3)*2,7 10-5= 3,8 10-4 mol L-1 s-1.
Quel est le réactif limitant ?
S2O82- + 2e- = 2SO42-
2I-=I2+2e-
S2O82- + 2I- = 2SO42- +I2.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ion iodure en défaut : t½ , date à laquelle la moitié du réactif limitant a disparu.
t½ correspond à x = ½ xmax = 10-3 mol I2 ; la lecture sur le graphe donne t½ voisin 55 s.
R= 12000 W ; conductance G=1/R = 1/12000 = 8,33 10-5 S.
constante de cellule : k = d/S = 0,01 / 1,1 10-4 = 90,9 m-1.
conductivité s = kG = 90,9 *8,33 10-5 = 7,57 10-3 Sm-1.
CH3-CH2-COO H + H2O=CH3-CH2-COO-+H3O+
[CH3-CH2-COO-] =[H3O+]= t c0 ; [CH3-CH2-COO H ]=(1-t )c0
s =[l(CH3-CH2-COO-) + l(H3O+) ] t c0 ; avec c0 = 3 10-3 *103 = 3 mol/m3.
t =s / [[l(CH3-CH2-COO-) + l(H3O+) ] c0 ] = 7,57 10-3 / [(35+3,6)10-3*3]=0,065.
Ka = [CH3-CH2-COO-] [H3O+] / [CH3-CH2-COO H ] = t² c0 / (1-t ) = 0,065² *3 10-3 / (1-0,065) = 1,36 10-5.
- Le benzoate de méthyle, à odeur
d'oeillet, est utilisé en parfumerie. Pour le
synthétiser, on chauffe à reflux, sous la
hotte pendant environ une heure 12,2 g d'acide
benzoïque C6H5COOH, 40 mL de
méthanol et 3 mL d'acide sulfurique. Après
refroidissement du mélange réactionnel, on
verse celui-ci dans une ampoule à décanter
contenant 50 mL de solution saturée de chlorure de
sodium. Après séparation des deux phases,
lavage, séchage de la phase organique , on
récupère par distilation une masse finale
mf=10,2 g de benzoate de
méthyle.
Quel est le rendement de cette synthèse ?composé acide benzoïque méthanol benzoate de méthyle M(g/mol) 122 32 136 m(g/cm3) 1,321 0,791 1,089
60 % ; 30 % ; 100 % ; 25 % ; 50 % ; 75 %. - La réaction entre l'acide butanoïque et
le pentan-1-ol permet d'obtenir un ester le butanoate de
pentyle de formule brute
C9H18O2, dont l'odeur
rappelle celle de l'abricot. Le taux d'avancement final
de la réaction est 0,67 à partir d'un
mélange équimolaire (n0= 100
mmol) d'acide et d'alcool maintenu à la
température de 50°C avec un montage à
reflux.
- Quelle est la valeur de la constante d'équilibre de la réaction ?
0,25 ; 61,5 ; 0,016 ; 4 ; 0,67 ; 2.
corrigé
Qté de matière : acide benzoïque 12,2 / 122 = 0,1 mol
alcool : masse = 40*0,791 = 31,64 g ; 31,64 / 32 = 0,988 mol (en excès)
Qté de matière théorique d'ester : 0,1 mol soit 0,1*136= 13,6 g
rendement = masse expérimentale / masse théorique = 10,2 / 13,6 = 0,75 (75%)
acide + alcool = ester + eau
K= [ester]éq[eau]éq/([acide]éq[alcool]éq)
[ester]éq=[eau]éq= tc ; [acide]éq=[alcool]éq=(1-t)c
K= (tc)² / ((1-t)c)² = t² / (1-t)²= 0,67 ² / (1-0,67)² = (0,67/0,33)² = 4.
- On réalise l'électrolyse d'une solution
de nitrate d'argent avec des électrodes
inattaquables de graphite. On observe à l'anode
l'oxydation de l'eau en dioxygène et à la
cathode un dépôt d'argent.
L'électrolyse dure 15 min, l'intensité du
courant étant maintenue constante et égale
à 0,08 A
Données : 1 Faraday = 96 500 C ; M(Ag= = 107,9 g/mol.
- Quelle est la masse (mg) du dépôt d'argent à la cathode ?
81 ; 40 ; 162 ; 20 ; 12,5 ; 10,8.
- Quelle est la quantité (mmol) du gaz formé à l'anode ?
0,75 ; 0,19 ; 1,5 ; 0,09 ; 3 ; 0,37. - On réalise une pile cadmium argent contenant
les couples oxydo-réducteur Ag+/Ag ;
Cd2+/ Cd.Les solutions électrolytiques
ont une concentration initiale en ion métallique
égale à 0,15 mol/L. La partie
immergée de l'électrode de cadmium a une
masse de 3g. Lorsque la pile fonctionne, la masse de
l'électrode de cadmium diminue et il se forme un
dépôt d'argent sur l'électrode
d'argent.
Données : Cd=112,4 ; Ag=108 g/mol.
- Quel est l'avancement de la réaction (mol) lorsque tout le cadmium immergé est consommé ?
1 ; 0,15 ; 0,5 ; 0,027 ; 0,30 ; 0,96.
- Quelle est la masse d'argent (g) formée sur la partie immergée de l'électrode d'argent ?
5,8 ; 3 ; 1,6 ; 6 ; 2,9 ; 2,1.
corrigé
Ag++ e- --> Ag à la cathode.
Qté d'électricité Q=I t = 0,08*15*60 = 72 C
Qté de matière d'électron = Qté de matière d'argent = 72/96500 = 7,46 10-4 mol.
masse d'argent : 7,46 10-4 *107,9 = 0,08 g = 80 mg.
à l'anode H2O--> ½O2 + 2H++2e-.
Qté de matière de dioxygène = 0,25 fois la qté de matière d'électrons
7,46 10-4 *0,25 = 1,86 10-4 mol = 0,186 mmol.
Cd + 2Ag+ --> Cd2+ + 2Ag
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
xfin =0,0267 mol |
|
|
masse d'argent déposé = 0,053*107,9 = 5,76 g.