|
l'atome ; radioactivité d'aprčs DTS IMRT 04 En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées ŕ vos centres d’intéręts. |
|||||||||||||||||||||
| .
. |
|||||||||||||||||||||
|
|||||||||||||||||||||
|
Répondre par vrai ou faux. (une seule affirmation est vraie) Les orbites électroniques de l'atome correspondent : A- ŕ des niveaux d'énergie d'autant plus bas que ces orbites sont plus proches du noyau. Vrai. B- ŕ des niveaux d'énergie d'autant plus haut que ces orbites sont plus proches du noyau. Faux Les énergies de l'atome sont négatives. C- ŕ des niveaux équidistants les uns des autres. Faux.
A- l'énergie de liaison d'un électron de la couche K est inférieure ŕ l'énergie de liaison d'un électron de la couche L. Faux. Un électron de la couche K est plus lié au noyau qu'un électron de la couche L : il faut dépenser davantage d'énergie pour l'arracher. B- l'énergie de liaison d'un électron de la couche K est pour tous les atomes égale ŕ -13,6 eV . Faux. C- l'énergie d'ionisation est l'énergie qu'il faut fournir pour extraire un électron de l'atome. Vrai.
A-
sur les valeurs
énergétiques des niveaux
électroniques car les longueurs d'onde des
raies émises sont proportionnelles ŕ
la différence des niveaux
d'énergie.
Faux. Ej-Ei =
hc/l. Plus la différence d'énergie est
grande, plus la longueur d'onde est petite. B-Certaines
raies ont la męme position dans le spectre
pour des atomes situés dans la męme
colonne de la classification
périodique.
Vrai. Pour que les raies K apparaissent dans le spectre des RX, il faut que l'énergie des électrons incidents soit : A-égale ou supérieure ŕ l'énergie de liaison des électrons de la couche K. Vrai. B-
inférieure ŕ
l'énergie de liaison des électrons de la
couche K.
Faux.
A-d'un choc d'un électron trčs énergétique sur le noyau de césium. Faux. B- du retour au niveau fondamental du noyau fils excité. Vrai. C-d'une
dématérialisation du noyau de
césium.
Faux.
Définir défaut de masse : Défaut de masse du noyau D m : expérimentalement, on a constaté que la masse du noyau atomique est inférieure ŕ la somme des masses des nucléons qui le constituent. On appelle défaut de masse d'un noyau la différence entre la masse totale des A nucléons séparés ( Z protons et A-Z neutrons), au repos et la masse du noyau formé, au repos Définir énergie de liaison d'un noyau : Énergie de liaison du noyau : on appelle énergie de liaison notée El d'un noyau l'énergie que doit fournir le milieu extérieur pour séparer ce noyau au repos en ses nucléons libres au repos.
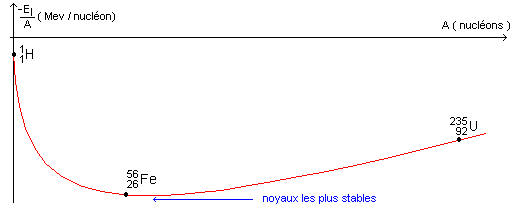
La courbe d'Aston donne l'énergie de liaison par nucléon en fonction du nombre de masse. Oů sont situés les noyaux stables ? Quels noyaux peuvent conduire ŕ une réaction de fusion ? Quels noyaux peuvent conduire ŕ une réaction de fission ?
La fission est une réaction nucléaire provoquée au cours de laquelle un noyau lourd "fissible" donne naissance ŕ deux noyaux plus légers. La réaction se fait avec perte de masse et dégagement d'énergie.
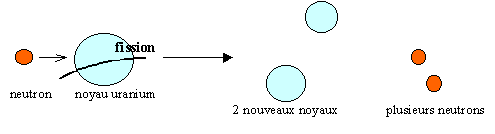
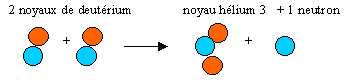
La fusion nucléaire est une réaction au cours de laquelle deux noyaux légers s'unissent pour former un noyau plus lourd. La réaction se fait avec perte de masse et dégagement d'énergie.
L'iode 12553I se désintčgre par capture électonique avec émission de photons et d'électrons. D'oů provient l'électron capturé par le noyau ? Quelle est l'origine de l'électron expulsé ? Ecrire l'équation de la réaction nucléaire de capture électronique. Un noyau atomique capture un électron situé sur une couche électronique interne de l'atome. Un proton se transforme alors en neutron : 11p + 0-1 e = 10n + neutrino. Un électron d’une couche de plus haute énergie peut venir remplir cette place vacante ( par capture électronique) : il en résulte un dégagement d’énergie. Cette énergie peut : - Causer l’émission d’un photon X : fluorescence X - Etre absorbée par un électron qui sera éjecté de l’atome (électron Auger)
Calculer leur constante radioactive en s-1. lT = ln2 ; l1 = ln2 / T1 = ln2 / (74*24*3600) =1,08 10-7 s-1. l2 = ln2 / T2 = ln2 / (18*3600) =1,07 10-5 s-1. Quel est de ces deux isotopes, celui qui sera éliminé le plus rapidement ? Justifier. Loi de décroissance radioactive : N1 = N01 exp(-l1t) ; N2 = N02 exp(-l2t) ln ( N1 / N01 ) =- l1t ; ln ( N2 / N02 ) =- l2t ; ln ( N1 / N01 ) -ln ( N2 / N02 ) =(l2 -l1) t (l2 -l1) est positif donc ln ( N1 / N01 ) > ln ( N2 / N02 ) ; Le logarithme est une fonction croissante : N1 / N01 >N2 / N02. L'isotope qui possčde la plus grande constante radioactive est éliminé le plus rapidement.
Définir l'activité et donner son expression en fonction du nombre de noyaux radioactifs. Activité en Bq : A: nombre de désintégrations par seconde. A = l N = A0 exp(-lt) avec A0 = l N0. Quelle était son activité ŕ 12 heures ? 18-12 = 6 heures; au bout d'une période, l'activité diminue de 50 % ; l'activité ŕ 12 h était : 80 MBq. Quelle sera son activité le lendemain ŕ 18 heures ? 24 h = 4 périodes ; au bout de 4 périodes l'activité vaut A0 / 24 = A0 /16 =0,0625 A0 = 0,0625*40 =2,5 MBq.
|
|||||||||||||||||||||
|
|
|||||||||||||||||||||
|
|