|
Dissolution de la silice dans l'eau ; polymčres : concours général 2006 En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées ŕ vos centres d’intéręts. |
|||||||
| .
. |
|||||||
|
|||||||
|
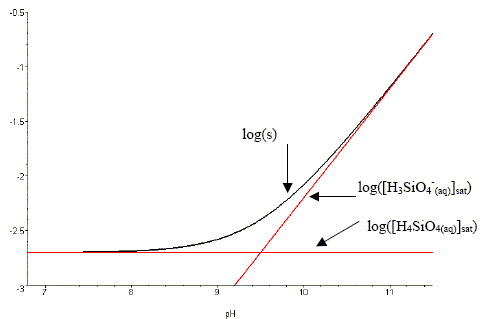
La solubilité de la silice pure amorphe est caractérisée par la réaction chimique suivante : SiO2(s) + 2H2O = H4SiO4 (aq) ; constante d'équilibre associée K = 10-2,7. Concentration de la silice dissoute ŕ 25 °C. K = [H4SiO4 (aq) ]éq = 10-2,7 = 2 10-3 mol/L. Masse maximale de silice pure amorphe que l'on peut dissoudre dans 1 L d'eau ŕ 25 °C. Masse molaire de la silice SiO2(s) : 28,1+2*16 = 60,1 g/mol Quantité de matičre (mol) dans 1 L : 2 10-3 mol masse m(g) = n(mol) * M (g/mol) = 2 10-3 *60,1 = 0,12 g. La solubilité de la silice dépend du pH du fait du caractčre acide de H4SiO4 (aq) ; on suppose que le seul couple acide base mis en eu est : H4SiO4 (aq) / H3SiO4- (aq). La solubilité s de la silice est définie comme la quantité de matičre maximale que l'on peut dissoudre par litre d'eau ( on dit alors que la solution est saturée en silice). s = [H4SiO4 (aq)] +[H3SiO4- (aq)] La figure suivante représente l'évolution du logarithme décimal des deux concentrations [H4SiO4 (aq)]sat, [H3SiO4- (aq)]sat et de la solubilité s, exprimées en mol/L, en fonction du pH ŕ 25°C.
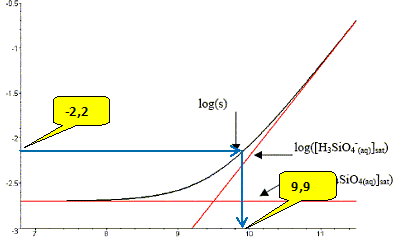
En milieu acide la solubilité est indépendante du pH. Definition et détermination graphique du pKa du couple H4SiO4 (aq) / H3SiO4- (aq). H4SiO4 (aq) + H2O = H3SiO4- (aq) + H3O+(aq) Constante d'acidité Ka = [H3SiO4- (aq)][H3O+(aq)] / [H4SiO4 (aq)] ; pKa = - log Ka. Lorsque [H3SiO4- (aq)] = [H4SiO4 (aq)] alors pH = pKa. On lit le pH correspondant ŕ l'intersection des deux droites rouges : pKa = 9,5. On désire dissoudre entiérement 0,38 g de silice solide dans 1 L d'eau ŕ 25°C. Déterminer graphiquement ŕ partir de quel pH cela est possible. s = m/M =0,38 / 60,1 = 6,3 10-3 mol/L ; log s = -2,2.
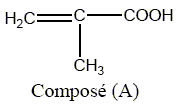
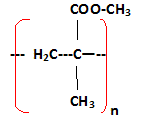
Le coeur et la gaine optique en silice doivent ętre protégés des attaques extérieures ( eau, griffure, cassage...). On procčde ŕ un enrobage par un polymčre de type acrylique. Définition d'un polymčre : macromolécule résultant de l'association par liaison covalente d'un grand nombre de molécules identiques ( monomčre). Les polymčres acryliques dérivent de l'acide acrylique et de l'acide méthacrylique, noté A.
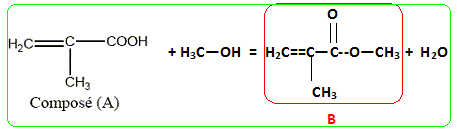
La réaction de A avec le méthanol donne le monomčre, noté B, du polyméthacrylate de méthyle ( PMMA). Quels groupes caractéristiques distingue t-o dans le composé A ? groupe acide carboxylique COOH et fonction alcčne ( double liaison entre deux atomes de carbone)
|
|||||||
|
|
|||||||
|
|