|
Acide valťrique concours kinť Ceerrf 2009.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
|||||||
| .
. |
|||||||
|
|||||||
|
M= 102 g/mol ; tempťrature de fusion : -35 įC ; tempťratue d'ťbullition : 186 įC ; densitť ŗ 20 įC : d = 0,94 ; solubilitť dans l'eau ŗ 20 įC : s = 33 g/L. Dans l'industrie on synthŤtise l'acide valťrique par oxydation mťnagťe d'un alcool qu'on notera B. Le nom courant de B est alcool "amylique", sa formule est C5H12O et sa chaine carbonťe est linťaire. Donner le nom et la formule d'un rťactif qui pourrait permettre l'oxydation mťnagťe de B en AH. Permanganate de potassium en milieu acide ; KMnO4. Expliquer pourquoi B ne peut Ítre que le pental-1-ol, d'aprŤs ce qui est ťcrit plus haut. La chaine carbonťe est linťaire et seul un alcool primaire peut conduire par oxydation mťnagťe ŗ un acide carboxylique.
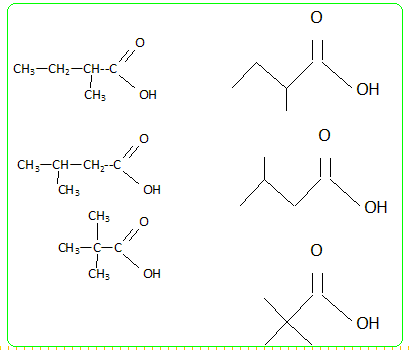
CH3-CH2-CH2-CH2-COOH
acide pentanoÔque CH3-CH2-CH (CH3)-COOH acide 2-mťthylbutanoÔque CH3-CH (CH3)-CH2-COOH acide 3-mťthylbutanoÔque (CH3)3C-COOH acide 2,2-dimťthylpropanoÔque.
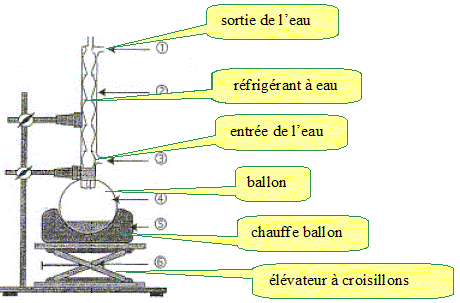
Pour extraire l'acide valťrique de la racine de valťriane on propose le protocole suivant : Etape 1 : introduire dans un ballon la racine de valťriane hachťe menu, ajouter 100 mL d'eau et des grains de pierre ponce. Placer le ballon dans un chauffe ballon et surmonter le ballon d'un rťfrigťrant ŗ eau. Etape 2 : porter le mťlange ŗ ťbullition et maintenir l'ťbullition durant 30 min. Etape 3 : refroidir ŗ 20 įC puis filtrer le contenu du ballon. Faire un schťma du montage de l'ťtape 2 en indiquant le sens de circulation de l'eau dans le rťfrigťrant. Comment s'appelle ce montage ? Chauffage ŗ reflux :
Etablir l'expression de la concentration c de la solution S en fonction de V, c' et VE. En dťduire la valeur de c. AH + HO- = A- + H2O. A l'ťquivalence les quantitťs de matiŤre des rťactifs mis en prťsence sont en proportions stoechiomťtrique cV = c' VE ; c = c' VE /V = 1,00 10-2 * 9,2 / 10 = 9,2 10-3 mol/L. L'acide valťrique utilisť ťtait -il rťellement pur ? Justifier. masse d'acide AH dans 1 mL : volume (mL) * densitť = 1,00 */ 0,94 = 0,94 g n=m/M = 0,94 / 102 = 9,2 10-3 mol dans 1 L : l'acide AH est pur.
|
|||||||
|
c |
|||||||
|
|