|
Pile, ťlectrolyse, transformations inversables concours kinť Ceerrf 2009.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
On considŤre la transformation modťlisťe par l'ťquation : Ni(s) + Cu2+aq = Cu(s) + Ni2+aq de constante d'ťquilibre K = 2 1019. Les solutions utilisťes ont toutes deux les concentrations de 0,10 mol/L en ions Cu2+aq et Cu2+aq et un volume V = 200 mL dans chaque compartiment. Exprimer puis calculer le quotient de rťaction initial Qr i relatif ŗ l'ťquation ťcrite prťcťdemment. Qr i =[Ni2+aq]i / [Cu2+aq]i = 0,10 / 0,10 = 1. Dans quel sens va ťvoluer le systŤme si on relie les plaques mťtalliques par un conducteur ohmique ? Justifier. Qr i < K, donc ťvolution dans le sens direct. On fait dťbiter par la pile ainsi obtenue, un courant d'intensitť I= 20 mA pendant 10 heures. Quel est l'avancement de la rťaction au bout de cette durťe ? Aide au calcul : 72/193 = 0,37. Quantitť d'ťlectricitť : Q = I t = 0,02 * 10*3600 = 720 C Quantitť de matiŤre d'ťlectrons n(e-) = Q / 96500 = 720 / 96500 = 72 / 9650 mol Or Cu2+aq + 2e- = Cu(s) d'oý la quantitť de matiŤre de cuivre : n(Cu(s) = Ĺn(e-) = 72/( 2*96,5*100) = 72 / 193 10-2 = 3,7 10-3 mol. L'avancement est ťgal ŗ la quantitť de matiŤre de cuivre formť : x = 3,7 10-3 mol. 0,02-3,7 10-3 =0,0163 = 0,0237 Calculer le quotient de rťaction final Q r 10 et le comparer ŗ Q r i et K. Faire un commentaire sur l'ťtat d'ťvolution du systŤme. Qr 10 =[Ni2+aq]f / [Cu2+aq]f = 0,1185 / 0,0815 =1,45 ~ 1,5. Valeur supťrieure ŗ Qr i mais infťrieur ŗ K : le systŤme va encore ťvoluer dans le sens direct tant que le circuit extťrieur sera fermť.
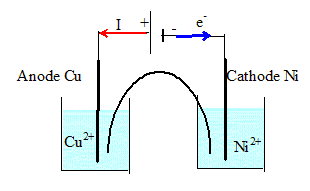
Au bout de ces 10 heures de fonctionnement on veut rťaliser la transformation inverse de celle qui a ťtť effectuťe ci-dessus. Ecrire son ťquation. Cu(s) + Ni2+aq = Ni(s) + Cu2+aq de constante d'ťquilibre 1/ K = 1/ 2 1019 =5 10-20. Faire un schťma lťgendť du montage en prťcisant la nature des pŰles de chaque dipŰle.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
c |
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|