|
Alcools ŕ 4 atomes de carbone, hydratation alcčne ; hydrolyse d'un ester concours kiné 2009.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées ŕ vos centres d’intéręts. |
|||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
Analyse : la classe des alcools. B-
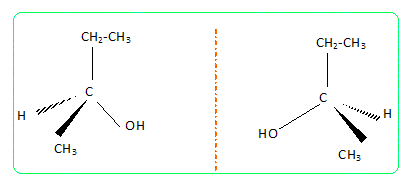
Analyse : le nombre d'isomčres. Le butan-2-ol possčde un carbone asymétrique, d'oů le couple d'énantiomčres :
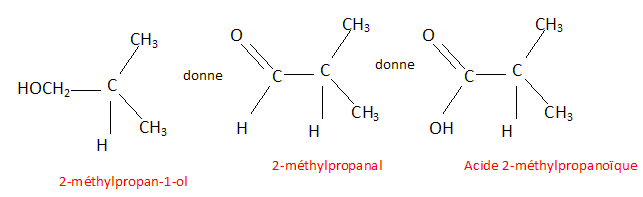
Donc au total 5 isomčres de formule brute C4H10O. Analyse : oxydation ménagée. La chaîne carbonée n'est pas modifiée. E- Un alcool secondaire ( butan-2-ol) donne une cétone ( butan-2-one). Un alcool primaire conduit ŕ un aldehyde puis ŕ un acide carboxylique. C-
La formule brute d'un alcčne est
CnH2n avec n entier
supérieur ŕ 1. Analyse : addition
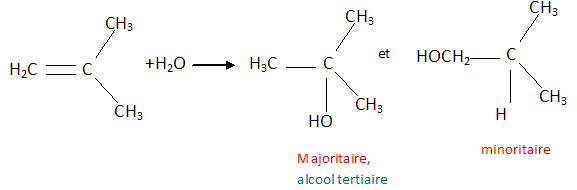
d'eau. L'addition d'eau, catalysée par l'acide
sulfurique, sur un alcčne
disymétrique au niveau de la double liaison
conduit ŕ deux alcools. B-
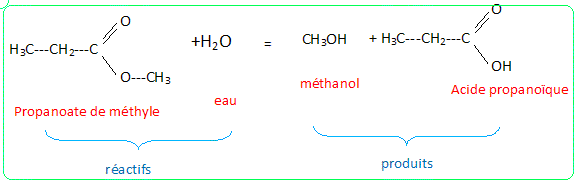
Hydrolyse d'un ester : D-
L'acide sulfurique catalyse cette hydrolyse. Analyse : rendement.
rendement : xf / xmax *100 = 0,66 / 2 *100 = 33 %.
|
|||||||||||||||||||||||||||||||
|
c |
|||||||||||||||||||||||||||||||
|
|