|
Acide base : pH, conductivitť ; oxydorťduction : pile, ťlectrolyse concours kinť 2009.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
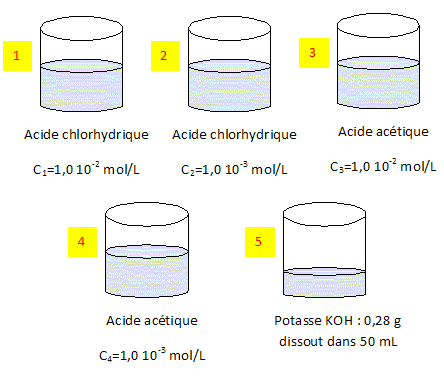
Analyse : acide faible, acide fort. A-C-E- L'acide chlorhydrique est "fort", entiŤrement dissociť dans l'eau ; pKa ( H3O+ / H2O = 0) Le pH de la solution (1) est ťgal ŗ : pH =-log c = - log 10-2 = 2. L'acide acťtique ( ťthanoÔque) est "faible", partiellement dissociť dans l'eau : pKa ( CH3COOH / CH3COO- = 4,8) Le pH de la solution (3) vaut : pH = pKa + log ([CH3COO-] /[CH3COOH]). A concentration ťgale, un acide est d'autant plus fort que son pKa est plus petit ; le pH de la solution (3) est supťrieur au pH de la solution (2). Analyse : dilution. B- En diluant 10 fois la solution (1) on obtient la solution (2) ; en diluant 10 fois un acide fort de concentration 0,01 mol/L, le pH augmente de log 10 = 1 unitť. D- En diluant 10 fois la solution (3) on obtient la solution (4) ; en diluant 10 fois un acide faible de concentration 0,01 mol/L, le pH augmente de moins de 1 unitť. Le pH de la solution (3) est donc plus petit que celui de la solution (4). La potasse ( solution 5 ) est entiŤrement
dissociťe dans l'eau : c'est une base
forte. pH = 14 + log
c. Masse molaire KOH : M = 39 + 16+1 = 56
g/mol. Quantitť da matiŤre ; n = m / M =
0,28 / 56 = 0,005 mol Concentration c = n / V = 0,005 / 0,05 = 0,1
mol/L pH ( solution 5) = 14 + log 0,1 = 14-1 =
13. Analyse : conductivitť. L'acide faible notť AH est partiellement dissociť dans l'eau ; la base conjuguťe est notťe A- ; le tableau suivant est rťalisť pour un volume V = 1 L de solution.
[A-]f=[H3O+]f = xf /V mol/L = 103xf /V mol m-3. s = lA- [A-]f + lH3O+ [H3O+]f = ( lA- + lH3O+ ) [H3O+]f =0,02 S m-1. On donne ( lA- + lH3O+ ) = 4,0 10-2 S m2 mol-1. [H3O+]f =0,02 / 0,04 = 0,50 mol m-3 = 5,0 10-4 mol /L. Analyse : taux d'avancement final. t = [H3O+]f / c = 5,0 10-4 / 1,0 10-3 = 0,5.
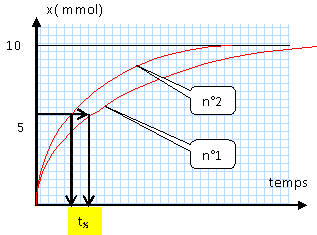
Zinc (mťtal) et solution de diiode : Zn (s) + I2(aq) = Zn2+(aq) + 2I-(aq) Le zinc mťtal oxyde lentement le diiode, seule espŤce colorťe. Le diiode ťtant l'un des rťactifs, la teinte jaune brune de la solution s'attťnue lentement.
A- A concentration ťgale, la rťaction est d'autant plus rapide que la tempťrature est plus ťlevťe. La solution 4 se dťcolore trŤs vite, par rapport ŗ la solution 1. Analyse : facteur cinťtique, la concentration d'un rťactif. F- A tempťrature identique, la rťaction est d'autant plus rapide que la concentration initiale en diiode est plus ťlevťe. En cours de rťaction, la concentration en diiode diminue, la vitesse de la rťaction diminue donc au cours du temps. Analyse : temps de demi-rťaction. Durťe au bout de laquelle l'avancement est ťgal ŗ la moitiť de l'avancement final. Ici la rťaction est totale, l'avancement final est ťgal ŗ l'avancement maximal. C- D - expťrience nį1 : 25įC et conditions stoechiomťtriques, xf = 10 mmol et xtĹ = 5 mmol. expťrience nį2 : 25įC, le zinc est le rťactif limitant et le diiode est en excŤs, xf = 10 mmol et xtĹ = 5 mmol.
Analyse : concentration finale en ion iodure. B- expťrience nį1 : 25įC et conditions stoechiomťtriques, xf = 10 mmol et n(iodure) =2 xf = 20 mmol. expťrience nį3 : 25įC, le zinc est le rťactif limitant et le diiode est en excŤs, xf = 10 mmol et n(iodure) =2 xf = 20 mmol.
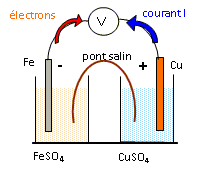
Pile
Le fer est oxydť et libŤre des ťlectrons ; le fer constitue l'anode nťgative de la pile : Fe(s) = Fe2+(aq) + 2e-. Les ions cuivre Cu2+(aq) sont rťduits ŗ la cathode positive : Cu2+(aq) + 2e- = Cu(s) Bilan : Fe(s) + Cu2+(aq) = Fe2+(aq) +Cu(s). C-E- La masse de l'ťlectrode de fer diminue, la masse de l'ťlectrode de cuivre augmente.
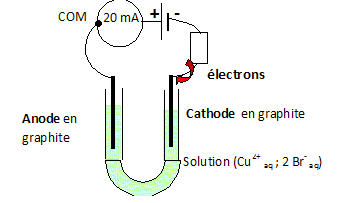
Ion hypochlorite ClO- et ion iodure I-.
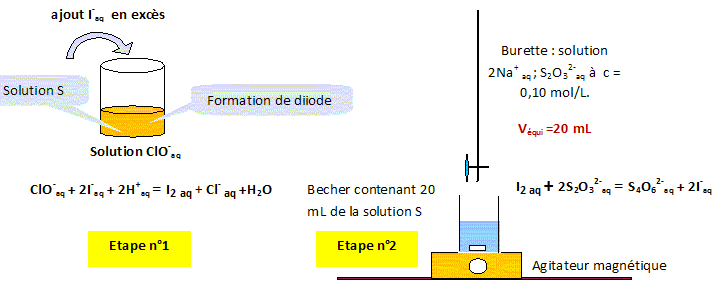
Analyse : dosage indirect : On rťalise un dosage indirect si la rťaction support du dosage n'est pas suffisamment rapide ou bien si l'on ne possŤde pas d'indicateur colorť mettant en ťvidence le point ťquivalent. Ce type de dosage met en oeuvre deux rťactions rapides. Analyse : indicateur colorť, ťtape nį2 : Le diiode est la seule espŤce colorťe ( teinte jaune brune ) ; en prťsence de diiode, l'empois d'amidon donne une teinte violette assez foncťe. Avant l'ťquivalence le diiode est en excŤs ( teinte violette) AprŤs l'ťquivalence toutes les espŤces sont incolores. B- A l'ťquivalence la teinte passe du violet ŗ l'incolore. Analyse : concentration en ion hypochlorite : Etape nį2 : ŗ l'ťquivalence n(I2) = 0,5 n(S2O32-) ; n(I2) = 0,5 * c Vťqui = 0,5*0,1 * 20 10-3 =1,0 10-3 mol. n(I2) =1,0 10-3 mol dans 20 mL de la solution S. [I2] = 1,0 10-3 / 20 10-3 =0,05 mol/L. C- Etape nį1 : les nombres stoechiomťtriques indiquent [I2] =[ClO-] = 0,05 mol/L.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
c |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||