|
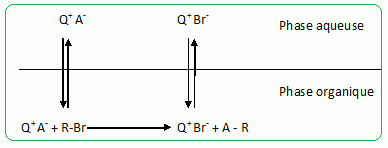
SynthŤse d'un ťtheroxyde : catalyse par transfert de phase concours Mines 2009. |
||||||||||||||||||
| .
. |
||||||||||||||||||
|
||||||||||||||||||
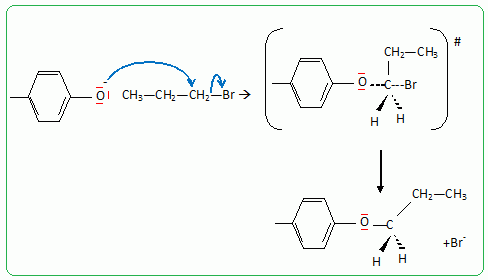
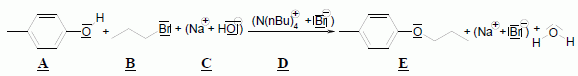 Pour rťaliser la synthŤse de l’ťtheroxyde E, on introduit dans un ballon : • 8,00 g de 4-mťthylphťnol A (soit 7,41.10-2 mol) ; • 9,10 g de 1-bromopropane B (soit 7,40.10-2 mol) ; • 3,00 g d’hydroxyde de sodium C (soit 7,50.10-2 mol) dans 10,0 mL d’eau ; • 0,20 g de bromure de tťtrabutylammonium (N(C4H9)4+ + Br-) D (soit 6,2.10-4 mol) dont le rŰle sera expliquť dans la partie suivante. On rťalise alors un montage ŗ reflux et on agite vigoureusement le milieu rťactionnel, constituť de deux phases : une phase organique (qui contient A, B et E) et une phase aqueuse (qui est constituťe de la solution d’hydroxyde de sodium C). Prťciser l’intťrÍt du montage ŗ reflux. Le montage ŗ reflux permet d'accťlťrer la rťaction en travaillant ŗ tempťrature modťrťe, tout en ťvitant les pertes de matiŤre : les vapeurs se condensent dans le rťfrigťrant ŗ eau et retombent dans le milieu rťactionnel. Alors que le pKa d’un couple alcool/alcoolate est couramment compris entre 16 et 18, celui d’un couple phťnol/phťnolate est situť entre 8 et 10. Le composť A peut donc Ítre dťprotonť par la solution d’hydroxyde de sodium. Proposer une justification ŗ cette diffťrence de pKa. L'ion phťnolate est stabilisť par rťsonance : sa charge est dťlocalisťe sur le cycle benzťnique. Il n'en est pas de mÍme pour l'ion alcoolate. Le proton du groupe phťnol est donc plus acide que le proton d'une fonction alcool. Indiquer une mťthode qui aurait permis de dťprotoner un alcool comme l’ťthanol. Lťthanol peut Ítre dťprotonť par une base forte comme l'hydrure de sodium NaH. Nommer cette rťaction de synthŤse d’ťtheroxyde puis proposer un schťma rťactionnel expliquant la formation de E. C'est une synthŤse d’ťther selon la mťthode de Williamson. Le phťnolate rťagit avec le bromopropane par une rťaction de substitution nuclťophile de type SN2.
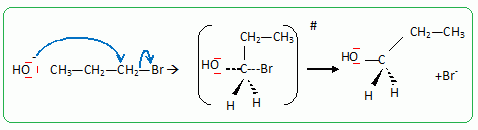
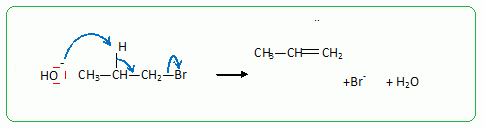
Passage au propan-1-ol par une rťaction de substitution nuclťophile de type SN2.
Dans une ampoule ŗ dťcanter on sťpare les espŤces solubles dans la phase aqueuse et les espŤces solubles dans le diethylťther ( le diťthylether et l'eau n'ťtant pas miscibles ). Le lavage ŗ l'hydroxyde de sodium ťlimine les traces de A et B en donnant l'ťtheroxyde E.
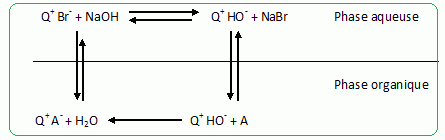
Principe de la catalyse par transfert de phase. On cherche ŗ expliquer le rŰle de catalyseur par transfert de phase jouť par le bromure de tťtrabutylammonium dans la synthŤse de l’ťtheroxyde E. Pour cela, on analyse le mode opťratoire suivant : Dans un tube ŗ essai, on obtient une solution violette aprŤs avoir introduit quelques cristaux de permanganate de potassium KMnO4 et 1 mL d'eau. On ajoute alors 1 mL de dichloromťthane CH2Cl2 ; aprŤs agitation, la phase organique est incolore. On ajoute alors quelques cristaux de bromure de tťtrabutylammonium (espŤce incolore dans l’eau et le dichloromťthane). AprŤs agitation, la phase organique devient colorťe. 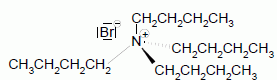 Dťterminer les configurations ťlectroniques fondamentales de l’oxygŤne (Z=8) et du manganŤse (Z = 25). Indiquer pour chacun de ces deux ťlťments le nombre d’ťlectrons de valence. Atome d'oxygŤne : 1s2 2s2 2p4 ( 6 ťlectrons de valence). Atome de manganŤse : 1s2 2s2 2p6 3s2 3p6 4s2 3d5 (2+5 = 7 ťlectrons de valence). En dťduire une formule de Lewis reprťsentative de l’ion permanganate MnO4-, et prťvoir sa gťomťtrie ŗ l’aide de la mťthode VSEPR. On prťcisera en particulier la valeur de l’angle entre deux liaisons ManganŤse-OxygŤne. 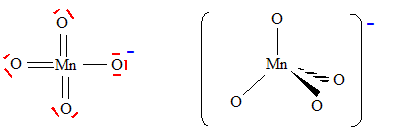 TťtraŤdre rťgulier ( les anglex valent 109į ) ; type AX4. Proposer les formules mťsomŤres les plus reprťsentatives de l’ion permanganate. Que peut-on dire des longueurs des liaisons ManganŤse-OxygŤne ? 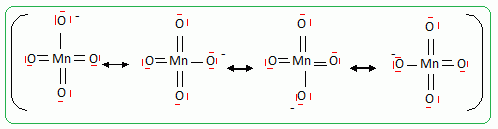 Les liaisons ont des longueurs intermťdiaires entre celles des liaisons simples et celles des liaisons doubles.
|
||||||||||||||||||
| |
||||||||||||||||||
|
|