|
Etude du biogaz de dťcharge, chimie concours Mines 08
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
|||||||||||||||||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||
|
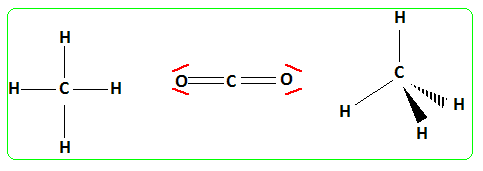
…tude de la rťaction de mťthanation du glucose. Les glucides ťtant des molťcules basťes sur le glucose de formule brute C6H12O6, nous ťtudierons ici sa dťcomposition. …crire l’ťquation de la transformation de glucose en mťthane et dioxyde de carbone. C6H12O6 = 3CH4 + 3CO2. Proposer une reprťsentation de Lewis pour les molťcules de mťthane et de dioxyde de carbone. Proposer une structure spatiale pour chacune de ces deux molťcules (indiquer les valeurs des angles de liaison).
Dans la structure tťtraŤdrique
rťguliŤre du mťthane, les anles
mesurent 109,28į. CO2 est linťaire,
les angles mesurent 180į.
Hormis quelques
applications pour lesquelles le biogaz peut
Ítre utilisť directement, il est
gťnťralement purifiť.
L’ťpuration consiste ŗ
ťliminer les ťlťments trace
(H2S, H2O) mais
ťgalement le dioxyde de carbone afin
d’enrichir le biogaz en mťthane.
L’ťpuration se fait
gťnťralement ŗ des pressions
de quelques dizaines de bars, nous prendrons ici
une pression P = 10 bar. La composition molaire du
biogaz considťrť est : CH4
: 60 %, CO2 : 39 %, H2S :
0,10 % et H2O : 0,90 %
. L’eau liquide peut dissoudre le dioxyde de carbone. Elle est en gťnťral ťliminťe par condensation ou par passage dans un dessicateur. La dissolution du dioxyde de carbone est telle que la concentration en CO2(d) dissous est proportionnelle ŗ la pression partielle en CO2(g) suivant la loi : [CO2(d)] = KCO2 PCO2/Pį . cį. (on rappelle que cį = 1,00 mol.L-1 et Pį = 1,00 bar). Au cours du trajet du biogaz et compte tenu de variations de tempťrature ťventuelles, l’eau peut se condenser en gouttelettes. On donne la valeur numťrique de la constante ŗ 300 K : KCO2= 2,5.10-2. Pour l’ťtude qui suit, la pression et la tempťrature sont constantes et valent : P = 10 bar et T = 300 K. Exprimer puis calculer la concentration en CO2(d) des gouttelettes d’eau en contact avec le dioxyde de carbone. Afin de simplifier les calculs numťriques, vous pourrez arrondir le pourcentage ŗ 40 %. PCO2 = fraction molaire CO2 * pression totale = 0,39 P = 0,39*10 = 3,9 bar ~ 4 bar. [CO2(d)] = KCO2 PCO2/Pį . cį = 2,5.10-2*3,9 ~ 0,10 mol/L. En dťduire le pH de cette
solution. On
nťgligera les propriťtťs acido-basiques
des constituants chimiques autres que le dioxyde de
carbone. 4 10-7(0,10-xťq ) = x2ťq ; x2ťq +4 10-7xťq -4 10-8=0 ; xťq ~2,0 10-4 mol/L ; pH = -log [H3O+] = - log (2,0 10-4) = 3,7. les gouttes d'eau prťsentes dans le biogaz sont acides : ces gouttes sont un peu corrosives , il vaut donc mieux ťliminer l'eau du biogaz.
…limination du sulfure de dihydrogŤne. Afin d’ťliminer ťgalement le sulfure de dihydrogŤne, on peut laver le gaz avec une solution contenant des amines. On utilise ici une solution de concentration c = 0,10 mol.L-1 en diťthanolamine (DEA) de formule HN(CH2CH2OH)2. La dissolution du sulfure de dihydrogŤne est similaire ŗ celle du dioxyde de carbone. La constante vaut KH2S = 1,0.10-1. ņ l’aide de la constante KH2S, calculer la concentration en H2S(d) lorsque la solution est en ťquilibre avec le biogaz (H2S ŗ 0,10 %, pression totale P = 10 bar). La pression partielle en H2S est constante par apport continu de biogaz. PH2S = fraction molaire H2S * pression totale = 10-3 P = 10-3 *10 = 0,010 bar. [H2S(d)] = KH2S PH2S/Pį . cį = 0,10*0,010 ~ 1,0 10-3 mol/L. …crire l’ťquation de la rťaction entre le sulfure de dihydrogŤne et la DEA. Calculer sa constante Kį. HN(CH2CH2OH)2 + H2S = H2N+(CH2CH2OH)2 +HS- ou DEA++ H2S =DEAH+ +HS- Kį = [DEAH+][HS-] /([H2S][DEA]) couples acide / base : H2S /HS- ; Ka1 = 10-7 = [HS-][H3O+] / [H2S] DEAH+ /DEA : Ka2 = 10-9 = [DEA][H3O+] / [DEAH+] par suite Kį =10-7 / 10-9 =100, valeur importante, la rťaction est totale ; H2S est ťliminť au fur et ŗ mesure de sa formation.
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|