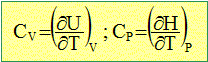|
Mesures thermodynamiques : calorimŤtre adiabatique, calorimŤtre ŗ basse tempťrature : physique concours Mines 08
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
|||||||||
| .
. |
|||||||||
|
|||||||||
|
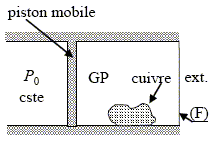
Expression du premier principe. Rappeler l’expression du premier principe de la thermodynamique, entre deux ťtats d’ťquilibre quelconques d’un systŤme fermť globalement immobile dans le rťfťrentiel d'ťtude. Expliquer trŤs simplement la diffťrence entre ę travail Ľ et ę transfert thermique Ľ. Lors de toute transformation, il y a conservation de l'ťnergie. Dans le cas des systŤmes thermodynamiques fermťs : La variation de l'ťnergie est ťgale ŗ la quantitť d'ťnergie ťchangťe avec le milieu extťrieur, sous forme de chaleur et sous forme de travail.. DU= W+Q. DU : variation d'ťnergie interne ; W : travail ťchangť, transfert ordonnť ; Q : chaleur ťchangťe, transfert microscopiquement dťsordonnť. On s’intťresse ŗ des systŤmes de variables d’ťtat (P, V, T), pour lesquels le seul travail est celui des forces pressantes ; ŗ partir de l’expression prťcťdente, dťmontrer la relation entre la variation d’enthalpie du systŤme et le transfert thermique dans le cas particulier de transformations isobares. dW = - PdV avec P = constante ; par suite W = -PDV. enthalpie : H = U+PV ; D H = D U +PDV = W + Q + +PDV = -PDV + Q + +PDV ; D H =Q. Calorimťtrie adiabatique. Le systŤme ťtudiť, constituť de n moles d’air assimilť ŗ un gaz parfait et d’une masse m de cuivre solide, est contenu dans un cylindre schťmatisť ci-dessous ; on prťcise que : • le piston est mobile sans frottement, les autres parois sont fixes ; • les ťlťments hachurťs sont athermanes (i.e. impermťables aux transferts thermiques), tandis que la paroi (F) permet ces tranferts. Coefficient de Laplace du gaz : g
= 1,4 ; R = 8,314 J K-1 mol-1
; n= 1 mole Capacitť thermique massique du cuivre : c
= 385 J.kg–1.K–1 ;
m = 269 g ; P0 est constante ; les valeurs de
g et c sont
indťpendantes de la
tempťrature. La capacitť thermique CV est l'ťnergie qu'il faut apporter ŗ un corps pour augmenter sa tempťrature de un Kelvin, le volume restant constant. La capacitť thermique CP est l'ťnergie qu'il faut apporter ŗ un corps pour augmenter sa tempťrature de un Kelvin, la pression restant constante. Elle s'exprime en Joule/Kelvin. C'est une grandeur extensive. Dans le cas d'un gaz parfait :
CV m : ťnergie nťcessaire pour ťlever la tempťrature d'une mole de corps pur de 1 kelvin, ŗ volume constant. CP m : ťnergie nťcessaire pour ťlever la tempťrature d'une mole de corps pur de 1 kelvin, ŗ pression constante. L'ťnergie interne d'un gaz parfait ne dťpend que de la tempťrature ; l'ťnergie interne d'une mole d'un gaz parfait monoatomique vaut U = 1,5RT. ( pour une mole d'un gaz diatomique U = 2,5 RT ) D'oý CV m = dU/dT = 1,5 R ( gaz monoatomique) et CV m = dU/dT = 2,5 R ( gaz diatomique) Pour une mole de gaz parfait : H= U+PV = U+ RT CP m = dH/dT = dU/dT +R ; CP m - CV m = R. Coefficient de Laplace du gaz : g =CP m /CV m ; g CV m- CV m = R ; CV m= R / (g-1). CP m = R+CV m =R+R/( g-1) ; CP m= g R / (g-1). La tempťrature extťrieure ťtant restťe trŤs longtemps ťgale ŗ T0, le fond (F) du cylindre est mis en contact avec une source (ou thermostat) ŗ la tempťrature T1 ; on laisse le systŤme atteindre l’ťquilibre. Le volume V occupť par le gaz subit une diminution relative de 5 % ŗ partir de la valeur initiale V0. En dťduire la tempťrature Celsius finale si q0 = 27 įC. La pression est constante. Pf = Pi ; Pi Vi = RTi ; Pf Vf = RTf ; Vi -Vf =R / Pi (Ti -Tf ) R / Pi = Vi / Ti d'oý : (Vi -Vf ) /Vi = (Ti -Tf ) / Ti = 0,05 Ti -Tf = 0,05 Ti ; Tf =0,95 Ti = 0,95(273,15+27) = 285 K ou ( 12įC).
En fonction des tempťratures et des donnťes, exprimer la variation d’enthalpie du systŤme lors de la transformation dťcrite ci-dessus, sous la forme DH = C'DT. Quelles propriťtťs essentielles de l’enthalpie utilise-t-on pour ťtablir cette expression ? L'enthalpie est une grandeur extensive : DH = DH(gaz) + DH (cuivre). L'enthalpie est une fonction d'ťtat, elle ne dťpend que des tempťrature initiale et finale : DH =(n CPM(gaz) + mc) DT. Or CP m= g R / (g-1) d'oý DH =(n g R / (g-1) + mc) DT. C' = n g R / (g-1) + mc. En dťduire l’expression du transfert thermique Q algťbriquement reÁu par le systŤme ŗ travers (F). Faire l’application numťrique et interprťter son signe. Q = DH= C' DT avec C' >0 et DT <0 : le systŤme cŤde de l'ťnergie au milieu extťrieur. g = 1,4 ; R = 8,314 J K-1 mol-1 ; n= 1 mole ; Capacitť thermique massique du cuivre : c = 385 J.kg–1.K–1 ; m = 269 g ; DT = -15 K. Q = ( 1,4*8,314/0,4 + 0,269*385) *(-15) =-1,99 ~ -2,0 kJ Exprimer et calculer la variation d’ťnergie interne DU du systŤme. Pour une mole de gaz parfait : H= U+PV = U+ RT DH= DU+ RDT ; DU = DH - RDT = -1,99 103 - 8,314 *(-15) = -1,87 kJ. DU = W+Q ; W =DU -DH= -1,99 +1,87 = 0,12 kJ W>0, le systŤme reÁoit du travail ; les forces pressantes extťrieures poussent le piston mobile. On rappelle des expressions usuelles de la fonction d’ťtat entropie S : SGP(T, V) = n CV m ln(T) + nT ln V + Cste ; SGP(T, P) = n CP m ln(T) - nT ln P + Cste ; Pour une phsase condensťe de capacitť C : Sphase condensťe (T) = C ln(T) + Cste.
phase (1) : entre t = 0 et t = t1, on
alimente une rťsistance R plongťe
dans le calorimŤtre : tension U et
intensitť I constantes ; phase (2) : le chauffage est coupť
ŗ t1 = 10 minutes. La masse M mesurťe en grammes est
enregistrťe ŗ intervalles
rťguliers de t = 0 ŗ t2 =
15 minutes (figure ci-contre : t en secondes) ; on
prťcise qu’ŗ tout instant il
reste de l’azote liquide dans le
rťcipient. La vapeur de diazote est en ťquilibre avec le liquide : la pression est constante ; appliquons la rŤgle des phases : v = c+2-j. 1 constituant, le diazote et une relation N2(liq) = N2 (g) soit c=0 ; 2 phases liquide et gaz : j = 2. La variance est nulle; la pression ťtant fixťe, la tempťrature reste constante soit 77,4 K. Pourquoi la masse diminue-t-elle mÍme en l’absence de chauffage ? Pourquoi est-il difficile de l’empÍcher ? L'ťcart de
tempťrature entre l'intťrieur du vase et
l'extťrieur est grand : il y a transfert thermique de
l'extťrieur vers l'intťrieur du vase. Une
partie du liquide s'ťvapore.
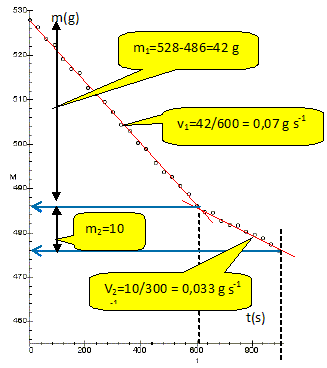
Pour chaque phase de l’expťrience, estimer la masse d’azote ťvaporť (m1 et m2). Calculer le rapport notť r des vitesses d’ťvaporation (phase1 / phase2). Voir graphe ci-dessus : r = 0,07 / 0,033 ~ 2,1. On dťsigne par PJ la puissance apportťe par effet Joule et par P celle des autres transferts thermiques, puissances algťbriquement reÁues par l’azote et supposťes constantes. …tablir pour chaque phase de l’expťrience une relation entre m1, m2, Lv, PJ, P et les dates nťcessaires. Phase 1 : puissances reÁues par le diazote : PJ+ P ; cette puissance reÁue permet l'ťvaporation du diazote pendant 600 s : m1Lv/600. PJ+ P = m1Lv/600. (1) Phase 2 : puissance reÁues par le diazote : P ; cette puissance reÁue permet l'ťvaporation du diazote pendant 300 s : m2Lv/300. P = m2Lv/300. (2) En dťduire une expression littťrale de Lv indťpendante de P, puis calculer sa valeur numťrique si U = 8,5 V et R = 10 ohms. PJ = RI2 = U2/R ; (1) -(2) donne : U2/R = (m1-2m2) Lv/600 ; Lv = 600 U2/ ( R(m1-2m2)). Lv = 600*8,52 /(10*(42-20)) = 197 ~ 200 J g-1.
|
|||||||||
|
|
|||||||||
|
|