|
acide base: critŤre d'ťvolution, taux d'avancement final concours Fesic 2008
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
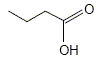
A- Il s’agit de l’acide propanoÔque. Faux. La formule topologique correspond ŗ : CH3-CH2-CH2-COOH, acide butanoÔque L'acide propanoÔque compte seulement 3 atomes de carbone. B- La masse molaire molťculaire de la molťcule reprťsentťe est ťgale ŗ 89 g.mol-1. Faux. M(C4H8O2) = 4*12+8+2*16 = 88 g/mol. C- La rťaction entre cet acide et l’eau est limitťe. Vrai. D- Le taux d’avancement final de la rťaction est d’environ 1,7 %. Vrai. Le tableau suivant est ťtabli pour un volume V = 1 L.
taux d'avancement final :
On dispose de quatre solutions de mÍme concentration molaire en solutť apportť c = 1,0.10–2 mol.L–1. Elles contiennent respectivement de l’acide ťthanoÔque H3C–CO2H(aq), de l’ťthanoate de sodium (Na+ (aq) + H3C–CO2-(aq)), de l’acide mťthanoÔque H–CO2H(aq) et du mťthanoate de sodium (Na+ (aq) + H–CO2-(aq)). On rťalise deux solutions, S1 et S2, en mťlangeant les volumes suivants, exprimťs en mL, des quatre solutions prťcťdentes :
On considŤre la rťaction d’ťquation : H3C–CO2H(aq) + H–CO2-(aq) = H–CO2H(aq) + H3C–CO2-(aq). pKa des couples
acide / base :
H–CO2H(aq)
/ H–CO2-(aq) :
pKa1 =
3,8. H3C–CO2H(aq)
/
H3C–CO2-(aq)
: pKa2 =
4,8. A-
La constante
d’ťquilibre de cette rťaction
s’ťcrit
:
C- Dans la solution S1, la rťaction a lieu dans le sens direct. Faux.
D- Dans la solution S2, la rťaction a lieu dans le sens inverse. Faux.
On rťalise un mťlange ŗ partir d’un volume V1 = 10 mL d’une solution aqueuse de chlorure de magnťsium (Mg2+(aq) + 2 Cl-(aq)) de concentration molaire en solutť apportť c1 = 0,10 mol.L-1 et d’un volume V2 = 10 mL de solution aqueuse de carbonate de sodium (2 Na+(aq) + CO32-(aq)) de concentration molaire en solutť apportť c2 = 0,10 mol.L-1. On donne l’ťquation de la rťaction modťlisant la prťcipitation du carbonate de magnťsium dans l’eau. Mg2+(aq) + CO32-(aq) = MgCO3(s). La constante de cette rťaction est K =1,0 105. On donne 10Ĺ = 3,2. A- L’expression du quotient de la rťaction est Qr = [Mg2+(aq)] [CO32-(aq)]. Faux.
B- Le quotient initial de la rťaction de dissolution Qr,i a une valeur ťgale ŗ 2,5.10-3. Faux. [Mg2+(aq)]i = c1V1 /(V1+V2)= Ĺ c1 = 0,050 mol/L ; [CO32-(aq)]i = Ĺ c2 = 0,050 mol/L.
C- On observe une prťcipitation du carbonate de magnťsium. Vrai. Qr i <K, ťvolution spontanťe en sens direct. D- La concentration molaire en ions carbonate ŗ l’ťquilibre [CO32-(aq)]ťq est ťgale ŗ 0,050 mol.L-1. Faux. [CO32-(aq)]ťq = [Mg2+(aq)]ťq = K-Ĺ =(105)-Ĺ = 10-2 * 10-Ĺ =10-2 /3,2 ~ 3 10-3 mol/L.
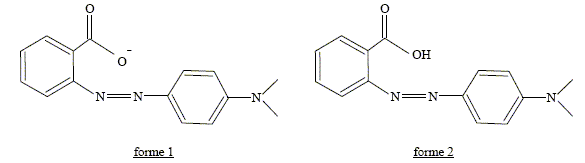
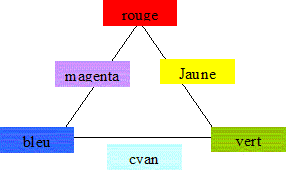
C15H14O2N3 : M = 15*12+14+2*16+3*14 =268 g/mol. B- Lorsque la forme 2 est prťpondťrante, la solution a une teinte jaune. Faux. La forme 2 est la forme acide ( R-COOH) du couple acide / base R-COOH / R-COO- : celle-ci prťdomine ŗ pH infťrieur ŗ pKa ( pH <5,2). La solution a une teinte rouge en milieu trŤs acide. C- L’absorbance de la forme 1 est nulle dans le jaune. Faux. La forme 1 est la forme basique : sa teinte est jaune. Elle absorbe la couleur complťmentaire du jaune, c'est ŗ dire le bleu.
L'absorbance est nulle dans le jaune ; l'absorbance est maximale dans le bleu. D-
A pH= 4,2 :
Produit ionique de l'eau :[H3O+][HO-]=10-pKe. L'eau pure est ťlectriquement neutre : [H3O+]= [HO-]=10-ĹpKe = 10-7,3. B- A 60įC une solution de pH ťgal ŗ 6,8 est basique. Vrai. Le pH du milieu neutre est 13/2 = 6,5. Une solution dont le pH est supťrieur ŗ 6,5 est basique ŗ 60įC. On dispose de trois solutions aqueuses S1, S2, S3, de mÍme concentration molaire en solutť apportť, respectivement d’acide benzoÔque C6H5COOH(aq), d’acide nitreux HNO2(aq), et de chlorure d’ammonium NH4+(aq) + Cl-(aq). Donnťes : A 25 įC : C6H5COOH(aq) /C6H5COO-(aq) : pKa1 = 4,2. HNO2(aq) /NO2-(aq) : pKa2 = 3,3. NH4+(aq) /NH3 : pKa3 = 9,2. C- L’avancement final de la rťaction de l’acide nitreux avec l’eau est plus grand que celui de la rťaction de l’acide benzoÔque avec l’eau. Vrai. A concentration ťgale, l'acide le plus fort possŤde le plus petit pKa. Plus l'acide est fort, plus l'avancement final est proche de l'avancement maximal. On considŤre une solution aqueuse de chlorure d’ammonium, de concentration molaire en solutť apportť c = 5,0 .10-3 mol/L. D- Le taux d'avancement final de la reaction t de cet acide avec l'eau est ťgal ŗ 0,20. Faux. pH =Ĺ( pKa - log c) = 0,5 (9,2 - log 5,0 .10-3 ) = 5,75. Pour 1 L de solution : avancement final xfin = 10-pH = 10-5,75 = 1,8 10-6 mol ; xmax =5,0 .10-3 mol taux d'avancement final :
Donnťes : 0,020 = 10 –1,7 ; volume molaire dans les conditions de l’expťrience Vm = 24 L.mol-1. A- La concentration molaire de la solution aqueuse S est ťgale ŗ 20 mmol/L. Vrai. Quantitť de matiŤre HCl(g) : n =V / Vm = 0,24 / 24 = 0,010 mol= 10 mmol. Concentration (mmol/L) = n(mmol) / volume de la solution (L) =10/0,5 = 20 mmol/L. On mesure le pH de la solution S, on trouve 1,7. B- Le chlorure d’hydrogŤne n’est pas totalement dissociť dans l’eau. Faux. Le chlorure d'hydrogŤne rťagi totalement avec l'eau et donne une solution d'acide chlorhydrique, acide fort. On obtient une solution S’ en mťlangeant 20 mL d’une solution d’acide chlorhydrique de concentration molaire en solutť apportť 1,0.10-1 mol.L-1 et 20 mL d’une solution aqueuse d’hydroxyde de sodium de concentration molaire en solutť apportť 5,0.10-2 mol.L-1. C- Le pH du mťlange est ťgal ŗ 3. Faux. couple acide / base : H3O+ / H2O et H2O / HO-.
Si l'hydroxyde de sodium est en excŤs : 1,0 10-3 -xmax =0 ; xmax =1,0 10-3 mol. Volume total : 20+20 = 40 ml = 0,04 L ; [H3O+]= 10-3 / 0,04 = 0,025 mol/L ; pH = -log 0,025 = 1,6. D- On dilue 5 fois la solution S’, le pH augmente alors d’une unitť. Faux. [H3O+]=0,025 / 5 = 0,005 mol/L ; pH = -log 0,005 =2,3.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|