|
Généralités sur les hydrogénations concours chimie Capes 2009.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées ŕ vos centres d’intéręts. |
|||||||||
| .
. |
|||||||||
|
|||||||||
|
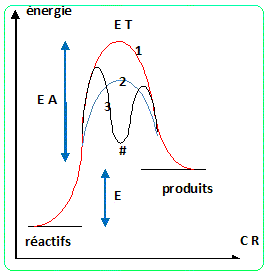
Un catalyseur augmente la vitesse d'une réaction sans intervenir dans le bilan global. Donner le diagramme d'énergie potentielle d'une réaction A-->B ( supposée élémentaire et endothermique) non catalysée, et la męme réaction catalysée. Y faire apparaître le ( ou les )état(s) de transition, le (ou les) intermédiaire(s) réactionnel(s) ainsi que les différentes grandeurs énergétiques. On met en abscisse CR, que signifie CR ?
Définir la catalyse hétérogčne et rappeler les principales étapes d'un mécanisme en catalyse hétérogčne. Le catalyseur est ŕ l'état solide, la phase réactive est liquide ou gazeuse. - Adsorption des réactifs ŕ la surface du catalyseur - quand toutes les nouvelles liaisons sont réalisées, le produit peu adhérent au catalyseur se détache de celui-ci par simple agitation thermique - le catalyseur est d'autant plus efficace que sa surface par unité de masse est grande. Les métaux de transition sont les
éléments qui possčdent une
sous-couche d partiellement remplie. Définition moins stricte : le terme
transition se réfčre aux
éléments situés entre le
groupe 2 et le groupe 13 du tableau
périodique. Définir la notion de complexe. Expliquer pourquoi l'utilisation de ce catalyseur implique une catalyse homogčne. Un complexe est un édifice polyatomique constitué d'un cation ou d'un atome central, entouré de plusieurs ligands ( molécules ou ions ) ; ces derniers délocalisent une partie de leur densité électronique sur le cation ou l'atome central, formant ainsi des liaisons chimiques avec celui-ci. Une catalyse est dite homogčne lorsque le catalyseur ne forme qu'une seule phase avec les réactifs : c'est le cas du catalyseur de Wilkinson, soluble dans les solvants organiques. Les alcčnes. Comment l'éthčne et le propčne sont-ils obtenus dans l'industrie ? éthylčne : ŕ partir du naphta provenant de la distillation fractionnée du pétrole (Europe) par vapocraquage ; ŕ partir de gaz naturel riche en éthane (USA) par pyrolyse ou craquage ŕ température élevée. Propčne : craquage catalytique dans les raffineries, déshydrogénation du propane. La polymérisation par voie radicalaire de l'éthčne fornit environ la moitié du tonnage mondial de popyéthylčne. Le polymčre obtenu par cette méthode n'est pas entierement linéaire mais légčrement ramifié, il est appelé "polyéthylčne basse densité" ou PEBD. Quels sont les noms des différentes étapes de ce mode de polymérisation ? Comment s'explique l'apparition des ramifications ? Amorçage : RO-OR --> 2 RO. ; RO. +CH2=CH2 --> RO-CH2-CH2.. Propagation : RO-CH2-CH2. + CH2=CH2 --> RO-CH2-CH2-CH2-CH2.. RO-CH2-CH2. + nCH2=CH2 --> RO-[CH2-CH2]n-CH2-CH2. . Terminaison : RO. + RO. =RO-OR par exemple. Des ramiffications se créent ŕ la suite de l'arrachement d'un hydrogčne tout au long de la chaîne de croissance par un centre radicalaire, suivi de l'apparition d'une nouvelle chaîne au niveau de ce nouveau radical.
L'autre moitié de la production mondiale de polyéthylčne est obtenue par polymérisation par coordination. Celle-ci s'effectue ŕ température ambiante et pression atmosphérique sur catalyseur ŕ base d'aluminium et de titane. ( Ziegler et Natta, prix Nobel 1963) Le polymére obtenu est parfaitement linéaire, il est nommé " polyéthylčne haute densité " PEHD. Justifier l'influence de la structure sur la densité. Dans le cas d'un polymčre linéaire, les chaînes peuvent se coller les unes aux autres par interaction de Van Der Waals : ce polymčre est dense. Cela n'est pas possible en présence de ramifications, les chaînes étant plus éloignées : le polymčre est moins dense. Le propčne est aussi polymérisé par catalyse de coordination et le polypropylčne obtenu est isotactique. Que signifie le terme isotactique ? Les substituants sont tous du męme côté de la chaîne du polymčre.
|
|||||||||
|
|
|||||||||
|
|