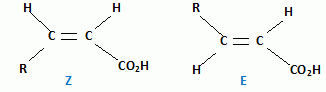|
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
||||||||
| .
. |
||||||||
|
||||||||
|
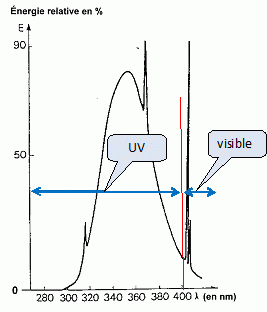
Installation d'un solarium. Le circuit ťlectrique prťvu pour brancher le solarium est protťgť par un disjoncteur thermique portant l'indication 16 A. Il est alimentť sous une tension ťlectrique de 230 V. La puissance ťlectrique du solarium est P =3240 W. Justifier, en calculant l'intensitť , que l'appareil choisi est adaptť ŗ l'installation. On admet que le solarium se comporte comme une rťsistance pure en rťgime permanent. Intensitť ( A) = puissance (W) / tension (V) I = 3240/230 =14,0 A. Cette intensitť ťtant infťrieure ŗ la valeur maximale admissible ( 16 A), le solarium est adaptť ŗ l'installation ťlectrique. Sur la mÍme prise du secteur, en dťrivation sur le solarium, on voudrait alimentť un appareil de chauffage- climatisation rťversible, mobile, d'une puissance de 1000 W. En dťduire que le disjoncteur dťclencherait lors de la mise sous tension. Puissance totale des appareils branchťs ŗ la sortie du disjonteur thermique : 3240 + 1000 = 4240 W Nouvelle intensitť en ligne : 4240/230 = 18,4~ 18 A. Cette valeur est supťrieure ŗ l'intensitť maximale admissible : le disjonsteur thermique se dťclenche ŗ la mise sous tension. On s'intťresse ŗ l'un des tubes d'ťmission UV du solarium dont on donne le spectre d'ťmission. Repťrer, sur un axe graduť en longueur d'onde, les diffťrents domaines de lumiŤres ťmises par le tube.
Irradiance totale : 27,0 + 0,38 = 27,38 W m-2 ; Le rayonnement laser se rťvŤle dangereux pour les yeux : son intensitť est comparable ŗ plusieurs fois celle d'un rayon solaire. l'intensitť de la lumiŤre ťmise par les tubes du solarium n'ont rien ŗ voir avec l'intensitť de la lumiŤre laser. eci le rend trŤs dangereux pour les yeux Etude de quelques actions chimiques du rayonnement UV sur la peau. La couche cornťe contient de l'acide urocanique, vťhiculť par la sueur, qui absorbe les UVB. On donne la formule de cet acide : 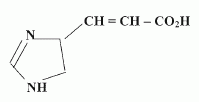 On pourra l'ťcrire plus simplement R-CH=CH-CO2H. Le rayonnement UV peut dťclencher une isomťrisation Z / E.
Ecrire
les formes Z et E de l'acide urocanique. La formation
de la mťlanine se fait par une succession de rťactions chimiques
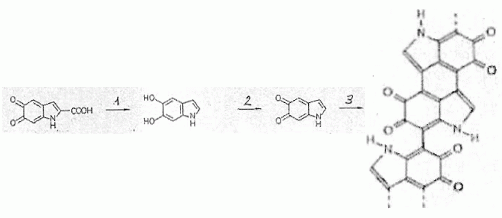
dťbutant avec la phťnylalanine. Parmi l'ensemble de ces rťactions
chimiques, on donne le schťma suivant : On passe d'un monomŤre ŗ un polymŤre : rťaction
de polymťrisation ( addition ou condensation de monomŤres) Ecrire
la demi ťquation ťlectronique correspond ŗ l'ťtape 2 et prťciser
sa nature.
Ecrire la demi-ťquation ťlectronique de cette rťduction. MnO4- aq + 8 H+aq + 5e- = Mn2+ aq + 4H2O(l). Ecrire l'ťquation associťe ŗ la rťaction corresdpondant ŗ l'ťtape 2 lors de l'action des ions permanganate. 2 MnO4- aq + 16 H+aq + 10e- = 2Mn2+ aq + 8H2O(l). 5 fois { 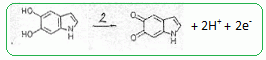 } }Puis additionner et simplifier. 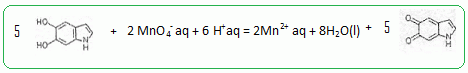
Dosage acide base. On rťalise un dosage acido-basique, suivi par pHmťtrie, d'une solution aqueuse d'acide urocanique, notť R-COOH. On prťpare une solution d'acide urocanique en dissolvant une masse m g de l'acide dans 1,000 L d'eau ŗ la tempťrature ambiante. On dose ensuite V = 200 mL de cette solution avec une solution d'hydroxyde de sodium de concentration molaire C = 0,010 mol/L. Le graphe suivant donne la variation du pH au cours du dosage. Ecrire l'ťquation associťe ŗ la rťaction support du dosage. R-COOH aq + HO-aq = R-COO-aq + H2O(l) Dťfinir l'ťquivalence et dťterminer graphiquement le point d'ťquivalence. A l'ťquivalence les quantitťs de matiŤre des rťactifs mis en prťsence sont en proportions stoechiomťtriques ; avant l'ťquivalence, l'un des rťactifs est en excŤs, aprŤs l'ťquivalence, l'autre rťactif est en excŤs. 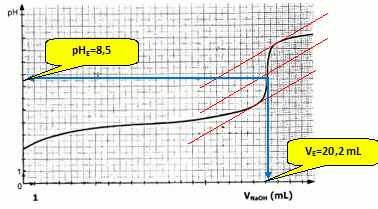
|
||||||||
| |
||||||||
|
|