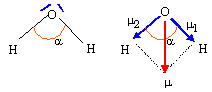|
L'eau : moment dipolaire, conductivitť, piles concours Mines 07 En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts. |
|||||||
| .
. |
|||||||
|
|||||||
|
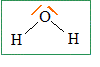
Donner la configuration ťlectronique, dans l'ťtat fondamental, des atomes de la molťcule d'eau. En dťduire la reprťsentation de Lewis de la molťcule d'eau. H : 1s1 ; O : 1s2 2s2 2p4.
Dťduire, ŗ partir de la theorie V.S.E.P.R., la gťomťtrie de l'arrangement des doublets ťlectroniques dans la molťcule d'eau et la gťometrie de cette derniere. 2 doublets liants et deux doublets non liants autour de l'atome central, l'oxygŤne. Type AX2E2, en forme de V. Justifier la valeur numťrique de l'angle a entre les liaisons O-H. Ces 4 paires se disposent autour de l'atome central, de telle maniŤre que les rťpulsions soient minimales. La molťcule d'eau ŗ la forme d'un V : l'angle est infťrieur ŗ 109 į 28 , la rťpulsion entre les doublets non liants ťtant plus importante que la rťpulsion entre les doublets liants. Le module du moment dipolaire permanent de la molťcule d'eau vaut 1,85 D. Dťterminer le moment dipolaire (sens et norme) des liaisons O-H en debye et en C.m. Pourcentage du caractŤre ionique de la liaison OH : dO-H = 96 pm
m1 = m2 ; m = 2 m1 cos (Ĺa) ; m1 =m / ( 2cos (Ĺa)) = 1,85 / (2*cos (104,5 / 2 )) = 1,52 D. or 1 Debye = 1D = 3,33 10-30 C m d'oý m1 =1,52* 3,33 10-30 = 5,06 10-30 C m Pourcentage de caractŤre ionique :
m1 /( e
dOH) = 5,06 10-30 / (1,6
10-19 * 96 10-12) = 0,329 (
33 %).
La liaison O-H a un
caractŤre polaire trŤs
marquť. L’eau pure est le siŤge d’une rťaction d’autoprotolyse. …crire l’ťquation de cette rťaction. Calculer ŗ 25įC la conductivitť thťorique de l’eau pure. 2H2O = HO-(aq) + H3O+(aq). Conductivitť molaire ionique lHO- =2,0 10-2 S m2 mol-1 ; lH3O+ =3,5 10-2 S m2 mol-1. conductivitť s(S m-1) =lHO- [HO-] +lH3O+[H3O+] avec [HO-] =[H3O+] = 10-7 mol/L = 10-4 mol m-3. s=3,5+2,0) 10-2*10-4 = 5,5 10-6 S m-1.
PH2 = 1 bar ; concentration en hydroxyde de potassium = concentration en chlorure de potasium c = 10-3 mol/L. Le chlorure d’argent est trŤs peu soluble dans la solution avec laquelle il est en contact.
A l'anode nťgative en platine, oxydation de H2 : H2 =2H+ 2e-. A la cathode positive en argent, rťduction de AgCl(s) : AgCl(s) +e- = Ag(s) + Cl-. Donner l’expression du potentiel de chaque ťlectrode en fonction de C et de constantes thermodynamiques connues. E- = Eį(H+ /H2 ) + 0,03 log (C2/PH2) = Eį(H+ /H2 ) + 0,03 log C2= Eį(H+ /H2 ) + 0,06 log C. E+ = Eį(AgCl(s)/ Cl- ) + 0,06 log (1/C). Indiquer le pŰle positif de la pile 1 et donner l’expression de la force ťlectromotrice (f.e.m.) E1 de la pile 1 en fonction de C et de constantes thermodynamiques connues. L'argent constitue la borne positive. E1 = E+ -E-=Eį(AgCl(s)/ Cl- ) + 0,06 log (1/C) - Eį(H+ /H2 ) - 0,06 log C. E1 =Eį(AgCl(s)/ Cl- )- Eį(H+ /H2 )+0,03 log (1/C2)- 0,03 log C. E1 =Eį(AgCl(s)/ Cl- )- Eį(H+ /H2 )-0,12 log C.
A l'anode nťgative en platine, oxydation de H2 en milieu basique : H2+ 2HO- =2e- + 2H2O. A la cathode positive en argent, rťduction de AgCl(s): AgCl(s) +e- = Cl- = Ag(s). Donner l’expression du potentiel de chaque ťlectrode en fonction de C, de constantes thermodynamiques connues et de pKe. E- = Eį(H+ /H2 ) + 0,03 log (1/([HO-]2PH2))= Eį(H+ /H2 ) + 0,03 log (Ke/C)2=Eį(H+ /H2 ) + 0,06 log (Ke/C). E+ = Eį(AgCl(s)/ Cl- ) + 0,06 log (1/C). Indiquer le pŰle positif de la pile 2 et donner l’expression de la force ťlectromotrice (f.e.m.) E2 de la pile 2 en fonction de C, de constantes thermodynamiques connues et de pKe. L'argent constitue la borne positive. E2 = E+ -(-E-)=Eį(AgCl(s)/ Cl- ) + 0,06 log (1/C) - Eį(H+ /H2 ) - 0,06 log (Ke/C). E2 =Eį(AgCl(s)/ Cl- )- Eį(H+ /H2 )-0,06 log Ke = Eį(AgCl(s)/ Cl- )- Eį(H+ /H2 )+0,06pKe. E2=Eį(AgCl(s)/ Cl- )- Eį(H+ /H2 )+0,06pKe. Les piles sont reliťes par leurs ťlectrodes d’argent. La mesure de la force ťlectromotrice de la pile double donne E = 0,472 V ŗ 25įC ; en dťduire la valeur du pKe de l’eau ŗ cette tempťrature et comparer ŗ la valeur connue ŗ 25įC. E = E2-E1=0,06pKe+0,12 log C. 0,06pKe=E-0,12 log C ; pKe=(E-0,12 log C )/0,06 = (0,472-0,12*(-3))/0,06 =13,87. En prenant 0,059, valeur plus prťcise, ŗ la place de 0,06 on trouve : pKe=14. La valeur expťrimentale est ťgale ŗ la valeur thťorique.
|
|||||||
|
|
|||||||
|
|