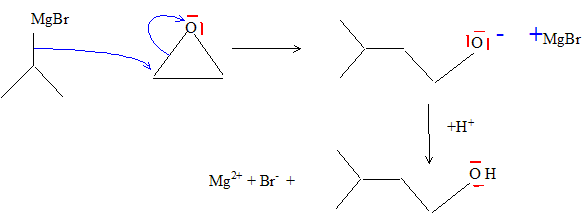|
SynthŤse d'un organomagnťsien, addition sur un alcŤne, dťshydratation d'un alcool concours Mines 03 En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts. |
|||||||
| .
. |
|||||||
|
|||||||
|
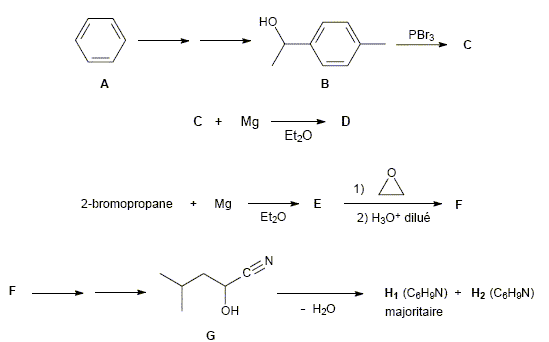
La dťcouverte des organomagnťsiens a valu ŗ leur inventeur le Prix Nobel de chimie en 1912. Quel est le nom de ce chimiste franÁais ? V. Grignard. A partir de quels rťactifs s’effectue la synthŤse d’un organomagnťsien ? Mg + RX dťrivť halogťnť. Proposer, en le justifiant, un solvant pour cette synthŤse (un seul critŤre est exigť). Solvant anhydre ťther ťthylique ou THF : l'eau dťtruit le magnťsien. Le solvant est une base de Lewis : il doit Ítre aprotique. La synthŤse d’un organomagnťsien s’effectue dans un tricol surmontť d’un rťfrigťrant. Quel est le rŰle de ce rťfrigťrant ? La rťaction ťtant exothermique et le solvant volatil, il faut condenser les vapeurs du solvant. La synthŤse suivante illustre le grand intťrÍt des organomagnťsiens en synthŤse organique. Il s’agit de la synthŤse au laboratoire d’un sesquiterpŤne (molťcule odorante en C15) : le calacorŤne, qui est prťsent dans le clou de girofle notamment.
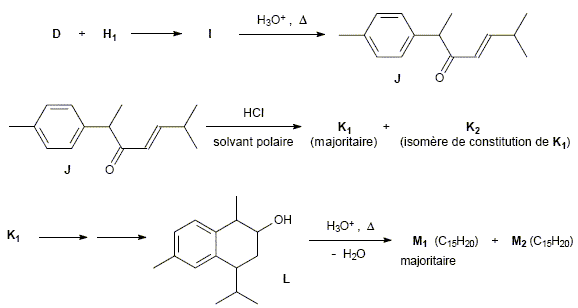
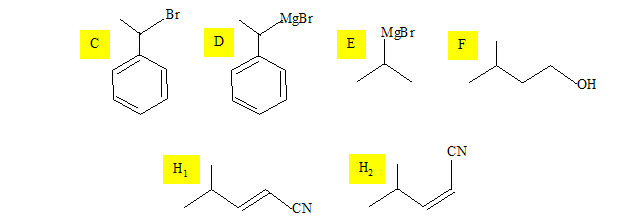
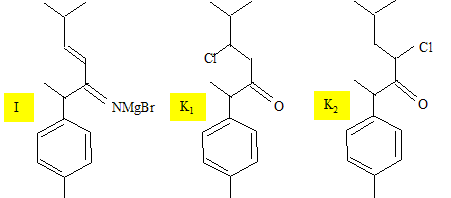
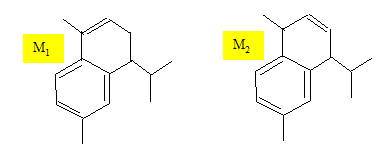
M1 est le calacorŤne. Ecrire la formule topologique des composťs C, D, E, F, H1, H2, I, K1, K2, M1 et M2.
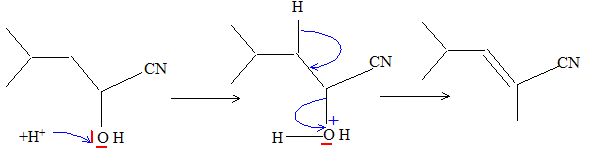
Dťcrire le mťcanisme de la rťaction E --> F. Quelle rťaction parasite pourrait se dťrouler si l’hydrolyse ťtait menťe en milieu acide trop concentrť ? Quelle prťcaution expťrimentale supplťmentaire permettrait d’ťviter celle-ci ? Un alcool est protonť en prťsence d'un acide fort ; H2O est un on nuclťofuge : l'alcool est dťshydratť. Cette rťaction d'ťlimination est ťvitťe en milieu acide peu concentrť et ŗ basse tempťrature. Prťciser les conditions opťratoires requises pour dťshydrater G. En milieu acide fort : acide sulfurique et ŗ chaud. Dťcrire le mťcanisme de la rťaction G -->H1. Justifier que H1 est majoritaire devant H2. L'ťlimination d'eau conduit ŗ l'alcŤne le plus stable ( isomŤre E) : rŤgle de Zaytseff.
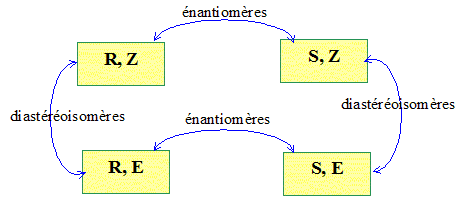
Combien J possŤde-t-il de stťrťoisomŤres ? Les dťsigner ŗ l'aide de la nomenclature adaptťe (R, S, Z, E) en indiquant la relation de stťrťoisomťrie qui existe entre eux. (on ne demande pas de reprťsenter les stťrťoisomŤres, ni de les nommer).
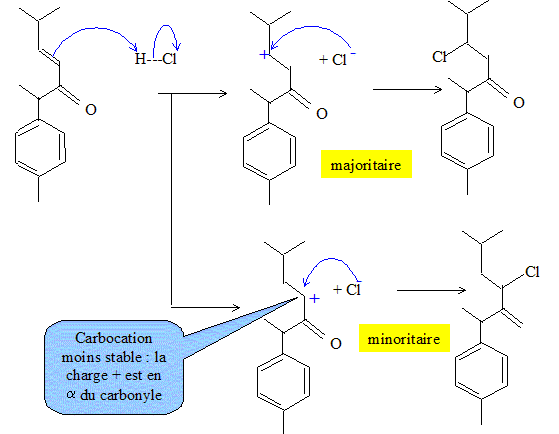
Dťcrire le mťcanisme de la rťaction J -->K1. Justifier que K1 est majoritaire devant K2. Addition de HCl sur la double liaison CC.
Justifier que M1 est majoritaire devant M2. L'ťlimination d'eau conduit ŗ
l'alcŤne le plus stable (le plus substituť) :
rŤgle de Zaytseff.
|
|||||||
|
|
|||||||
|
|