|
Propriťtť rťductrice du magnťsium ; duretť de l'eau : dosage par l'EDTA concours Mines 03 En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Le magnťsium est un ťlťment relativement abondant dans l’ťcorce terrestre. L’eau de mer qui contient 0,135 % de magnťsium sous forme de Mg2+ peut Ítre considťrťe comme une rťserve quasiment inťpuisable de ce mťtal. Propriťtťs atomiques. Le numťro atomique du magnťsium est Z=12. Indiquer sa configuration ťlectronique dans l’ťtat fondamental et en dťduire sa position (numťros de ligne et de colonne) dans la classification pťriodique. 1s2 2s2 2p6 3s2 : seconde colonne, 3Ťme ligne. Le tableau ci-dessous regroupe quelques propriťtťs atomiques du magnťsium et d’ťlťments issus de la mÍme colonne de la classification pťriodique. Il s’agit du numťro atomique (Z), du rayon atomique(ratomique), du rayon ionique du cation M2(rionique), des ťnergies de premiŤre et de deuxiŤme ionisation de l’atome (Eionisation1 et Eionisation2), du potentiel redox standard du couple M2+/M (Eį(M2+/M)).
Lorsque le rayon atomique augmente, les ťlectrons de valence, plus ťloignťs, sont de moins en moins liťs au noyau : en consťquence l'ťnergie de 1Ťre ionisation diminue. Justifier que, pour chaque atome, Eionisation2 > Eionisation1. Les rayons ioniques sont tous infťrieurs aux rayons atomiques correspondants : l'ťlectron de valence dans l'ion M+ est plus liť au noyau que dans l'atome. L'ťnergie de 2Ťme ionisation sera donc plus ťlevťe que l'ťnergie de premiŤre ionisation. Des cinq ťlťments prťsentťs dans ce tableau, lequel est le meilleur rťducteur ? En dťduire lequel est le moins ťlectronťgatif. Plus Eį(M2+/M) est nťgatif, plus le caractŤre rťducteur et plus le caractŤre mťtallique augmentent : Ba est le meilleur rťducteur. Propriťtťs
rťductrices du
magnťsium. Le magnťsium sert ŗ la fabrication
de piles amorÁables ŗ l’eau de
mer, trŤs utilisťes dans la marine.
Ce type de pile est constituť d’une
demi-pile AgCl (s) / Ag (s) et d’une demi-pile
MgCl2 (s) / Mg (s). La pile est
ťtanche mais peut Ítre activťe
par ouverture d’un opercule permettant le
contact entre l’eau de mer et les
ťlectrodes. En milieu chlorure, le potentiel standard du
couple MgCl2 (s) / Mg (s) vaut
–1,71 V ; celui du couple AgCl (s) / Ag (s) vaut 0,22
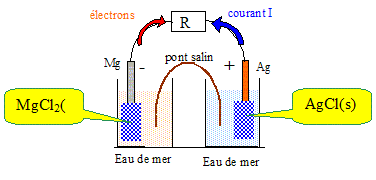
V. A l'anode nťgative, le mťtal le plus rťducteur s'oxyde : le mťtal le plus rťducteur appartient au couple redox ayant le plus petit potentiel. Le magnťsium s'oxyde ŗ l'anode nťgative : Mg + 2Cl-= MgCl2 + 2e-. A la cathode positive, l'oxydant de l'autre couple redox se rťduit : 2AgCl (s) +2e- = 2Ag(s) + 2Cl-. Quelle est la rťaction de fonctionnement de la pile ? Mg (s) +2AgCl (s) = MgCl2 (s) + 2Ag(s). Faire un schťma de la pile en fonctionnement en prťcisant la polaritť des ťlectrodes et le sens de dťplacement des ťlectrons.
Mg + 2Cl-= MgCl2 + 2e-. E1 = Eį( MgCl2 (s) / Mg (s)) +0,03 log (1/[Cl-]2) 2AgCl (s) +2e- = 2Ag(s) + 2Cl-. E2 =Eį (AgCl (s) / Ag (s)) +0,03 log (1/[Cl-]2) E = E2 -E1 = Eį (AgCl (s) / Ag (s)) -Eį( MgCl2 (s) / Mg (s)) E = 0,22-(-1,71) = 1,93 V. Quel est le rŰle de l’eau de mer ? L'eau de mer assure la continuitť ťlectrique : la migration des ions est ainsi assurťe entre les ťlectrodes.
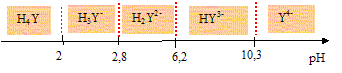
La duretť de l’eau est un concept qui a ťtť introduit afin d’en connaÓtre la teneur en ions Ca2+ et Mg2+. Les eaux dites dures sont des eaux riches en ions calcium et magnťsium. Elles ont le dťfaut de faire prťcipiter les savons qui perdent alors leur pouvoir moussant. De plus, elles favorisent la formation de tartre (CaCO3 et MgCO3) dans les canalisations. On se propose dans cette partie de dťterminer la duretť totale, c’est-ŗ-dire la somme [Ca2+]+ [Mg2+], d’une eau minťrale en la dosant ŗ l’aide d’acide ťthylŤnediaminetťtraacťtique (EDTA) notť H4Y. L’EDTA (notť H4Y) est un tťtraacide dont les pKa successifs valent respectivement : 2,0 ; 2,7 ; 6,4 ; 10,2. Le mode opťratoire est le suivant : ę On place 10 mL d’eau ŗ analyser dans un erlenmeyer de 150 mL. On y ajoute 10 mL d’une solution tampon de pH = 10 et 12 gouttes d’une solution de l’indicateur colorť Calmagite fraÓchement prťparť. La solution, incolore avant l’ajout du Calmagite, prend alors une coloration rose ę lie de vin Ľ. On place dans la burette une solution de sel disodique d’acide ťthylŤnediaminetťtraacťtique dihydratť (Na2H2Y, 2 H2O) de concentration c = 0,050 mol.L–1. On appelle v le volume de titrant versť. On observe le virage de la solution du rose au bleu pour un volume versť v = ve.Ľ. Prťparation des solutions. Pour prťparer la solution de titrant, on introduit une masse m de sel disodique d’acide ťthylŤnediaminetťtraacťtique dihydratť (Na2H2Y, 2 H2O) dans une fiole jaugťe de 250 mL. On complŤte au trait de jauge avec de l’eau distillťe. On bouche la fiole et on agite pour homogťnťiser la solution. Dťterminer la masse m que l’on doit peser avec prťcision pour obtenir une solution de concentration c = 0,050 mol.L–1. Na : 23 ; H4Y : 292 ; H : 1,0 ; O : 16,0 g/mol. Masse molaire (Na2H2Y, 2 H2O) : M = 23*2+290+36=372 g/mol. Quantitť de matiŤre dans 0,25 L : n=0,25 c = 0,25*0,05 = 0,0125 mol Masse m = n M = 0,0125*372 = 4,65 g. Indiquer les domaines de prťdominance des diffťrentes formes de l’EDTA en fonction du pH. Quelle est l’espŤce prťdominante ŗ pH = 10 ?
A pH =10, la forme HY3- est majoritaire. Dans la suite du problŤme on considťrera, par souci de simplification, que tout l’EDTA est sous cette forme ŗ pH = 10. Pour prťparer la solution de solution tampon pH = 10, on dissout une masse m’ de NH4Cl dans 100 mL de soude molaire et on complŤte le volume jusqu'ŗ 250 mL avec de l'eau distillťe. Ecrire l’ťquation-bilan de la rťaction qui se produit quand on mťlange ces deux rťactifs. NH4+/NH3 : pKa1 = 9,2 ; H2O/HO- : pKe=14. NH4++ HO- = NH3 + H2O. Calculer sa constante d’ťquilibre. Que peut-on en dťduire ? K = [NH3] /( [NH4+][HO-]) avec Ka1 = [NH3][H3O+] /[NH4+] soit : [NH3] /[NH4+] = Ka1 /[H3O+] Repport dans K : K = Ka1 /( [H3O+][HO-]) =Ka1 /Ke =10-9,2/10-14 =104,8 = 6,3 104. K ťtant grande, la rťaction est totale. Faire le bilan de matiŤre. En dťduire la valeur de la masse m’ que l’on doit peser pour obtenir une solution tampon de pH = 10. Le couple NH4+/NH3 fixe le pH : pH= pKa1 + log([NH3]/[NH4+]). 10-9,2 = 0,8 = log([NH3]/[NH4+]) ; [NH3]/[NH4+] = 100,8 = 6,3 ou n(NH3) =6,3 n(NH4+) (1) Conservation de l'ťlťment azote : n(NH3) + n(NH4+) = m'/M=m'/53,5 et en tenant compte de (1) :7,3 n(NH4+) =m'/53,5 m'=53,5*7,3 n(NH4+) =3,90 102n(NH4+) (2)
0,1-x = 2,5 10-5 soit x = 9,9975 10-2 mol n(NH4+)=(NH3)/6,3 = 9,9975 10-2 /6,3 =1,5869 10-2. (2) donne : m'= 390*1,5869 10-2 ; m' = 6,2 g.
Principe du dosage. Dans une solution tamponnťe ŗ pH 10, l'indicateur Calmagite (notť In) est rose ę lie de vin Ľ lorsqu'il est complexť au Mg2+ et il est bleu lorsqu'il n'y a aucun ion magnťsium disponible. Les ions calcium ne sont pas complexťs par le Calmagite. L'EDTA complexe les ions Mg2+ et Ca2+ pour donner des ions MgY2– et CaY2–. Ces complexes EDTA-mťtal sont incolores. Ecrire l’ťquation-bilan des deux rťactions de titrage qui se produisent pour 0<v<ve. Mg2+ +HY3- = MgY2–+HO- ; Ca2+ +HY3- = CaY2– +HO- Ecrire l’ťquation-bilan de la rťaction qui explique le changement de couleur se produisant ŗ l’ťquivalence. Donnťes : Mg2++In = MgIn2+ ; b = 4,9 105. Ca2+ +Y4- = CaY2– ; b' = 5,0 1010 ; Mg2+ +Y4- = MgY2– ; b" = 4,9 108. Le complexe MgIn2+ est moins stable que MgY2– : avant l'ťquivalence , l'EDTA ťtant en dťfaut, Mg2+ en excŤs, la couleur rose est due au complexe MgIn2+. AprŤs l'ťquivalence , l'EDTA ťtant en excŤs, Mg2+ en dťfaut, le complexe MgIn2+ n'existe plus et la solution est bleue. MgIn2+ +HY3-
+HO-= MgY2– +In + H2O
gouttes de solution de Na2MgY ŗ l’ťchantillon d’eau ŗ analyser. Ecrire l’ťquation-bilan de la rťaction prťpondťrante qui se produit quand on ajoute des ions MgY2– ŗ un mťlange d’ions Mg2+ et Ca2+. Formation du complexe le plus stable : MgY2– + Ca2+ = CaY2– + Mg2+.(3) Puis Mg2++In = MgIn2+ ; la coloration rose est plus intense. Calculer sa constante d’ťquilibre. K = [CaY2–][Mg2+] /([MgY2–][Ca2+ ]) or : Ca2+ +Y4- = CaY2– ; b' = 5,0 1010 =[CaY2–]/([Ca2+ ][Y4-]) Or Mg2+ +Y4- = MgY2– ; b" = 4,9 108=[MgY2–]/([Mg2+ ][Y4-]) Il en rťsulte K= b' /b" =500/4,9 = 102. Montrer que l’ajout des quelques gouttes de solution de Na2MgY ne modifie pas la valeur du volume ŗ l’ťquivalence. (3) indique : la quantitť de matiŤre d'ion Ca2+ consommťs est ťgale ŗ la quantitť de matiŤre d'ion Mg2+ formťs. La valeur du volume ťquivalent n'est donc pas modifiťe. Rťsultats. Le volume d’EDTA nťcessaire pour observer le virage de la solution est ve = 3,0 mL. En dťduire la valeur de [Ca2+]0+ [Mg2+]0 dans l’ťchantillon d’eau ŗ analyser. A l'ťquivalence, les quantitťs de matiŤre de rťactifs mis en prťsence sont en proportions stoťchiomťtriques : n0(Ca2++Mg2+) = Ve. c = 3,0 10-3 * 0,050 = 1,5 10-4 mol dans 10 mL d'eau minťrale. [Ca2+]0+ [Mg2+]0 = 1,5 10-4 / 10-2 = 1,5 10-2 mol/L. Sur l’ťtiquette de la bouteille d’eau, le fabricant indique les teneurs en ions suivantes : Ca2+ : 467 mg.L–1 et Mg2+ : 84 mg.L–1. Ces valeurs sont-elles compatibles avec le rťsultat expťrimental ? [Ca2+]0 = 0,467 /40 = 1,167 10-2 mol/L ; [Mg2+]0 =0,084/24,3 =3,46 10-3 mol/L. [Ca2+]0+ [Mg2+]0 =1,167 10-2 +3,46 10-3 = 1,51 10-2 mol/L. Les valeurs portťes sur l'ťtiquette sont donc compatibles avec les rťsultats du dosage. Lors de l’ťtude de ce dosage, on n’a pas tenu compte de la formation ťventuelle d’un prťcipitť de Mg(OH)2. Justifier. Donnťes : pKs(Mg(OH)2) = 10,7. Mg2+ + 2HO- =Mg(OH)2(s) ; [Mg2+][HO- ]2 = 10-10,7 avec [HO- ] = 10-4 mol/L le prťcipitť apparaÓt dŤs que [Mg2+] atteint la valeur : 10-10,7 / 10-8 = 10-2,7 =2,0 10-3 mol/L Or "On place 10 mL d’eau ŗ analyser dans un erlenmeyer de 150 mL. On y ajoute 10 mL d’une solution tampon de pH = 10." En tenant compte de la dilution : [Mg2+]max =0,5*3,46 10-3 = 1,7 10-3 mol/L. Valeur infťrieure ŗ 2
10-3 : Mg(OH)2(s) n'apparaÓt
pas.
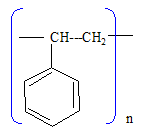
Traitement de l’eau dure. Un des traitements utilisťs pour adoucir l’eau du robinet est un traitement physique par passage sur une rťsine ťchangeuse d’ions. Cette rťsine est prťparťe ŗ partir de polystyrŤne. Celui-ci subit une rťaction de sulfonation par action d’acide sulfurique concentrť. On gorge ensuite d’eau cette rťsine puis on la sature en chlorure de sodium. Au contact d’eau riche en ions calcium ou magnťsium, il se produit un ťchange de deux ions Na+ par un ion Ca2+ ou Mg2+. On rappelle la formule du styrŤne : Ph–CH=CH2 oý Ph– dťsigne un radical phťnyle (C6H5–). Quelle est la formule du polystyrŤne ?
Dťcrire le mťcanisme de l’ťtape d’allongement de chaÓne lors de la polymťrisation radicalaire du styrŤne. Ph–CH--CH2. + Ph–CH=CH2--> Ph–CH--CH2--CH Ph --CH2. Citer une autre utilisation courante du polystyrŤne. PolystyrŤne expansť : isolant thermique
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|