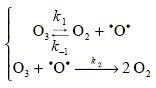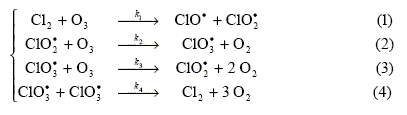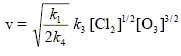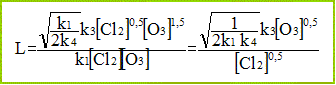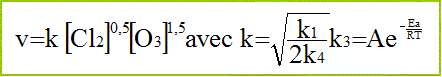|
cinťtique chimique : dťcomposition de l'ozone atmosphťrique concours Mines 03 En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts. |
|||||||
| .
. |
|||||||
|
|||||||
|
Le but de cette partie est d’ťtudier le mťcanisme de la dťcomposition de l’ozone, et l’influence des chlorofluorocarbures (C.F.C.) sur cette dťcomposition (qui mŤne au problŤme actuel du ę trou Ľ dans la couche d’ozone). L’ozone est thermodynamiquement instable par rapport au dioxygŤne. Il peut se dťcomposer, en l’absence de catalyseur, suivant la rťaction trŤs lente : 2 O3(g)--> 3 O2(g) pour laquelle on peut proposer le mťcanisme suivant :
Rappeler la dťfinition d’un intermťdiaire rťactionnel. Illustrez votre dťfinition d’un exemple tirť du mťcanisme prťcťdent. EspŤce formť au cours d'une ťtape et qui est consommťe lors d'une ťtape ultťrieure : un intermťdiaire rťactionnel ne figure pas dans le bilan de la rťaction. Les intermťdiaires rťactionnels restent en quantitť pratiquement constante et trŤs faible. d[Pintermťdiaire] / dt =0 exemple tirť de ce mťcanisme : .O.. Dťterminer la loi de vitesse de la rťaction prťcťdente en fonction de [O3], [O2] et des constantes de vitesse. On appliquera pour cela le principe de Bodenstein, ou des ťtats quasistationnaires. 2 O3(g)--> 3 O2(g) ; v = 1/3 d[O2]/dt. d[O2]/dt = k1[O3]-k-1[O2][.O.] + 2k2 [O3][.O.] (1) d[.O.]/dt = k1[O3]-k-1[O2][.O.]-k2 [O3][.O.]=0 (2) (1)- (2) donne : d[O2]/dt =3k2 [O3][.O.] (3) (2) donne [.O.] = k1[O3] / ( k-1[O2] + k2 [O3] ) Repport dans (3) : d[O2]/dt = 3 k1 k2 [O3]2 / ( k-1[O2] + k2 [O3] ). v = k1 k2 [O3]2 / ( k-1[O2] + k2 [O3] ).
Justifier cette
affirmation. Un inhibiteur est une substance chimique
ralentissant ou empÍchant une rťaction
. Dans l'expression de v,
[O2] figure au
dťnominateur : si la concentration en
dioxygŤne croÓt, alors la vitesse v
diminue. destruction de l’ozone atmosphťrique. En effet, la vitesse de dťcomposition de l’ozone est fortement accrue en prťsence de dichlore. Le mťcanisme proposť est le mťcanisme de rťaction en chaÓne suivant :
Rappeler les diffťrentes ťtapes, ainsi que leur signification, que comporte un mťcanisme de rťaction en chaÓne. Identifiez-les dans le mťcanisme ici proposť. Initiation : ťtape 1, crťation d'intermťdiaires rťactionnels. Propagation : ťtapes 2 et 3, consommation puis rťgťnťration de ces intermťdiaires. Terminaison : ťtape 4, disparition des intermťdiaires rťactionnels.
Justifier alors le rŰle catalytique du dichlore dans la dťcomposition de l’ozone. Dans l'expression de v, [Cl2] figure au numťrateur : si la concentration en dichlore croÓt, alors la vitesse v augmente. Le dichlore se comporte donc comme un catalyseur.
On dťfinit la longueur moyenne de chaÓne, notťe L , par : L = vitesse globale de dťcomposition de O3 / vitesse d'initiation. Dťterminer l’expression de L en fonction de [O3], [Cl2] et des ki (i = 1, 2, 3 ou 4). L'ťtape (1) est l'initiation ; la vitesse de cette rťaction est : k1[Cl2] [O3].
Quelle est l’influence de [Cl2] sur cette longueur de chaÓne ? L est inversement proportionnelle ŗ la racine carrťe de la concentration en dichlore. Si [Cl2] croÓt, alors la longueur de chaÓne diminue.
Montrer que la rťaction globale obťit ŗ la loi d’Arrhťnius. La vitesse peut se mettre sous la forme :
En dťduire l’expression de son ťnergie d’activation en fonction des ťnergies d’activation des diffťrentes ťtapes. k1 = A1 exp (-Ea1/(RT)) ; k3 = A3 exp (-Ea3/(RT)); k4 = A4 exp (-Ea4/(RT)) ; k= A exp(-Ea/(RT)). On identifie : exp(-Ea/(RT)) ŗ exp (-ĹEa1/(RT)) . exp (-Ea3/(RT)) . exp (+ĹEa4/(RT)) soit Ea = ĹEa1+Ea3-ĹEa4.
|
|||||||
|
|
|||||||
|
|