|
Concours manipulateur ťlectroradiologie mťdicale Lyon 2008 acide monochloroacťtique ; chromage : ťlectrolyse ; prťcipitation ; acťtate d'eugťnyle. En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
On prťpare 1,00 L d'une solution aqueuse S d'acide monochloroacťtique ClCH2-COOH. Le pKa du couple acide base associť est ťgal ŗ 2,8 et le pH de la solution obtenue est 1,9. Lors du dosage d'un prťlevement de 20,0 mL de la solution S par de l'hydroxyde de sodium telle que cb=0,50 mol/L, le volume ťquivalent mesurť est Vťq=8,0 mL. La constante de la rťaction de dosage est ťgale ŗ 10-11,2. Faux. ClCH2-COOH + HO- = ClCH2-COO- + H2O. K = [ClCH2-COO-] / ([ClCH2-COOH ][HO-]) Or Ka = [ClCH2-COO-][H3O+] / [ClCH2-COOH ] soit [ClCH2-COO-] /[ClCH2-COOH ] =Ka /[H3O+] Repport dans K : K=Ka /([H3O+][HO-]) = Ka/Ke = 10-2,8/10-14 = 1011,2. A l'ťquivalence du dosage le pH est basique. Exact. A l'ťquivalence on a une solution de monoacťtate de sodium ; la rťaction prťpondťrante est : ClCH2-COO- + H2O = ClCH2-COOH + HO-. K' =1/K= 10-11,2. K' ťtant petit cette rťaction est trŤs limitťe.
[ClCH2-COOH ] =[HO-] = xťq /0,028 Par suite K = 10-11,2 = x2ťq /(0,028 n1) ; x2ťq = 6,3 10-12*0,028* 4 10-3 ; d'oý xťq = 2,65 10-8 mol ; [HO-] = 2,65 10-8 /0,028 =9,5 10-7 mol/L [H3O+] = 10-14 / 9,5 10-7 ~ 10-8 mol/L soit pH ~ 8. La concentration de la solution S est ťgale ŗ 20 mmol/L. Faux. A l'ťquivalence 20 C = 8 cb ; C = 8/20*0,5 ; C= 0,2 mol/L = 200 mmol/L. m = n M = 0,2*94,5 =
18,9 g dissout dans
1 L.
On verse un volume V1 = 10 mL d'une solution aqueuse de chlorure de calcium( Ca2+aq + 2Cl- aq) de concentration c1 = 0,10 mol/L dans un volume V2=10 mL de solution de carbonate de sodium ( 2Na+aq + CO32-aq) de concentration molaire c2=0,10 mol/L. On observe la formation d'un prťcipitť blanc de carbonate de calcium : Ca2+aq + CO32-aq = CaCO3 (s). Constante de cette rťaction K = 108. Le quotient initial de rťaction est supťrieur ŗ la constante d'ťquilibre. Faux. On observe la formation du prťcipitť de carbonate de calcium : l'ťquilibre ťvolue dans le sens direct ; le principe d'ťvolution spontanť conduit ŗ : Qr i <K. Le quotient initial de rťaction a pour valeur Qr i =100. Faux. Qr i = 1/([Ca2+aq]i[CO32-aq]i) [Ca2+aq]i = c1V1 / (V1 +V2) =0,10*10/20 = 0,05 mol/L. [CO32-aq]i= c2V2 / (V1 +V2) =0,10*10/20 = 0,05 mol/L. Qr i =1/ (0,05*0,05) = 1/(25 10-4) = 100*100/25 = 400. A l'ťquilibre, la concentration molaire en ion carbonate est [CO32-aq ]ťq = 10-4 mol/L. Exact. K= 1/([Ca2+aq]ťq[CO32-aq]ťq)
soit [CO32-aq]ťq= 1/KĹ = 1/104 = 10-4 mol/L. AprŤs passage ŗ l'ťtuve du prťcipitť, on obtient une masse de 100 mg. Exact. 50(10-3 -xťq) = 10-4 ; 10-3 -xťq = 10-4 /50 = 2 10-6 mol ; xťq =9,98 10-4 mol. M(CaCO3) = 40+12+3*16=100 g/mol m = xťq M = 9,98 10-4 *100 = 9,98 10-2 g = 99,8 mg.
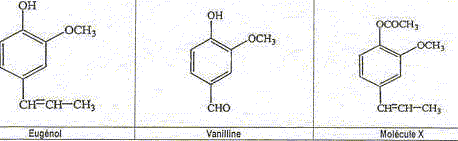
L'eugťnol extrait de l'huile essentielle des clous de girofle, est utilisťe dans certains produits des domaines mťdical et dentaire en raison de ses propriťtťs antalgiques et antiseptiques. On peut ťgalement l'utiliser pour rťaliser l'hťmisynthŤse de la vanilline, molťcule aromatique prťsente dans la vanille.
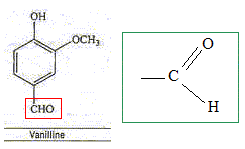
La vanilline est un ester de l'eugťnol. Faux. La molťcule de la vanilline
ne possŤde pas le groupe La vanilline possŤde une fonction aldehyde. Exact.
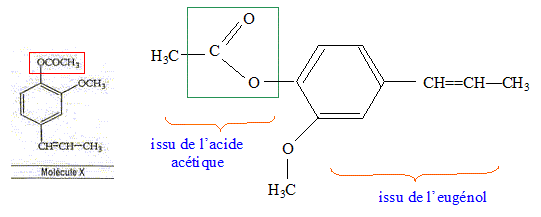
La molťcule X est l'acťtate d'eugťnyle. Exact.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
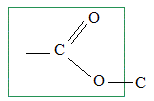 caractťristique
de la fonction ester.
caractťristique
de la fonction ester.