|
Concours adjoint technique principal de laboratoire interne 2008. spectrophotomťtrie : option
C. En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts |
|||||||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||
|
Prťciser la liste du matťriel nťcessaire ŗ la prťparation, ŗ partir de dichromate de potassium K2Cr2O7 pur cristallisť, 100 mL de solution de dichromate de potassium ŗ 100 mg/L en milieu acide sulfurique diluť. Balance ťlectronique de prťcision, spatule et coupelle. Fiole jaugťe de 100 mL, pissette d'eau distillťe, dispositif d'agitation, acide sulfurique diluť. Prťciser les ťquipements de protection individuels nťcessaires pour rťaliser la pesťe du dichromate de potassium. Port de gants, blouse et travail sous hotte aspirante. Prťciser les ťquipements de protection individuels nťcessaires pour prťparer ŗ partir d'acide sulfurique pur commercial, la solution d'acide sulfurique ŗ environ 0,005 mol/L utilisť comme solvant pour la dissolution de dichromate de potassium. Port de blouse, gants et lunettes de protection. ContrŰle de la solution de dichromate de potassium par dosage volumťtrique.
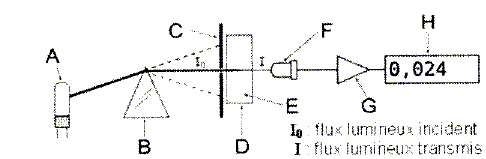
ContrŰle du spectrophotomŤtre. Loi de beer Lambert. A = elc. Donner la signification des grandeurs utilisťes dans cette loi. e est le coefficient d'extinction molaire, caractťristique de la substance (L mol-1 cm-1), l est l'ťpaisseur de la cuve (cm) et c la concentration de la solution (mol/L). A est l'absorbance ou densitť optique. Prťciser les conditions d'application de cette loi. Cette loi est vťrifiťe lorsque la solution est de concentration infťrieure ŗ : c < 0,1 mol.L-1. Schťma d'un spectrophotomŤtre monofaisceau.
Complťter le tableau ci-dessous :
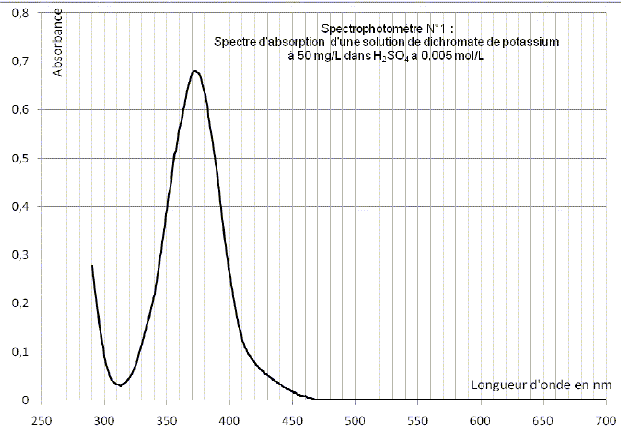
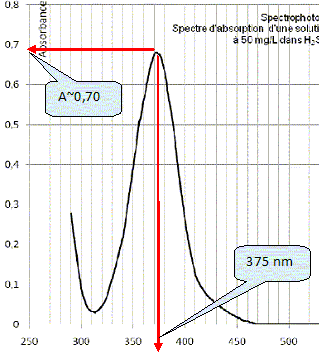
ContrŰle de l'exactitude des absorbances : Ce contrŰle peut Ítre fait par des filtres, des verres neutres ou des substances en solution ( par exemple le dichromate de potassium, nitrate de nickel ) qui prťsentent de larges bandes d'absorption :
Conclure sur l'exactitude de ce spectrophotomŤtre.
Ce spectrophotomŤtre ne donne pas de bons rťsultats.
|
|||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||
|
|