|
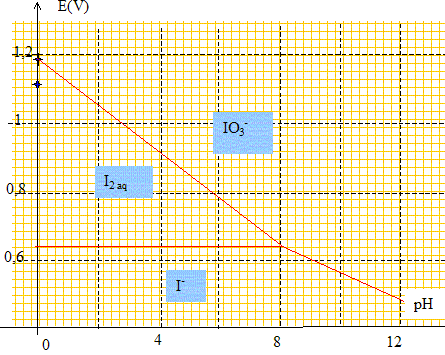
Influence du pH sur la stabilité du diiode en solution aqueuse concours Capes interne 2008 En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées ŕ vos centres
d’intéręts. |
|||||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||
|
n.o(I) +3 n.o(O) = -1 avec n.o(O) - -2 d'oů n.o(I) = +V. Soient les deux couples redox IO3- aq/I2aq et I2aq/I-aq. Ecrire les demi-équations électroniques pour ces deux couples. 2IO3- aq+ 12H+aq + 10e- = I2aq+ 6H2O. I2aq+2e- =2I-aq. Expliciter les potentiels d'électrode correspondants : E1 = E°(IO3- aq/I2aq ) + 0,06/10 log([IO3- ]2[H+]12/ [ I2]) E2 = E°( I2aq/I-aq ) + 0,03 log([ I2]/ [I-]2)
Le potentiel de Nernst dépend de la température. Justifier. Le potentiel de Nernst découle des potentiels chimiques : ces derniers dépendent de la température. On prendra les
concentrations des espčces
considérées égales ŕ
0,100 mol/L sur cette frontičre. E°(IO3-
aq/I2aq ) = 1,19 V ; E°(
I2aq/I-aq ) = 0,62
V. E1 = 1,19 - 6 10-3 +0,072 log [H+] ; E1 = 1,18 - 0,072 pH. ŕ pH 0 : E1 = 1,18 V ; ŕ pH=10 : E1 = 0,464 V ; E2 = 0,62 + 0,03 log([ 0,1]/ [0,1]2) = 0,62 +0,03 log 10 ; E2 =0,65 V. Tracer les diagrammes de prédominance des espčces relatives ŕ ces couples et conclure quand ŕ la stabilité du diiode ŕ ces pH. IO3- aq+ 6H+aq + 6e- = I- aq+ 3H2O. E3 =E°(IO3- aq/ I- aq) + 0,01 log([IO3- ][H+]6/ [ I- ]) E3 =E°(IO3- aq/ I- aq) + 0,01 log ([IO3- ]/ [ I- ]) -0,06 pH
Que se passe t-il si on acidifie, sans variation de volume, la solution jusqu'ŕ pH=0 ? Médiamutation : obtention d'un degré d'oxydation intermédiaire ŕ partir de composés de degrés d'oxydation différents. 2IO3- aq+ 12H+aq + 10e- = I2aq+ 6H2O.(2) 10I-aq= 5I2aq+10e-. (3) (2) + (3) donne : IO3- + 5I- + 6 H+= 3I2 + 3H2O. (4) Calculer la constante d'équilibre correspondante. K = [I2]3 /([IO3-][I-]5[H+]6). E1 = E°(IO3- aq/I2aq ) + 0,06/10 log([IO3- ]2[H+]12/ [ I2]) E2 = E°( I2aq/I-aq ) + 0,03 log([ I2]/ [I-]2) A l'équilibre E1 =E2 : E°(IO3- aq/I2aq ) + 0,06/10 log([IO3- ]2[H+]12/ [ I2]) = E°( I2aq/I-aq ) + 0,03 log([ I2]/ [I-]2) E°(IO3- aq/I2aq ) - E°( I2aq/I-aq ) = 0,03 log([ I2]/ [I-]2) -0,006 log([IO3- ]2[H+]12/ [ I2]) E°(IO3- aq/I2aq ) - E°( I2aq/I-aq ) =0,006 log ([ I2]6/ ([IO3- ]2[H+]12[I-]10)) E°(IO3- aq/I2aq ) - E°( I2aq/I-aq ) =0,012 log K log K = (1,19-0,62) / 0,012 ; log K= 47,5 ; K = 3,2 1047. Valeur trčs grande, la réaction est quantitative. Quelle concentration maximale en diiode peut-on obtenir ? "n1 = 1,00 10-4 mole d'iodate de sodium (Na+ ; IO3-) et n2 = 2,00 10-2 mol d'iodure" L'ion iodate est en défaut ( réactif limitant) . D'aprčs les nombres stoechiométriques de (4) : n(I2 )= 3 n(IO3-) = 3n1 = 3,00 10-4 mole de diiode dans V= 0,100 L [I2]max = 3,00 10-3 mol/L.
Quel doit ętre le pH de la solution pour obtenir 90% de cette concentration maximale en diiode ? [I2] =0,9 [I2]max = 2,70 10-3 mol/L soit xf = [I2] *V =2,70 10-4 mol
L'expression de K donne : [H+]6 = [I2]3/(K [IO3-][I-]5. [H+]6=( 2,70 10-3)3/[1047,5*10-4*0,19555]= 0,697 10-48. [H+] = 0,94 10-8 ; pH= 8,0.
|
|||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||
|
|