|
Etude et exploitation du diagramme E=f(pCN) de l'or : cyanuration de l'or BTSchimiste 2008. En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts. |
||||||||||||||||||||||||
| .
. |
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|
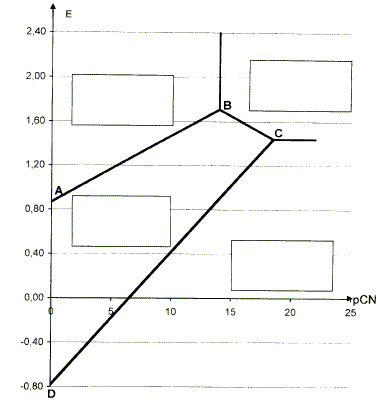
On donne le diagramme E= f(pCN). Il fait intervenir les nombres d'oxydation 0, I et III de l'or. Ce diagramme a ťtť ťtabli pour une tempťrature de 298 K et une condition de concentration pour chaque espŤce soluble de l'ťlťment or sur une frontiŤre telle que : c= 1,0 10-3 mol/L.
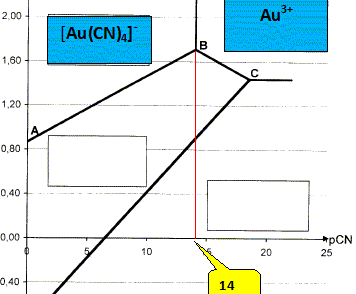
Calculer la valeur de pCN sur la frontiŤre correspondant au systŤme [Au(CN)4]- /Au3+. On donne la constante de formation globale du complexe [Au(CN)4]- : log b4 =56. sur la frontiŤre [
[Au(CN)4]-]
= [Au3+] par suite : log b4
=-4 log [CN-] = 4 pCN =
56 ; pCN =
14. Le complexe prťdomine lorsque [CN-] est ťlevť, c'est ŗ dire pCN faible : donc ŗ gauche de cette frontiŤre.
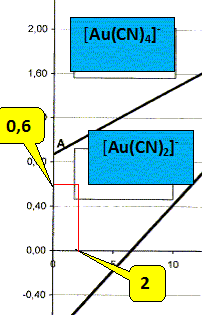
Ecrire la demi ťquation ťlectronique du couple [Au(CN)2]- /Au(s). Calculer le potentiel standart de ce couple et ťtablir la relation entre le potentiel de frontiŤre de ce couple et pCN. On donne : constante de formation globale de [Au(CN)2]- : log b2 = 38 et le potentiel standard du couple Au+/Au(s) : Eį1 = 1,68 V. Au(s) =Au+ + e- ; E1=Eį1 +0,06 log [Au+]. (1) Au+ + 2 CN- = [Au(CN)2]-
Sur la frontiŤre [ [Au(CN)2]-] = 1,0 10-3 mol/L d'oý : E1= -0,60 +0,12 pCN-0,06*3 ; E1= -0,78 +0,12 pCN.
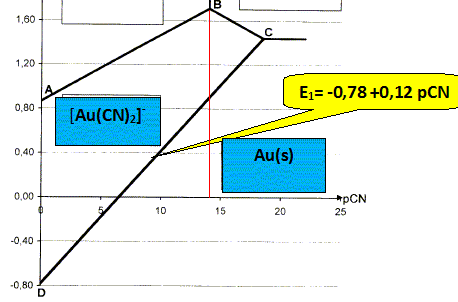
Quel phťnomŤne est mis en ťvidence au point C ? Donner l'ťquation de la rťaction correspondante. Au point C il y a ťquilibre entre trois espŤces : Au(s), [Au(CN)2]- et [Au(CN)4]- 3 [Au(CN)2]- = 2Au(s) + [Au(CN)4]- + 2 CN- : dismutation de [Au(CN)2]- . Etablir par le calcul la pente du segment BC. On donne : potentiel standard du couple Au3+/Au+ : Eį2= 1,41 V ; potentiel standard du couple Au3+/Au : Eį3= 1,50 V Sur la frontiŤre BC, il y a ťquilibre entre [Au(CN)2]- et Au3+. Au+ = Au3++ 2e- : E2 = Eį2+ 0,03 log [Au3+] / [Au+] (2)
E2 = 1,41 +0,03*38 +0,06 log[CN-] ; E2 = 2,55 - 0,06pCN.
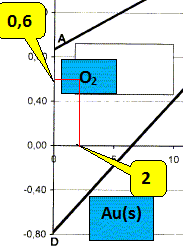
Au cours d'un traitement d'un minerai d'or, l'or mťtal qu'il contient est soumis ŗ l'action d'une solution aqueuse de cyanure de sodium NaCN, de concentration 0,010 mol/L, saturťe en dioxygŤne gazeux, et maintenue ŗ un pH = 10,5 par addition de chaux. Cette opťration porte le nom de cyanuration de l'or. Prťciser pourquoi la sťcuritť impose de s'ssurer que le milieu est nettement basique. On donne la constante d'aciditť du couple acidobasique HCN / CN- : pKa = 9,2. L'acide cyanhydrique HCN est extrÍmement toxique : ŗ pH =10, cet acide est minoritaire tandis que l'ion cyanure CN-, sa base conjuguťe est majoritaire. Etablir la relation permettant de calculer le potentiel du couple O2(g) / H2O si le pH est ťgal ŗ 10,5 et sous une pression de dioxygŤne de 1,00 bar. Donner la valeur numťrique correspondante. On donne le potentiel standard du couple O2(g) / H2O : E4į = 1,23 V. ĹO2(g) + 2H+(aq) + 2e- = H2O ; E4 = E4į + 0,03 log [H+(aq)]2 PĹO2. E4 = 1,23 -0,06 pH. ŗ pH=10,5, E4 = 1,23-0,06*10,5 = 0,6. Lire sur le diagramme E=f(pCN)
de l'or les espŤces solubles de cet
ťlťment pouvant Ítre prťsentes
dans la solution 0,010 mol/L de cyanure de
sodium. Montrer que dans ces conditions, le dioxygŤne doit oxyder l'or. Ecrire l'ťquation de la rťaction correspondante. O2 est
situť au dessus du domaine Au(s) : le
dioxygŤne oxyde l'or. O2 (g) /
H2O : E
= 0,6 V ŗ pH=10,5. ĹO2
+H2O + 2e- = 2HO-.
(1) [Au(CN)2]-
/Au(s) :
E1=
-0,78 +0,12 pCN =
-0,78 +0,12*2 =-0,54 V ŗ pCN=2. 2Au(s) + 4CN-
=2[Au(CN)2]- +
2e-
(2)
(1)
+
(2)
donne : 2Au(s) +
ĹO2 + 4CN- +
H2O =
2[Au(CN)2]- +
2HO-.
|
||||||||||||||||||||||||
|
|
||||||||||||||||||||||||
|
|