|
concours Agrťgation 2005 : le fer : structures cristallines ; oxydes de fer ; sites octaŤdrique et tťtraŤdrique. En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
|||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||
|
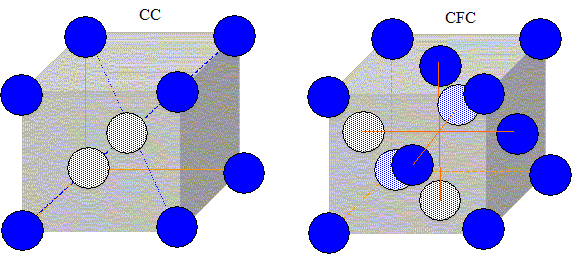
Configuration ťlectronique de l’atome de fer ( Z=26) dans son ťtat fondamental : 1s2 2s2 2p6 3s2 3p6 3d6 4s2. Nature des ions les plus courants de cet ťlťment : Fe2+ 1s2 2s2 2p6 3s2 3p6 3d6 ( perte facile des 2 ťlectrons 4s2) et Fe3+ 1s2 2s2 2p6 3s2 3p6 3d5 ( la couche 3d5 est ŗ moitiť pleine). Structure cristalline du fer et du monoxyde de fer : On s’intťresse ŗ deux variťtťs allotropiques du fer qui existent sous la pression atmosphťrique : - pour t < 912 įC, le fer a (Fe a) - pour 912 įC < t < 1538 įC, le fer g (Fe g ). Le fer a cristallise dans un systŤme cubique centrť (CC) tandis que le fer g cristallise dans un systŤme cubique ŗ faces centrťes (CFC). Reprťsentation des mailles ťlťmentaires de type CC et CFC :
Calcul de la masse volumique thťorique des variťtťs allotropiques du fer a et du fer g. M(fer) = 55,85 g/mol
Les atomes de fer sont tangents suivant la grande diagonale du cube, de longueur 3Ĺa = 4 Ra. Ra = 3Ĺa / 4 = 3Ĺ * 287 /4 = 124 pm. Rayon maximum des atomes susceptibles de s’insťrer dans chacun des sites aprŤs avoir localisť et dťnombrť ceux-ci :
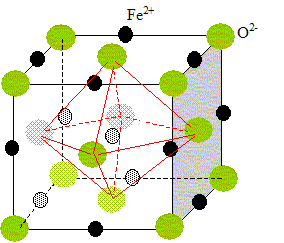
Le fer et le carbone donnent des solutions solides ; or les rayons du fer ( 124 pm) et du carboen (77 pm) sont trŤs diffťrents : ce ne sont pas des olutions solides de substitution. Les rayons des sites tťtraŤdrique et octaŤdrique ťtant infťrieurs ŗ 77 pm, il y a insertion du carbone et dťformation de la maille. Le monoxyde de fer, de formule FeO, est un solide ionique qui cristallise dans une structure de type NaCl. L'oxygŤne dans les oxydes mťtalliques est sous forme d'ion oxyde O2-. La maille cristalline : les ions oxyde constituant le rťseau hŰte, les cations occupent les ites octaŤdriques avec une coordinence, nombre de plus proches voisins ( anions oxydes) ťgale ŗ 6.
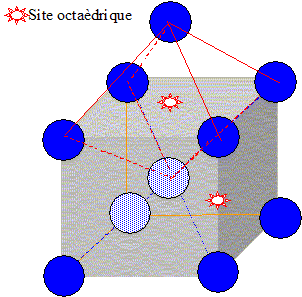
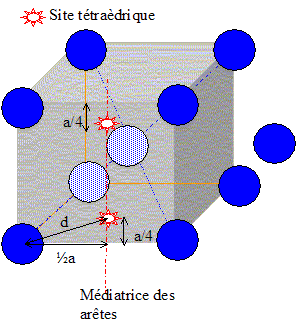
Nombre de sites octaťdriques dans une maille ťlťmentaire CFC : 1 au centre et les milieux de chaque arÍtes ( appartenant chacun ŗ 4 maille) : total : 1 + 12/4 = 4 sites octaŤdriques. Nombre de sites tťtraťdriques dans une maille ťlťmentaire CFC : 8 par maille.
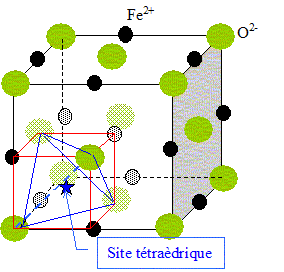
On considŤre la structure dans laquelle la moitiť des sites octaťdriques sont occupťs par des ions Fe3+ ( 2 ions Fe3+ par maille) et 1/8 des sites tťtraťdriques par des ions Fe2+ ( 1 ion Fe2+ par maille). Ion oxyde : 4 par maille. La formule stoechiomťtrique de cet oxyde est : Fe3O4. Dimension des sites dans un rťseau d'ions O2-CFC non dťformť :
Connaissant la masse volumique de cet oxyde( r= 5,18 103 kg m-3), calcul de la valeur de l'arÍte a de la maille supposťe rťguliŤre dans tout le rťseau. Dans le cas d'un rťseau d'ion oxyde non dťformť : a =2*2ĹRO2- = 2*2Ĺ*132 = 373 pm ; volume de la maille : V= a3 ; masse de la maille : m = 3 mFe + 4 mO = (3 MFe + 4MO)10-3/NA m =(3*55,85+4*16)10-3 / 6,02 1023 = 3,846 10-25 kg r= m/a3 soit a3 = m/r = 3,845 10-25 / 7,43 103 =2,05 10-29 m3 ; a = 420 pm, valeur supťrieure ŗ 373pm, ce qui confirme la dťformation du rťseau.
|
|||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||