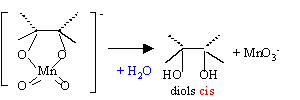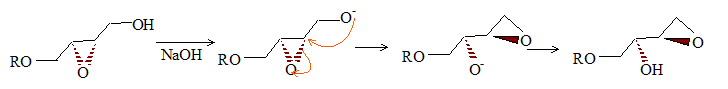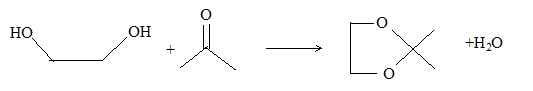|
Agrťgation 2005 : les epoxydes, les diols En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
|||
| .
. |
|||
|
|||
|
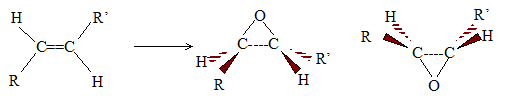
L'acide mťtachloroperoxybenzoÔque ( m-CPBA), le dioxygŤne en prťsence de catalyseur ŗ base d'argent, permettent de passer d'un alcŤne ŗ l'ťpoxyde. Le pont "oxygŤne se forme soit au dessus du plan de la double liaison, soit en dessous : en consťquence, ŗ partir de l'alcŤne suivant, plusieurs ťnantiomŤres sont obtenus.
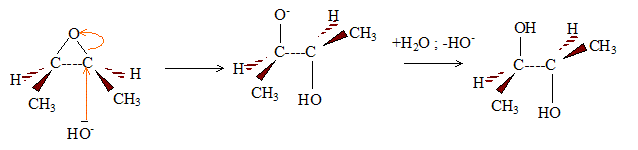
Par hydrolyse acide ou basique d'un ťpoxyde, on obtient un diol :
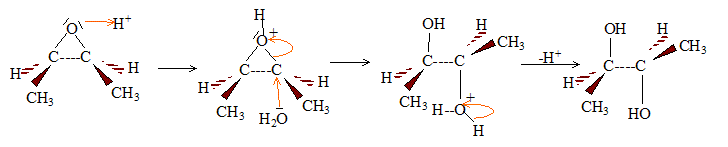
L'attaque initiale de HO- est ťquiprobable sur chaque carbone : on obtient donc les deux ťnantiomŤres dans la mÍme proportion ( mťlange racťmioque). En milieu acide l'attaque initiale de H+ porte sur l'atome d'oxygŤne.
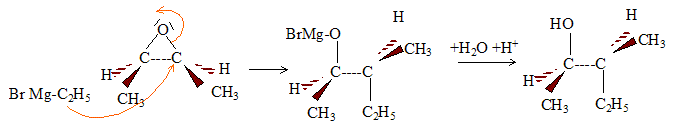
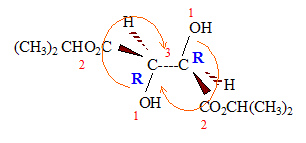
En RMN du proton 1H, ce diol donne trois signaux du fait de la symťtrie de la molťcule : le signal du proton du groupe OH ( singulet), trŤs dťblindť ; le signal des 3 protons du groupe CH3 ( doublet), le moins dťblindť ; le signal de l'hydrogŤne fixť sur le carbone ( quadruplet), dťblindť par la prťsence de l'atome d'oxygŤne. Par action de l'organomagnťsien C2H5-MgBr, suivie d'une hydrolyse, sur un ťpoxyde, on obtient un alcool :
La synthŤse stťrťosťlective des ťpoxydes proposťe par Sharpless a ťtť rťalisťe ŗ partir d’un alcool allylique en prťsence d’un complexe chiral ŗ base de titane . Ce complexe fait intervenir, selon les cas, le (+ ou dextrogyre )-tartrate de diisopropyle ou le (- ou lťvogyre)-tartrate de diisopropyle, que l’on notera respectivement (+)-DIPT ou (-)-DIPT. La formule du (+)-tartrate de
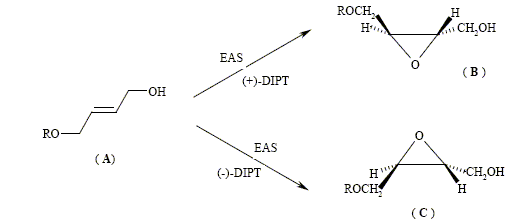
diisopropyle est : Le mťcanisme de l’ťpoxydation asymťtrique de Sharpless (que l’on notera EAS) est complexe : il fait intervenir une association entre le tartrate, le titane, et la fonction alcool de l’alcool allylique ; on ne donnera que le rťsultat (le rendement est significatif dans chaque cas) obtenu ŗ partir du composť (A) reprťsentť ci-dessous :
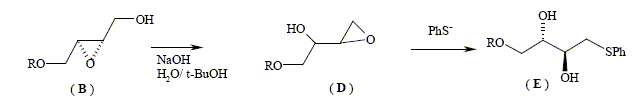
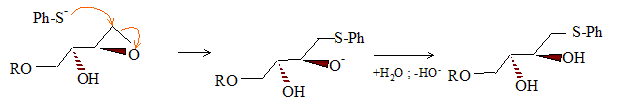
Le stťrťoisomŤre obtenu dťpend donc de la nature du DIPT utilisť. La suite est effectuťe ŗ partir de (B). Dans la molťcule (A), R reprťsente le groupement (C6H5)2CH- que l’on pourra noter Ph2CH oý Ph est le symbole du noyau benzťnique. Nom de A : (E)-6,6-diphťnyl-5-oxahex-2-ťn-1-ol. L’hydrolyse du composť (B) est rťalisťe en milieu basique, et en prťsence de PhS-, ion phťnylthiolate. On a pu mettre en ťvidence les transformations successives (rťarrangement de Payne) :
La prťsence du noyau
benzťnique augmente l’aciditť de Ph-SH
par rapport ŗ un thiol RSH (R ťtant un
groupement alkyle) : en effet le doublet ťlectronique
prťsent dans la base conjuguťe
Ph-S- est dťlocalisť sur le noyau
benzťnique ; la base conjuguťe en sera
d'autant plus stable et en consťquence
l'hydrogŤne sera plus mobile ( aciditť
augmentťe)
La rťaction d'estťrification d'un alcool conduit ŗ l'ester ; l'hydrolyse de l'ester donne l'alcool de dťpart : en passant ŗ l'ester, on protŤge la fonction alcool. De mÍme, l'amide est le protecteur la fonction amine ; l'hydrolyse acide de l'amide conduit ŗ l'amine de dťpart. Le diol est protťgť par la formation d’un acťtal :
Dans un cas gťnťral, la rťaction de formation d’un acťtal ŗ partir d’une mole d'acťtone et de deux moles d’alcool ROH est une rťaction ťquilibrťe peu en faveur de l’acťtal ; dans le cas ci-dessus (formation d’un acťtal cyclique) l’ťquilibre est beaucoup plus en faveur de l’acťtal. Pour dťplacer
l'ťquilibre vers la formation de l'acťtal, on
peut utiliser un rťactif en excŤs, ou
ťliminer l'un des produits au fur et ŗ mesure
qu'il se forme par distillation.
|
|||
|
|
|||
|
|