|
concours assistant ingťnieur chimiste, sciences des matťriaux 2006 En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
|||||
| .
. |
|||||
|
|||||
|
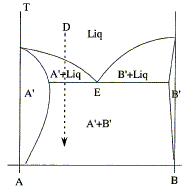
On considŤre le diagramme d'ťquilibre suivant entre deux mťtaux A et B en fonction de la tempťrature.
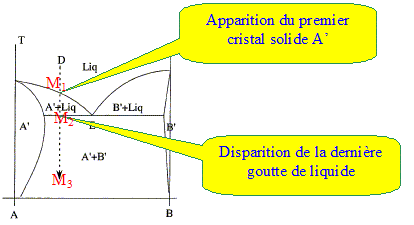
Quel genre de morphologie typique observe t-on pour un alliage riche en A refroidi lentement depuis l'ťtat liquide selon la verticale D ? rťponse : solution solide de substitution A' et B' : les deux solides cristallisent dans le mÍme type de rťseau cristallin avec des paramŤtres de mailles voisins; l'un des solides peut prendre la place de l'autre dans le rťseau. Le premier cristal de A' apparaÓt ( point M1). La composition du liquide suit la courbe M1E ; la phase liquide s'appauvrit en A. En E apparaissent les premiers cristaux de B. Au point M2 il y a disparition de la derniŤre goutte de liquide. La tempťrature diminue encore et on arrive ŗ M3.
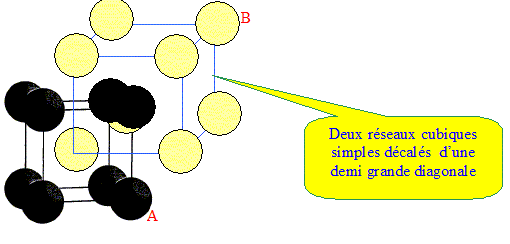
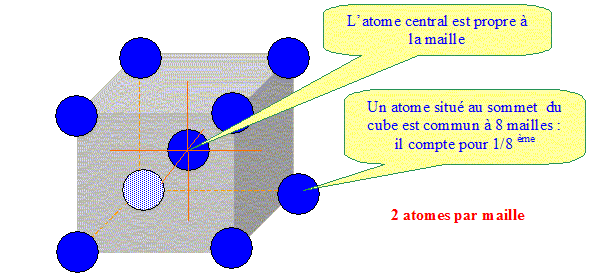
MÍme question pour un alliage ayant la composition du point E ? eutectique : mťlange de deux corps purs qui fond et se solidifie ŗ tempťrature constante. Du point de vue de la fusion, l'eutectique se comporte comme un corps pur. Un alliage (A, B) prťsente une structure cristallographique cubique dont la maille est reprťsentťe ci-dessous avec les atomes A en noir et les atome B en blanc. - Cet alliage est-il cubique simple, cubique centrť ou cubique ŗ faces centrťes ? - Quelle est sa composition chimique AnBm ? rťponse :
Chaque maille compte un atome de A et un atome B d'oý la composition chimique AB.
Une mongolfiŤre gonflťe ŗ l'air chaud ŗ 90įC possŤde un volume de 1500 m3 en un lieu oý la pression est de P0=1 bar. L'air se comporte comme un gaz parfait R= 8,31 J K-1 mol-1 ; Mair = 29 g/mol. Calculer la masse de lest total ( incluant la nacelle et l'enveloppe) nťcessaire pour maintenir la mongolfiŤre en ťquilibre : La mongolfiŤre est en ťquilibre sous l'action de son poids ( P= mg ) et de la poussťe d'ArchimŤde due ŗ l'air P= rair V g. loi des gaz parfaits : PV= nRT avec n= masse (g) / masse molaire (g/mol) = m/M d'oý rair = m/V = PM/(RT). rair = 105*29 10-3 / (8,31*(273+90)) = 0,961 kgm-3. mg = rair V g donne m = rair V= 0,961*1500 =1442 kg. Calculer le plafond thťorique : La masse de l'aťrostier et de son ťquipement est de 100 kg. La tempťrature est supposťe constante ( 25įC) ainsi que le volume de l'enveloppe. L'ťvolution de la pression avec l'altitude est donnťe par P= P0 exp (-H/7,5) avec H en km. m = rair V=PVM/(RT) = P0 exp (-H/7,5) VM/(RT) exp (-H/7,5) = mRT/(P0M V) = 100 *8,31*(273+25) / ( 105*0,029*1500) = 0,0569 -H/7,5 = ln 0,0569 = -2,866 soit H= 2,866*7,5 = 21,5 km.
Ordre de grandeurs des valeurs physiques suivantes : Tempťrature de l'azote liquide : -196 įC ou 77 K. Les tempťratures de fusion du cuivre ( 1083 įC ), du fer ( 1535 įC ) , du tungstŤne (3410 įC). La tempťrature de ramollissement du verre : 610 įC La vitesse du son dans l'air
:
330 m/s.
26 protons et 56-26 = 30 neutrons. Donner la valeur de Z pour l'ion Fe2+. Z=26, ťlťment fer. Donner la configuration ťlectronique du fluor : F ( Z= 9). 1s2 2s2
2p5.
Reprťsenter une maille, donner le nombre d'atomes par maille :
Calculer la masse volumique et en dťduire la densitť du chrome : masse de deux atomes de chrome : 2*MCr/NA = 2*0,052/ 6,023 1023 = 1,726 10-26 kg. volume de la maille : a3 = (2,8879 10-10)3= 2,41 10-30 m3. masse volumique : m/V = 1,726 10-26 / 2,41 10-30 = 7,17 103 kg m-3. densitť :
d=
7,17.
Quelle est la concentration massique en H2SO4 ? masse d'acide pur dans 1 L : 1,78*0,86 = 1,53 kg /L = 1531 g/L. Quelle est la concentration molaire en H2SO4 ? masse molaire H2SO4 : M= 98 g/mol 1531 / 98 = 15,6 mol/L. Quel volume faut-il prťlever pour prťparer 1 L de solution 6 M ? Facteur de dilution : F= 15,6 / 6 = 2,6 volume ŗ prťlever : 1/2,6 =0,385 L = 385 mL. |
|||||
|
|
|||||
|
|