|
chimie
organique, calcul de pH, spectromťtrie de masse,
chromatographie en phase gazeuse concours
Cnrs 2003 En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
|
| .
. |
|
|
|
|
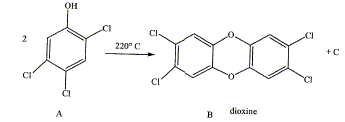
La dioxine est produite ŗ partir du 1,2,4,5-tťtrachlorobenzŤne antiseptique utilisť dans l'industrie pharmaceutique et c'est un intermťdiaire dans la fabrication des pesticides ( contre termites).
Nommer les groupes caractťristiques (fonction chimique ) des produits A et B. Equilibrer la rťaction A donnant B, quel composť C se forme ? Comment mettre en ťvidence la nature chimique de C ? Comment le dťtruire.
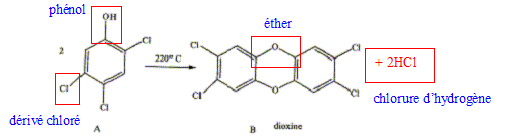
Le chlorure d'hydrogŤne est trŤs soluble dans l'eau : il donne une solution d'acide chlorhydrique. Celle-ci en prťsence d'une base conduit ŗ
un sel.
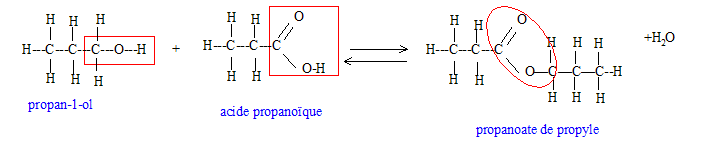
Soit les rťactions successives suivantes : (A) CH3-CH2-CH2OH ---> (B) CH3-CH2-CHO ---> (C) CH3-CH2-COOH Donner la formule dťveloppťe de ces produits. Quelles sont les fonctions chimiques de ces produits ? Ces rťactions sont-elles des rťactions de rťduction, d'hydrolyse, de couplage, d'oxydation ? Deux produits parmi A, B, C peuvent rťagir ensemble, lesquels ? Ecrire la rťaction ; quel est son nom ? Est une rťaction totalement dťplacťe, ťquilibrťe, ne se fait pas. En cas de rťponse "ťquilibrťe", comment dťplacer l'ťquilibre ? 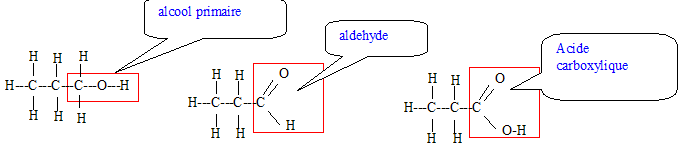
Rťaction d'oxydation mťnagťe d'un alcool primaire en aldehyde puis acide carboxylique. L'alcool A peut rťagir avec l'acide carboxylique C pour conduire ŗ un ester et de l'eau.
La rťaction d'estťrification est limitťe ťquilibrťe ) par l'hydrolyse de l'ester. En utilisant un rťactif en excŤs ( ou en ťliminant l'un des produits au fur et ŗ mesure qu'il se forme), on dťplace l'ťquilibre vers la droite, formation de l'ester.
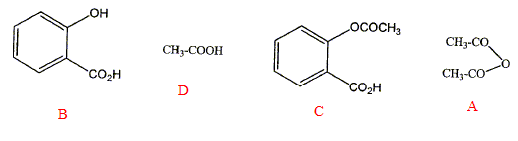
Question 3 : SynthŤse d'un ester ŗ partir d'un anhydride d'acide et d'un alcool. L'aspirine est prťparťe suivant cette rťaction. L'ester C est ici l'aspirine ou acide acťthylsalicylique. (A) anhydride d'acide + (B) alcool ---> (C) ester + (D) acide carboxylique. Les produits de la rťaction sont listťs ci-dessous : attribuer ŗ chacun d'eux la lettre A, B, C ou D correspondant ŗ leur fonction.
On souhaite prťparer 100 kg d'aspirine, le rendement thťorique de la rťaction est 95 %. Quelle masse d'acide salicylique faut-il utiliser ? (C : 12 ; H : 1 ; o : 16 g/mol)
Masse molaire de l'aspirine C9H8O4 : M = 9*12+8+4*16 = 180 g/mol Quantitť de matiŤre d'aspirine (mol) = masse (g) / masse molaire (g/mol) n(aspirine) = 100 000 / 180 = 555,56 mol D'aprŤs les coefficients stoemťtriques de l'ťquation : n(aspirine) = n( acide salicylique) masse (g) = quantitť de matiŤre(mol) * masse molaire (g/mol) m(acide salycilique) = 555,56*138 = 76,66 kg tenir compte du rendement : 76,66 /
0,95 = 80,7
kg.
Dans un catalogue de produits chimiques on a relevť les informations suivantes : "glutaraldťhyde 25 % en solution ; C5H8O2 ; M= 100,12 g/mol ; d=1,06. Quelle est la concentration du
glutaraldťhyde en solution ?
Quantitť de matiŤre
de glutaraldťhyde en solution = masse (g) / masse
molaire (g/mol) = 265/100,12 =
2,65 mol dans 1
L.
couple
(NH4+ / NH3) :
pKa =9,26.
[NH3] /[NH4+] =5,75 On note v (mL) le volume de solution de NH4Cl ajoutť : [NH4+] =0,34 v/(250+v) ; [NH3] =0,82*250/(250+v) [NH3]
/[NH4+] =0,82*250/0,34 v =
5,75 ; v= 0,82*250 /(0,34*5,75)
=105
mL.
De quelle(s) faÁon(s) peut-on procťder ? Le facteur de dilution est : 1/0,0005 = 2000. - 2 dilutions successives : 5 mL dans une fiole jaugťe de 100 mL, puis 10 mL dans une fiole jaugťe de 1000 mL Facteur de dilution : 100/5 * 1000/10 = 20*100=2000 ( correct). -2 dilutions successives : 20 mL dans une fiole jaugťe de 100 mL, puis 5 mL dans une fiole jaugťe de 1000 mL. Facteur de dilution : 100/20 * 1000/5 = 5*200=1000 ( incorrect). - 2 dilutions successives : 5 mL dans une fiole jaugťe de 50 mL, puis 5 mL dans une fiole jaugťe de 1000 mL. Facteur de dilution : 50/5 * 1000/5 = 10*200=2000 (correct). - 2 dilutions successives : 25 mL dans une fiole jaugťe de 1000 mL, puis 20 mL dans une fiole jaugťe de 1000 mL. Facteur de dilution : 1000/25 *
1000/20 = 40*50=2000
(correct).
pico = 10-12 ; femto = 10-15 ; nano = 10-9 ; micro = 10-6 ; atto = 10-18; dťci = 0,1.
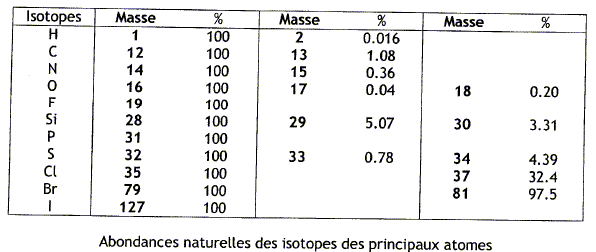
L'ionisation est une opťration permettant de produire : - Un ion ŗ partir d'un atome ou d'une molťcule neutre. (correct) - un atome ŗ partir d'un atome ou d'une molťcule neutre. - Une molťcule neutre ŗ partir d'un atome ou d'un ion. Un spectromŤtre de masse est : - Un instrument qui analyse les molťcules suivant le rapport m/z. - Un instrument qui analyse les ions suivant le rapport m/z. (correct ) - Un instrument qui analyse les composťs suivant le rapport m/z. Lors de l'analyse par spectromŤtrie de masse, on produit des ions molťculaires, de quoi s'agit-il ? - Un ion issu d'une molťcule par perte ou gain d'un proton. - Un ion issu d'une molťcule par perte ou gain d'un ťlectron. (correct) - Un ion issu d'une molťcule par perte ou gain d'un neutron. L'analyse par spectromtrie de masse du benzŤne permet de dťtecter un pic intense ŗ M= m/z = 78, ceci correspnd au pic de base du spectre. Un pic plus petit apparaÓt ŗ M+1 = 79. Comment expliquer la prťsence de ce pic ? Quelle est son abondance relative ?
La prťsence de ce pic est dues aux isotopes du carbone ( 13C : 1,08%) et de l'hydrogŤne ( 2H : 0,016%). Abondance relative : 1,08+0,016 =
1,1 %.
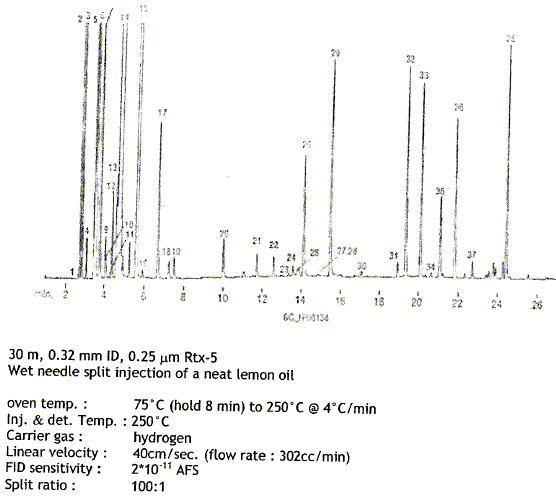
La grandeur expťrimentale caractťristique est le temps de rťtention, cette grandeur est-elle dťpendante ou indťpendante des paramŤtrs suivants : - Dťbit du gaz porteur ( dťpendant) - Quantitť injecťe ( indťpendante) - Nature et abondance des autres constituants, s'ils sont bien sťparťs ( indťpendante). - Phase stationaire ( dťpendant) - Tempťrature de la colonne
( dťpendant).
La colonne est-elle polaire, apolaire ? apolaire.( 5% diphťnyl : substituant apolaire) Parmi les 38 composťs dťtectťs, attribuer l'ordre de sortie aux composťs suivants ( la valeur indiquťe entre parenthŤse correspond ŗ la tempťrature d'ťbullition) limonŤne (176į ), gťraniol (230į ), nťrol (224į), linalol (198į), camphŤne (159į). Sťparation des produits suivant leur point d'ťbullition ; les composťs ayant les points d'ťbullition les plus ťlevťs sont les plus polaires. Ils prťsentent peu d'affinitť pour la phase fixe d'oý l'ordre de sortie : gťraniol, nťrol, linalol, limonŤne, camphŤne. Le temps de rťtention du composť 33 est de 20 min, quelle est la tempťrature du four ? Quel type de dťtecteur a ťtť utilisť ? dťtecteur ŗ ionisation de flamme : trŤs sensible Citez trois autre dťtecteurs utilisables en chromatographie en phase gazeuse. - dťtecteur ťlectrique, basť sur le principe du pont de Wheatstone ( catharomŤtre ) - dťtecteur ŗ absorption ťlectronique - spectromŤtre de masse et la spectroscopie infrarouge. |
|
|
|
|
|
|