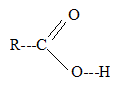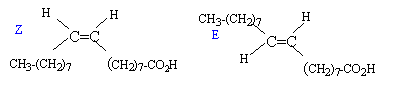|
Bts esthťtique 2002 : olťine ; ťlectricitť; gaz parfait En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
|||
| .
. |
|||
|
|||
corrigť La mťthode VSEPR permet de prťvoir la gťomŤtrie d'une molťcule ŗ partir du nombre de directions de liaisons et du nombre de doublets non liants de l'atome central. Les doublets liants et non liants se repoussent et se disposent le plus loin possible les uns des autres. Le carbone du groupe acide carboxylique possŤde 3 directions de liaisons et aucun doublet non liant : d'oý le type AX3.
Dans l'hypothŤse d'une chaÓne carbonťe saturťe, ŗ partir de 17 atomes de carbone, on s'attend ŗ 17*2+1 = 35 atomes d'hydrogŤne. Or la chaÓne C17H33- ne compte que 33 atomes d'hydrogŤne : celle-ci est insatuťre ( prťsence d'une double liaison >C=C< ) L'acide olťique prťsente une isomťrie de type Z E : diastťrťoisomťrie.
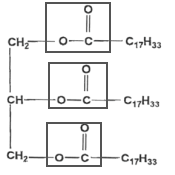
La molťcule d'olťine, ťcrite ci-dessous compte trois fonctions ester.
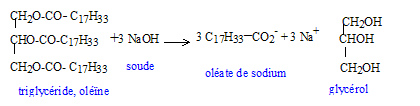
ťquation de la rťaction d'addition du diiode sur l'olťine : C57 H104 O 6 + 3I2 = C57 H104 O 6 I6. Indice d'iode de l'olťine : Le diiode se fixe sur les liaisons doubles carbone carbone ; l'olťine possŤde ce genre de liaisons ( 3 par molťcule) Une mole d'olťine peut donc fixer 3 moles de diiode I2. olťine : C57 H104 O 6 soit 884 g/mol ; diiode : (127+127 ) = 254 g/mol n( olťine) = 35/884 mole ; n(I2 ) = 3 n(olťine) = 3 *35/884 =0,119 mol indice d'iode : 3*254*35/884 = 30,2 saponification, lente mais totale :
glycťrol ou propan-1,2,3 triol. savon obtenu : olťate de sodium ; un savon est amphipile ( il possŤde une extrťmitť hydrophile -COO- et une longue chaÓne carbonťe lipophile ) masse de savon thťoriquement obtenu : n (olťine ) = 265,2 / 884 = 0,3 mol ; n(savon) = 3*0,3 = 0,9 mol M( savon) =12*178+33+32+23=304 g/mol m = nM = 0,9*304 =273,6 g.
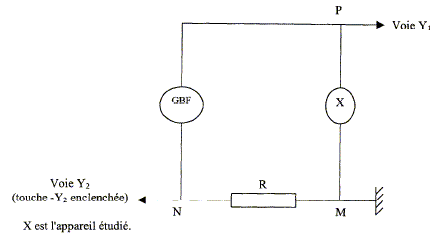
Aux bornes d'un gBF, on branche en sťrie une rťsistance R= 10 W et un appareil ťlectrique notť X utilisť en esthťtique. On visualise deux tensions sur un oscilloscope. La touche -Y2 est enclenchťe et permet d'observer la tension -uNM = uMN.
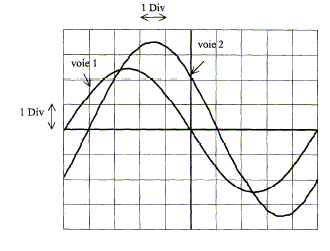
corrigť On visualise sur la voie Y2 une tension proportionnelle ŗ l'intensitť du courant. pťriode T = 10 divisions soit 10*2 = 20 ms = 0,02 s ; frťquence : f=1/T = 1/0,02 = 50 Hz ; pulsation w = 2pf = 6,28*50 = 314 rad/s. La diffťrence de phase entre la tension aux bornes de l'appareil X et l'intensitť du courant correspond ŗ une division soit 0,1 pťriode soit j = 360*0,1 = 36 į = 0,2 p rad. La tension aux bornes de X ( voie 1) est en avance sur l'intensitť ( voie 2) : l'appareil X est donc inductif. Le facteur de puissance est cosj = cos 36 = 0,81. intensitť maximale : voie 2 UNM max = 3,5*2 = 7 V R= 10 W d'oý Imax = 7/10 = 0,7 A. intensitť efficace : Ieff = Imax / 1,414 = 0,5 A. impťdance Z de X : voie 1 Umax = 2,5*5 = 12,5 V Z = Umax / Imax =12,5/0,7 = 17,8 W. puissance moyenne consommťe par X : P = Ueff Ieff cos j avec Ueff = 12,5 / 1,414 = 8,84 V P = 8,84*0,5*0,81 = 3,6 W. puissance apparente : S = Ueff Ieff = 8,84*0,5 = 4,4 VA. |
|||
corrigť
n = 4,00 105 * 2 10-4 (8,32 *293) = 3,28 10-2 mol. nouvelle pression du diazote : T = 273+50 = 323 K P = nRT/V = 3,28 10-2 *8,32*323/2 10-4 =4,4 105 Pa. |
|||
|
|