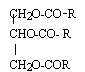|
Bts esthťtique 2001 : acide lactique, triglycťrides, ťlectricitť En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
|||
| .
. |
|||
|
|||
L'huile de ricin est un corps gras utilisť en cosmťtologie. Elle est constituťe essentiellement de triricinolťate de glycťryle, de masse molaire M= 932 g/mol, molťcule insaturťe dťsignťe par A.
corrigť Masse molaire acide lactique C3H6O3 : M =3*12+6+3*16 =90 g/mol. Quantitť de matiŤre (mol) = masse (g) / masse molaire (g/mol) : n = m/M = 18/90 =2,0 10-1 mol. concentration (mol/L) = quantitť de matiŤre (mol) / volume de la solution (L) = n/V = 0,2 / 0,25 =8,0 10-1 mol/L. Equation bilan de la rťaction de l'acide lactique avec l'eau : CH3-CHOH-COOH + H2O = CH3-CHOH-COO- + H3O+. constante d'ťquilibre ou constante d'aciditť du couple acide base CH3-CHOH-COOH /CH3-CHOH-COO- Ka =[ H3O+][CH3-CHOH-COO-] / [CH3-CHOH-COOH] ; pKa = - log Ka c : concentration de l'acide lactique ; pH = - log [ H3O+] avec [ H3O+] exprimťe en mol/L Conditions de validitť de la relation pH= Ĺ( pKa + log c) : solution pas trop concentrťe afin de confondre activitť et concentration ; l'acide doit Ítre peu dissociť afin que CH3-CHOH-COO- soit nťgligeable devant [CH3-CHOH-COOH] pH = 0,5(3,9 + log 8 10-1) =1,9. d'oý [ H3O+]=[CH3-CHOH-COO-]= 10-1,9=1,25 10-2 mol/L et [CH3-CHOH-COOH] = 0,8-0,0125 =0,787 mol/L La relation pH= Ĺ(
pKa + log c) ťtait donc bien appliquable.
Une solution tampon permet de maintenir le pH constant par suite d'une dilution modťrťe. Pour obtenir une lotion de pH ťgal ŗ 3,9 ŗ partir d'une solution d'acide lactique de concentration 0,01 mol/L, il faut ajouter de la soude jusqu'ŗ ce que : [CH3-CHOH-COO-]
=[CH3-CHOH-COOH] =0,01/2 = 0,005 mol/L
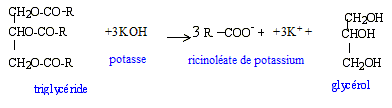
Equation bilan de la saponification d'un triglycťride avec une solution d'hydroxyde de potassium :
Masse d'hydroxyde de potassium nťcessaire ŗ l'obtention de 10 g de ricinolťate de potassium : La masse molaire du triglycťride est ťgale ŗ : 3 masse molaire de R + ( 6*12+5+6*16) M = 3MR + 173 = 932 doý MR= (932-173) / 3 = 253 g/mol M (RCOOK) = 253+12+32+39=336 g/mol n(RCOOK) = m/M = 10/336 = 2,98 10-2 mol d'aprŤs les coefficients de l'ťquation ci-dessus : n( potasse) = n(RCOOK) m(potasse) = 2,98 10-2
*(39+16+1) =1,67 g.
L'hydrogťnation catalytique de A donne une chaÓne carbonťe saturťe. Le produit, corps gras saturť, est un solide. L'indice d'iode d'un corps gras A est la masse de diiode (I2), exprimťe en grammes, que peut fixer 100 g de A. Relation entre les quantitťs de matiŤre de diiode et A : n( triglycťride) = 100 / 932 = 0,107 mol. n(I2) = 82/(2*127) = 0,323 mol d'oý n(I2) = 3 n( triglycťride). La molťcule A compte 3 liaisons doubles C=C.
Un broyeur porte les indications suivantes : 220 V ; 550 W. Cet appareil est constituť d'un moteur qui permet la rotation d'un couteau. La rťsistance interne du moteur vaut r =2W. Le moteur est conÁu pour un fonctionnement assez bref : au delŗ de 7 min d'utilisation il convient de laisser le broyeur se refroidir pendant 10 min. Un interrupteur de protection contre les surintensitťs est intťgrť au circuit ťlectrique de l'appareil. On admettra que les lois du courant continu s'appliquent.
corrigť Intensitť du courant : P= UI soit I= P/U = 550/220 = 2,5 A. Force contre ťlectromotrice du moteur : U = E+rI soit E=U-rI = 220-2*2,5 = 215 V. Puissance dissipťe par effet Joule dans le bobinage du moteur : PJ= rI2 = 2*2,52 = 12,5 W Quantitť de chaleur dissipťe dans le bobinage au bout de 7 min de fonctionnement : Q= PJDt
= 12,5*7*60 = 5,25 kJ.
Puissance dissipťe par effet Joule dans le moteur : rI2 = 2*110*110 = 24 kW. L interrupteur de protection contre les surintensitťs, intťgrť au circuit ťlectrique de l'appareil coupe l'alimentation du moteur ; sinion le moteur serait grillť. |
|||
|
Un appareil ŗ cire est constituť d'une cuve en aluminium de masse 0,25 kg chauffť par une rťsistance thermo-rťgulťe.La puissance ťlectrique de cet appareil est 200 W. La cuve contient 500 g de cire, ressolidifiťe aprŤs fusion et ťpousant la forme de la cuve. L'ensemble est ŗ la tempťrature ambiante de 18įC. Cette cire dite "tiŤde" commence ŗ fondre ŗ 37įC. Le dťbut de la fusion est observť au bout de 2 min 10 s.
corrigť Capacitť thermique massique, notťe c, de la cire solide : ťnergie ťlectrique reÁue en Dt =2 min 10 s = 130 s : Q1= P Dt =200*130 = 2,6 104 J ťnergie reÁue par la cire : Q= m c Dq =0,5 c* (37-18) = 9,5 c ťnergie reÁue par l'aluminium : Q' = m Al cAl Dq = 0,25*895*(37-18) =4,25 103 J Q1 = Q+Q' ; 2,6 104 = 9,5 c + 4,25 103 ; c = ( 2,6 104-4,25 103)/ 9,5 = 2289 J kg-1 K-1. Cette cire n'ťtant pas un corps pur, sa tempťrature de fusion n'est pas constante. Quantitť de chaleur nťcessaire ŗ cette seconde ťtape : P Dt = 200*12*60 = 1,44 105 J Quantitť de chaleur nťcessaire ŗ la fusion de 1 kg de cette cire : 2*1,44 105 = 2,88 105 J kg-1.
|
|||
|
|