|
Le sulfure d'hydrogŤne : un acide, un rťducteur BTS mťtiers de l'eau 2007 En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
|||||
| .
. |
|||||
|
|||||
|
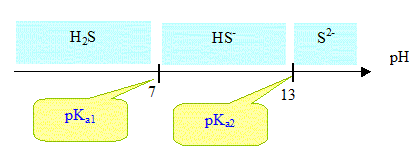
Donnťes : 11H ; 3216S ; 5525Mn. Produits de solubilitť ( ŗ 25 įC) NiS : Ks1 = 10-21 ; MnS : Ks2 = 10-16. Constante d'aciditť : couple H2S/HS- : Ka1 = 10-7 ; couple HS-/S2- Ka2 = 10-13. La molťcule de sulfure d'hydrogŤne : Donner la structure ťlectronique des atomes suivants : hydrogŤne H, soufre S, manganŤse Mn. H : 1 s1 ; S : 1s2 2s2 2p6 3s2 3p4 ; Mn : 1s2 2s2 2p6 3s2 3p6 4s2 3d5 Justifier la formule de l'ion S2-. L'atome de soufre a tendance ŗ complťter ŗ huit sa couche ťlectronique externe ( rŤgle de l'octet ). Pour cela il gagne facilement deux ťlectrons et donne l'ion S2-. Le sulfure d'hydrogŤne est un diacide : Dťfinir un acide au sens de BrŲnsted. Espťce, ion ou molťcule, susceptible de cťder un proton H+. Ecrire les ťquations des rťactions avec l'eau qui se produisent lors de la dissolution de H2S. couples acide / base : H2S/HS- ; H3O+/H2O H2S + H2O = HS- + H3O+ (1) couples acide / base : HS-/S2- ; H3O+/H2O HS- +H2O = S2- + H3O+(2) (1)
Ka1 = [HS-][H3O+]
/ [H2S] (2)
Ka2 = [S2-][H3O+]
/ [HS-] Tracer sur un axe
horizontal de pH, le diagramme de
prťdominance des
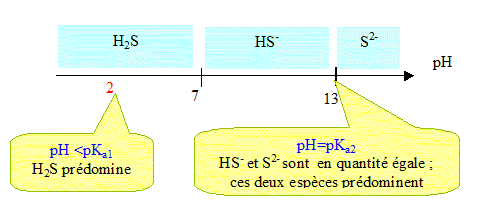
espŤces. Indiquer la ou les espŤce(s) prťdominante(s) ŗ pH=2 et ŗ pH=13.
On considŤre une solution aqueuse de sulfure d'hydrogŤne de concentration C=5,0 10-2 mol/L. On considŤrera que, dans ces conditions, le couple HS-/S2- n'a pas d'influence sur la valeur du pH. Etablir l'expression littťrale du pH de la solution. (1) Ka1 = [HS-][H3O+] / [H2S] Conservation de l'ťlťment soufre : [HS-] +[H2S] = C (3) La solution reste ťlectriquement neutre ( en milieu acide HO- est nťgligeable) : [ HS-]=[H3O+] (4) repport dans (1) : Ka1 = [H3O+]2 / [H2S] (5) (3) donne : [H2S] = C-[HS-] = C-[H3O+] repport dans (5) : Ka1 = [H3O+]2 / (C-[H3O+] ) Dans l'hypothŤse oý C >> [H3O+] il vient : Ka1 = [H3O+]2 / C [H3O+] = (Ka1C )Ĺ. log[H3O+] = Ĺ[logKa1+log C] pH= - log[H3O+] = Ĺ[pKa1-log C]. Calculer la valeur du pH. pH= Ĺ(7-log(0,05)]= 4,2. [H3O+] = 10-4,2 = 7 10-5 mol/L, valeur trŤs infťrieure ŗ C=0,05 ( hypothŤse confirmťe).
Le sulfure d'hydrogŤne est un rťducteur : obtention de soufre. Dťfinir un rťducteur . EspŤce, ion ou molťcule, susceptible de libťrer un ou plusieurs ťlectrons dans un rťaction appelťe "oxydation". Indiquer le nombre d'oxydation (n.o) de l'ťlťment soufre dans H2S(g) et dans S(s). Le nombre d'oxydation de l'ťlťment hydrogŤne est +1 ; dans H2S, la somme des nombre d'oxydation de tous les ťlťments est nulle, doý : n.o(S) + 2 n.o(H) = 0 ; n.o(S) +2 = 0 ; n.o(S) = -2. Dans un corps pur simple, S(s) le nombre d'oxydation de l'ťlťment est nul : n.o(S) =0 dans S(s). Ecrire la demi-ťquation ťlectronique du couple S(s) / H2S(aq) en solution aqueuse). H2S(aq)=S(s) + 2H+(aq) + 2e- (1) Ecrire la demi-ťquation ťlectronique du couple SO2(aq) / S(s) en solution aqueuse). SO2(aq) +4H+(aq) + 4e- = S(s) + 2H2O(l) (2) Ecrire la demi-ťquation ťlectronique du couple SO2(aq) / H2S(aq) en solution aqueuse). Faire 2 fois (1) + (2) : 2H2S(aq) +
SO2(aq) = 3S(s) +2H2O(l)
Si on fixe la pression en sulfure d'hydrogŤne ťgale ŗ 1 bar, ŗ 20įC, la concentration en sulfure d'hydrogŤne en solution aqueuse reste constante et ťgale ŗ [H2S]= 0,10 mol/L. On considŤre une solution contenant des ions nickel et des ions manganŤse telle que [Ni2+]=[Mn2+]=0,010 mol/L. On fait barboter, sous une pression de 1 bar, le sulfure d'hydrogŤne dans la solution et on ťtudie la prťcipitation des sulfure MnS et NiS. Ecrire les ťquations de prťcipitation des deux solides NiS et MnS. NiS(s) = Ni2+(aq) + S2-(aq). Mn(s) =Mn2+(aq) + S2-(aq). Donner l'expression de leur produit de solubilitť Ks. Ks1 = [Ni2+][S2-] Ks2 = [Mn2+][S2-] A partir du produit des constantes d'acicitť Ka1 Ka2 et de la concentration [H2S], vťrifier que [S2-]= 10-21 / [H3O+]2. Ka1 = [HS-][H3O+] / [H2S] Ka2 = [S2-][H3O+] / [HS-] Ka1 Ka2 = [H3O+] 2 [S2-] / [H2S] avec Ka1 Ka2 = 10-20 et [H2S] = 0,1 mol/L [S2-] = Ka1 Ka2 [H2S] / [H3O+] 2 [S2-] = 0,1 10-20 / [H3O+] 2 = 10-21 /[H3O+] 2 . Sachant que la solution est tamponnťe ŗ pH=2, quel est (sont) l'ion ( les ions) qui prťcipite (nt). Justifier. [S2-] = 10-21 / (10-2 )2= 10-17 mol/L [Ni2+][S2-] = 0,01 * 10-17 = 10-19, valeur supťrieure ŗ Ks1 = 10-21 : le produit de solubilitť ťtant atteint, NiS prťcipite. [Mn2+][S2-] = 0,01 * 10-17 = 10-19, valeur infťrieure ŗ Ks1 = 10-16 : le produit de solubilitť n'ťtant pas atteint, MnS ne prťcipite pas.
|
|||||
|
|
|||||
|
|