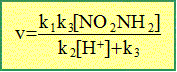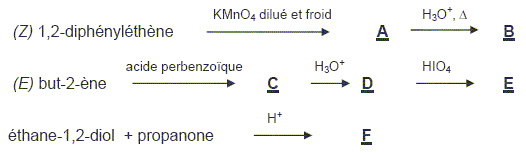|
cinétique : décomposition nitroamine ; chimie organique : alcool et polyol BTS chimiste 2007 En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptés ŕ vos centres d’intéręts. |
||||
| .
. |
||||
|
||||
|
Décomposition de la nitroamine en solution aqueuse : NO2NH2 = N2O+H2O On propose le mécanisme suivant ( ki est la constanbte de vitesse de l'étape i ) : (1) NO2NH2 ---> NO2NH- + H+ k1. (2) NO2NH- + H+ --->NO2NH2 k2. (3) NO2NH- ---> N2O + HO- k3. (4) H+ + HO- ---> H2O k4. Choisir une définition pour la vitesse v de la réaction. v = d[N2O]/dt ou bien v = - d[NO2NH2]/dt. A l'aide de l'approximation des états quasistationnaires appliquée ŕ l'espčce NO2NH- montrer que la vitesse de la réaction est :
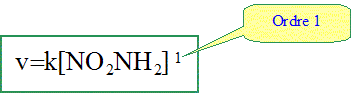
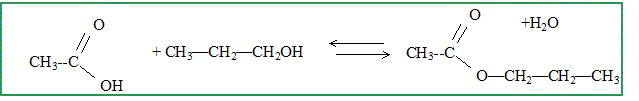
d[ NO2NH-]/dt = 0 =k1[NO2NH2] - k2[ NO2NH-][ H+] -k3[ NO2NH-] d'oů [ NO2NH-] =k1[NO2NH2] / (k2[ H+]+k3) or v = d[ N2O ]/dt =k3[ NO2NH-] =k1 k3 [NO2NH2] / (k2[ H+]+k3). Justifier que dans une solution de pH fixé, la réaction est d'ordre 1. [ H+] = constante ; on pose k = k1 k3 / (k2[ H+]+k3) = constante de vitesse. d'oů Alcool et polyol : Donner les équations des réactions suivantes : acide acétique( éthanoďque) avec le propan-1-ol en présence d'acide sulfurique.
pentan-1-ol avec le chlorure de thionyle SOCl2. CH3-CH2-CH2-CH2-CH2OH + SOCl2 ---> CH3-CH2-CH2-CH2-CH2Cl + SO2 + HCl.
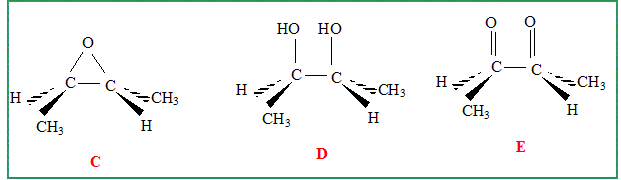
On considčre les suites de réactions ( toutes les synthčses sont indépendantes ) Formules semi-développées de C, D et E .
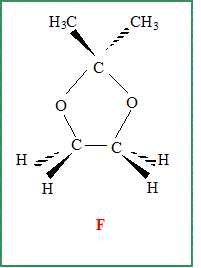
Formule semi-développée de F.
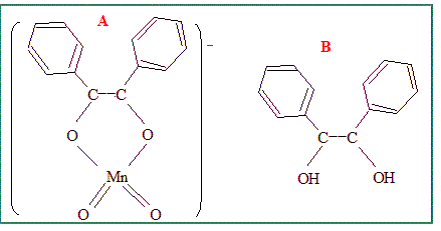
Préciser le mécanisme de la transformation de A en B.
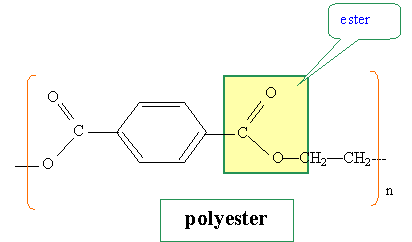
L'éthylčne glycol ( éthane-1,2 diol) réagit avec l'acide téréphtaliqur ( acide benzčne-1,4-dicarboxylique) en milieu acide phosphorique pour donner par polycondensation un polymčre P. Représenter le motif élémentaire de P. A quelle famille de polymčres appartient P ?
|
||||
|
|
||||
|
|