|
Titrage potentiomťtrique du fer dans un produit phytosanitaire bac STL biochimie, gťnie biologique, 2007 France
|
||||
|
||||
|
Le sulfate de fer (Fe2+ + SO42- ) constitue le principe actif de nombreuses solutions destinťes ŗ combattre la chlorose ferrique des vťgťtaux. Il est utilisť pour revitaliser les gazons. L'ťtiquette d'une solution commerciale indique qu'elle contient ,6,0 % en masse d'ťlťment fer soit une concentration molaire ťgale ŗ 1,09 mol/L.
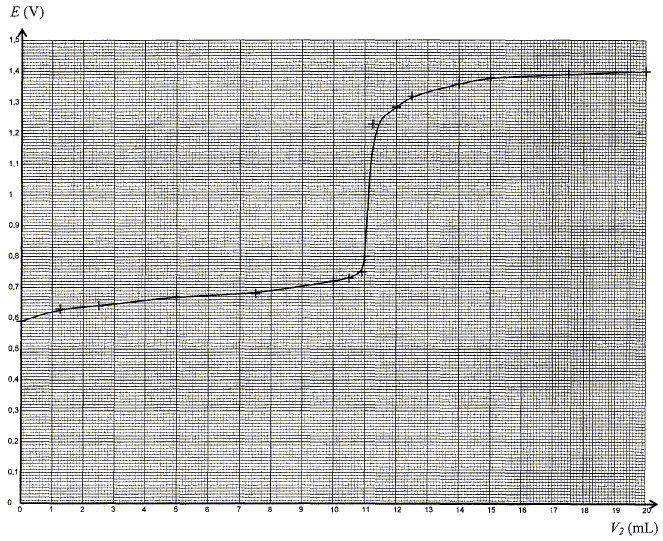
On souhaite dťterminer la concentration c1 en ion fer (II) Fe2+ de la solution S' par titrage potentiomťtrique. Pour cela, on prťlŤve un volume V1 = 10,0 mL de la solution S' dans laquelle on plonge une ťlectrode de mesure et une ťlectrode de rťfťrence. La solution titrante utilisťe est une solution acidifiťe de sulfate de cťrium IV (Ce4+ + 2SO42- ) de concentration c2 = 0,100 mol/L. On note V2 le volume de solution titrante versťe et E le potentiel de l'ťlectrode de mesure donnť par rapport ŗ l'ťlectrode standard ŗ hydrogŤne.
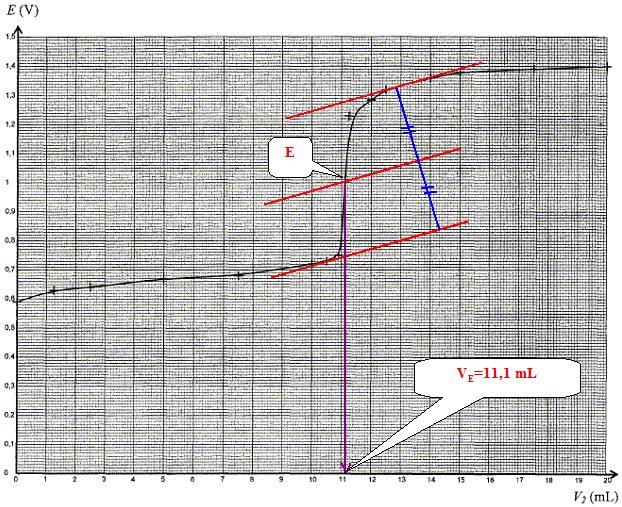
Rťponse : couples oxydant / rťducteur : Fe3+ / Fe2+ : Fe2+ = Fe3+ + e- oxydation. Ce4+ / Ce3+ : Ce4+ + e- = Ce3+ rťduction. Ce4+ +Fe2+ = Fe3+ + Ce3+. A l'ťquivalence du titrage les quantitťs de matiŤre des rťactifs mis en prťsence sont en proportions stoechiomŤtriques. n(Fe2+) =n(Ce4+ ) n(Ce4+ ) = c2 VE ; n(Fe2+)= c1 V1 ; c1 V1=c2 VE ; c1 =c2 VE /V1. c1 = 0,100*11,1/10,0 = 0,111 mol/L ; c = 10 c1 = 1,11 mol/L. ťcart relatif : (1,11-1,09 )/ 1,09 = 0,018 ( 1,8 %). En accord avec l'indication de l'ťtiquette.
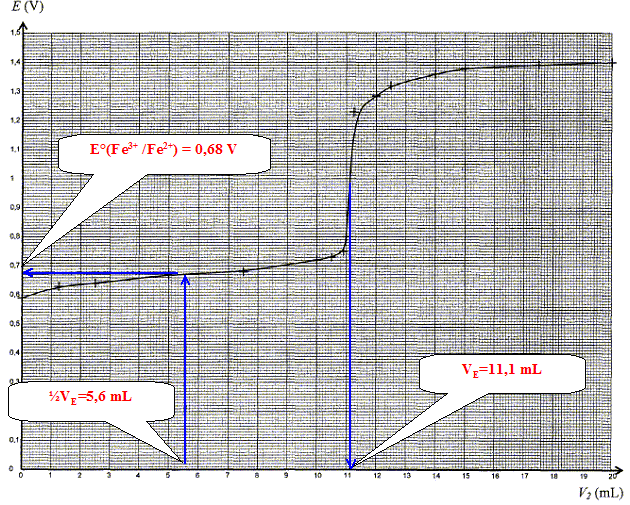
- Ecrire la demi-ťquation ťlectronique relative au couple Fe3+ / Fe2+ puis donner l'expression littťrale du potentiel d'ťlectrode du couple Fe3+ / Fe2+. - Etablir la relation entre les concentrations [Fe2+] et [Fe3+] ŗ la demi ťquivalence c'est ŗ dire pour V=ĹVE. - Donner l'expression littťrale du potentiel d'ťlectrode du couple Fe3+ / Fe2+ ŗ la demi ťquivalence. - Dťterminer graphiquement la valeur du potentiel standard du couple Fe3+ / Fe2+ et comparer avec la valeur thťorique ( 0,68 V). Rťponse : Fe2+ = Fe3+ + e- E = Eį(Fe3+/Fe2+) + RT/F ln ([Fe3+]/[Fe2+]) Quantitť de matiŤre initiale d'ion Fe2+ : n(Fe2+)0= c1 V1 ; c1 V1=c2 VE ; n(Fe2+)0=c2 VE Quantitť de matiŤre d'ion Fe2+ restant ŗ la demi ťquivalence : n(Fe2+)ĹVE= Ĺc1 V1 ; n(Fe2+)ĹVE= Ĺc2 VE Quand une mole d'ion fer II disparaÓt, il se forme une mole d'ion fer III. Quantitť de matiŤre d'ion Fe3+ formť ŗ la demi ťquivalence : n(Fe3+)ĹVE= Ĺc2 VE = n(Fe2+)ĹVE. En consťquence ln ([Fe3+]/[Fe2+]) = ln 1 = 0 et le potentiel d'ťlectrode du couple Fe3+ / Fe2+ vaut : Eį(Fe3+/Fe2+)
|
||||
|
|
||||
|
|