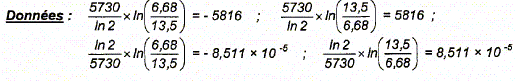|
Radioactivitť,
datation au carbone 14 bac
S 2007 La Rťunion |
|||
|
|||
|
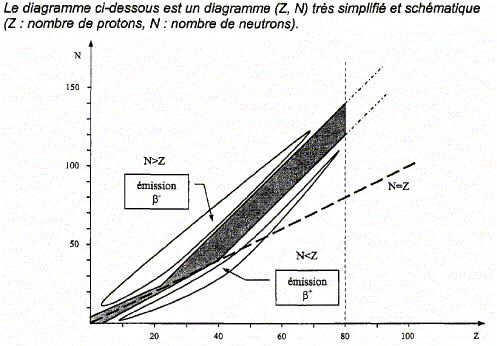
La radioactivitť naturelle fut dťcouverte en 1896 par H. Besquerel. Le signe le plus perceptible de la radioactivitť est l'existence d'un rayonnement ťmis par les atomes de certains nuclťides et dont l'origine se situe au niveau de leur noyau qui est instable. On observe ainsi, par exemple, les rayonnements ( on parle de radioactivitť) b ( bťta+ ou bťta-), qui s'accompagnent souvent d'ťmission g ( gamma), radiation ťlectromagnťtique de mÍme nature que la lumiŤre, provenant du retour ŗ l'ťtat fondamental d'un noyau fils suite ŗ la transmutation d'un noyau pŤre radioactif. Equation de la dťsintťgration nuclťaire, diagramme (Z, N) : Parmi les trois types de radioactivitť ťtudiťs en classe, citer celle qui n'a pas ťtť ťvoquťe dans le texte plus haut. Donner la composition de la particule ťmise lors de cette radioactivitť.
Que reprťsente la zone grisťe dans ce diagramme ?
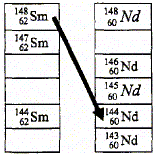
Parmi les trois types de radioactivitť ťtudiťs en classe, la radioactivitť de type a n'a pas ťtť ťvoquťe dans le texte plus haut. La particule ťmise lors de cette radioactivitť est un noyau d'helium 42He ( 2 protons et 4-2 = 2 neutrons). La zone grisťe du diagramme reprťsente la "vallťe de la stabilitť ", ensemble des noyaux stables. Soit la rťaction nuclťaire de transmutation indiquťe par la flŤche ci-dessus : 14862 Sm---> 14460 Nd + AZX Conservation du nombre de nuclťons : 148=144+A soit A=4. Conservation de la charge : 62 = 60 + Z soit Z=2 ; donc ťlťment hťlium La particule ťmise est un noyau d'hťlium 42He : la radioactivitť de type a.
De toutes les mťthodes radio-chronologiques ( basťes sur la loi statistique de Curie-Rutherford-Soddy ou loi de dťcroissance radioactive), celle de la datation au carbone 14 est la plus connue. Dans la haute atmosphŤre, soumis au rayonnement cosmique galactique constituť de protons, des neutrons secondaires interagissent avec les noyaux d'azote 14. Cette rťaction forme un isotope AZX du carbone : le fameux carbone 14. Immťdiatement formť le carbone 14 s'oxyde en se combinant avec l'oxygŤne pour former du dioxyde de carbone qui se mťlange avec le reste de l'atmosphŤre. Or le carbone 14 est radioactif. La teneur en carbone 14 est constante dans le monde ( dans l'atmosphŤre comme dans chaque organisme vivant ). Cela est du ŗ un ťquilibre entre la dťsintťgration et la production de carbone 14. Chaque gramme de carbone contient des atomes de carbone 14. On enregistre en moyenne 13,5 dťsintťgrations par minute et par gramme de carbone. Lorsqu'un arbre, par exemple, est abattu, le bois cesse de vivre, le processus de photosynthŤse s'arrÍte et il n'y a plus d'absorption de dioxyde de carbone. Le carbone 14 est alors libre de se dťsintťgrer sans compensation. On peut donc dater l'‚ge de la mort de l'organisme ( au moment oý cesse tout ťchange de CO2 avec l'atmosphŤre). Donnťes : 6C ; 7N. Formation du carbone 14 dans la
haute atmosphŤre
: Dans la haute atmosphŤre la rťaction qui a lieu entre le neutron et le noyau d'azote 14 s'ťcrit : 147N + 10n---> AZX + 11p. Vťrifier, en justifiant avec
les lois de conservation, que AZX est
bien du carbone 14.
L'azote 14 147N et le carbone 14 146C ne sont donc pas isotopes. 147N + 10n---> AZX + 11p Conservation de la charge : 7 = 1+Z d'oý Z= 6, ťlťment carbone. Conservation du nombre de
nuclťons : 14+1 = A+1 d'oý A = 14.
L'ťtude de l'ťvolution de la population moyenne d'un ensemble de noyaux radioactifs permet d'ťcrire : DN= - l N Dt oý N est le nombre de noyaux ŗ la date t et DN est la variation du nombre de noyaux pendant la durťe Dt. Cette relation conduit ŗ la loi de dťcroissance radioactive N(t) = N0 exp (-lt), dans laquelle N0 est le nombre de noyaux ŗ la date t=0.
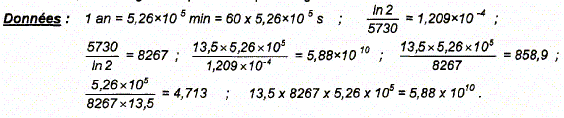
l est la constante radioactive. Dťfinition de la demi-vie ou pťriode du carbone 14 : Durťe au bout de laquelle la
moitiť des noyaux initiaux se sont
dťsintťgrťs. d'oý : 0,5 N0 = N0 exp (-ltĹ) ; 0,5 = exp (-ltĹ) ln 0,5 = -ltĹ ; -ln 2 = - ltĹ ; l
= ln2
/tĹ. ln 2 est sans dimension ; tĹ a la dimension d'un temps donc [ln2 /tĹ] = T-1. La constante radioactive est l'inverse d'un temps. Montrons que l'activitť A ŗ l'instant t et le nombre N de noyaux prťsents dans l'ťchantillon ŗ la date t sont liťs par la relation : A = l N. A = - dN/dt avec N = N0 exp (-lt) dN/dt = -l N0 exp (-lt) = - l N d'oý A = l N. Calcul du nombre N d'atomes de carbone 14 dans 1 g de carbone tel que A= 13,5 dťsintťgrations par minute et par gramme de carbone : N = A/l avec A = 13,5 / 60 Bq. l = ln2 /tĹ ; 1/l = tĹ/ ln2 avec tĹ = 5730 ans = 60*5,26 105 s. N= 13,5 / 60 * 5730*60*5,26 105 / ln 2 = 5730 / ln 2 *13,5*5,26 105 N=8267*13,5*5,26 105 = 5,88 1010.
La loi de dťcroissance radioactive peut ťgalement s'ťcrire en fonction de l'activitť , A(t) =A0 exp (-lt), dans laquelle A0 est l'activitť ŗ la date t=0 et A l'activitť mesurťe ŗ l'instant t. Le prťlŤvement d'une poutre en bois dans une tombe au Sahara fournit une activitť au moment de la mesure telle que A= 6,68 dťsintťgrations par minute et par gramme de carbone alors que A0 = 13,5 dťsintťgrations par minute et par gramme de carbone. Dťmontrer que l'expression qui permet de donner l'‚ge de la mort d'un organisme s'ťcrit : t = tĹ / ln 2 * ln(A0/A) avec tĹ = 5730 ans. Calculer en faisant apparaÓtre l'application numťrique, l'‚ge t de la tombe de ce vizir de la premiŤre dynastie des pharaons.
A(t) /A0 = exp (-lt) ; ln [A(t) /A0 ] = -lt ; ln [A0/A(t) ] =lt ; ln [A0/A(t) ] = t ln2 / tĹ ; t = tĹ / ln 2 * ln(A0/A) t =5730 / ln2 * ln(13,5 / 6,68) = 5816 ans. |
|||
|
|
|||
|
|