On dispose d'un échantillon dont on cherche à connaître la masse d'oxyde de fer III (formule Fe2O3) qu'il contient. Pour cela, on traite l'échantillon par une solution d'acide chlorhydrique concentré ce qui permet de libérer en solution les ions fer III. Dans la solution obtenue précédemment on introduit de la poudre de zinc en excès, jusqu'à obtenir une décoloration de la solution. Les ions Fe III sont transformés en ions Fe II selon la réaction d'équation :
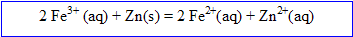
Une solution colorée absorbe des ondes électromagnétiques dans le domaine visible [400 nm ; 800 nm]. En présence d'orthophénanthroline les ions FeII donnent une coloration rouge orangée.
1. L'équation de la réaction donnée ci-avant correspond-elle à une réaction d'oxydoréduction ? A une réaction acide-base ? A un autre type de réaction ? Justifier.
premier couple redox : 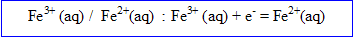 de l'ion fer III
de l'ion fer III
second couple redox : 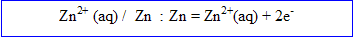 du zinc
du zinc
Donc réaction d'oxydo-réduction.
2. Préparation d'une solution S de concentration C.
On pèse une masse m = 0,20 g de sel de Mohr de formule  , de masse molaire M = 392,1 g/mol que l'on dissout dans une fiole jaugée de 500 mL. On complète avec de l'eau distillée jusqu'au trait de jauge.
, de masse molaire M = 392,1 g/mol que l'on dissout dans une fiole jaugée de 500 mL. On complète avec de l'eau distillée jusqu'au trait de jauge.
- Déterminer la quantité de matière mise en solution.
quantité de matière (mol) = masse (g) par la masse molaire (g/mol)
n= 0,20 / 392,1 = 5,1 10^ -4 mol = mmol.
- Calculer la concentration C de la solution S. En déduire la concentration en ion Fe II.
concentration (mol/L )= quantité de matière (mol) divisée par le volume de la solution (L)
C= 5,1 10^ -4 /0,5 = 1,02 10^-3 mol/L = mmol/L
Au regard de la formue du sel de Mohr la concentration en ion fer II est 1 mmol/L.
3. Préparation d'une gamme de solutions-étalon :
À partir de la solution S de concentration C, on prépare chaque solution étalon en prélevant Vi(mL) de solution S que l'on introduit dans une fiole jaugée de volume V = 50 mL complétée ensuite avec de l'eau distillée jusqu'au trait de jauge. Le contenu de chacune de ces fioles est versé dans une série de béchers numérotés de 1 à 4. Dans chacun des béchers, on introduit un volume Vo = 10 mL d'une solution d'orthophénanthroline et on agite. Chaque mélange prend alors une coloration rouge-orangée, plus ou moins intense, suivant la valeur de la concentration en ion Fe II de la solution.
-Quelle grandeur est conservée au cours d'une dilution ?
La de matière (mol) du soluté est conservée au cours d'une dilution.
- Exprimer la concentration en ions Fe II dans un bécher en fonction de Vi, V, Vo et C.
Quantité de matière (mol) = volume prélevé fois concenbtration de la solution S = Vi C
volume de la solution dans un becher : V+Vo = 50 +10 = 60 mL
concentration en ion fer II dans un bécher : Vi C / (V+Vo)
- Calculer la concentration en ions Fe II dans chaque bécher et compléter le tableau ci-dessous :
4. Utilisation d'une courbe d'étalonnage
On procède à la mesure de l'absorbance A de chaque solution avec le spectrophotomètre réglé à 510 nm (longueur d'onde choisie pour effectuer les mesures). Le graphe ci-dessous représente la courbe d'étalonnage donnant l'absorbance A en fonction de la concentration soit A = f[Fe II].
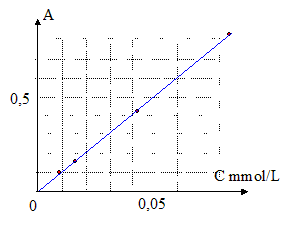
- Quelle relation littérale lie les grandeurs A et [Fe II] ?
L'absorbance et la concentration en ion Fe II sont
.
- Calculer la valeur du coefficient directeur de la droite en donnant son unité.
0,8 / 0,08 = 100 L / mmol.
5. Détermination de la concentration en ion Fe II de la solution Sx.
Sur le volume initial de 200 mL de la solution Sx, on effectue un prélèvement de 50 mL et on y introduit 10 mL de la solution d'orthophénanthroline. On mesure l'absorbance A de ce nouveau mélange dans les mêmes conditions que précédemment. La valeur obtenue pour A est 0,6.
- Pourquoi faut-il respecter les volumes proposés (50 mL de Sx et 10 mL de solution d'orthophénanthroline) ?
Pour utiliser la courbe d'étalonnage précédente il faut se trouver dans les mêmes conditions exprérimentales de préparation des solutions contenues dans les bechers ( même facteur de dilution)
- Déterminer à partir de la courbe la concentration des ions Fe II présents dans Sx.
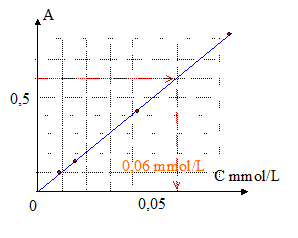
- Calculer la quantité de matière en ions Fe II présents dans Sx et la quantité d'oxyde de fer Fe2O3. En déduire la masse d'oxyde de fer contenu dans l'échantillon.
Données :
Masse molaire atomique du fer M(Fe) = 56 g/mol
Masse molaire atomique de l'oxygène M(O) = 16 g/mol
- quantité de matière (mmol) en ions Fe II présents dans Sx : concentration (mmol/L)
volume (L) = 0,06*0,2 = 0,012 mmol
donc 0,012 / 2 = 0,006 mmol Fe2O3.
- masse molaire Fe2O3 : 56*2 +3*16 = 160 g/mol
- masse (mg) d'oxyde de fer : masse molaire (g/mol)
quantité de matière (mmol) = 160*0,006 = 0,96 mg.