|
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
||||||||||||||||||||||||
| .
. |
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|
|
corrigť H2O2 = H2O +Ĺ O2(g) concentration d'une solution de peroxyde d'hydrogŤne ŗ 130 volumes : quantitť de matiŤre O2(mol) = volume (L) / volume molaire (L/mol) = 130/22,4 =5,8 mol d'aprŤs les coefficients de l'ťquation ci-dessus, la quantitť de matiŤre (mol) de peroxyde d'hydrogŤne est ťgale ŗ deux fois celle de dioxygŤne : 5,8*2 = 11,6 mol dans 1 L. autre mťthode : masse de peroxyde d'hydrogŤne pur dans 1 L : 1,13*1000*0,33 = 372,9 g Qtť de matiŤre (mol) = masse (g) / masse molaire (g/mol) = 372,9 / 34,01 = 10,96 mol dans 1 L ťcart relatif voisin de 6% : rťsultats identiques ŗ 6% prŤs. L'eau oxygťnťe en vente en pharmacie est une solution ŗ 6% et de densitť 1,02 : n(H2O2) = 1020*0,06 / 34,01 = 1,8 mol dans 1L d'aprŤs les coefficients de l'ťquation ci-dessus n(O2 ) =Ĺ n(H2O2) = 0,9 mol volume (L) = Qtť de matiŤre (mol) * volume molaire (L/mol) = 0,9*22,4 = 20 volumes.
|
|||||||||||||||||||||||
conservation de l'ťlťment carbone : [CH3COOH] +[CH3COO-]=C0d'oý [CH3COOH] =C0(1-a) Ka = (a C0)≤ / (C0(1-a)) = C0a≤/(1-a) Calcul de a si C0 = 0,1 mol/L : pKa = 4,75 soit Ka =1,78 10-5 ; 1,78 10-5(1-a) = 0,1a≤. 0,1a≤+1,78 10-5a -1,78 10-5 = 0 ; la rťsolution donne a = 1,32 10-2. volume d'eau faut ŗ ajouter ŗ 1 L de solution aqueuse d'acide ťthanoÔque pour que a double : Ka = C0a≤/(1-a) = C(2a)≤/(1-2a) soit C0(1-2a) = 4C (1-a) ; C= C0(1-2a)/(4(1-a)) = 0,1*0,9736/(4*0,9868) = 2,446 10-2 mol/L facteur de dilution : f = C0/C = 0,1/ 2,446 10-2 = 4,05 f = volume total / volume solution mŤre soit volume total = 4,05*1 = 4,05 L ; il faut ajouter 3,05 L d'eau ŗ 1L de la solution mŤre de concentration C0. volume d'acide ťthanoÔque pur ŗ ajouter ŗ 1 L de solution aqueuse d'acide ťthanoÔque pour que a soit divisť par 2 : ( mÍme mťthode) Ka = C0a≤/(1-a) = C'(0,5a)≤/(1-0,5a) soit C0(1-0,5a) = 0,25C' (1-a) ; C'= C0(1-0,5a)/(0,25(1-a)) = 0,4*0,9934/0,9868 =0,403 mol/L soit 0,403 mol d'acide dans 1 L : il a fallu ajouter 0,403-0,1 = 0,303 mol d'acide pur. soit en masse m 0,303*60,05 = 18,2 g ou encore 18,2 / d= 18,2/1,05 = 17,3 mL.
|
||||||||||||||||||||||||
corrigť le cuivre n'est pas attaquť par les ions oxonium : le rťsidu est du cuivre ( 3,2 g) On note mZn, la masse de zinc et mAl la masse d'aluminium : mZn + mAl = 14,1-3,2 = 10,9 (1) Qtť de matiŤre (mol) : nZn = mZn/ 65,39 ; nAl = mAl/ 26,98 ; (1) s'ťcrit : 65,39 nZn + 26,98 nAl =10,9 (1' ) Zn + 2 H+ = Zn2+ + H2(g) ; n(H2)1 = nZn. Al+ 3 H+ = Al3+ + 1,5 H2(g) ; n(H2)2 =1,5 nAl Qtť de matiŤre totale H2 : nZn + 1,5 nAl = 6,8 / 22,4 = 0,304 (2) (2) donne nZn = 0,304- 1,5 nAl ; repport dans (1') : 65,39(0,304- 1,5 nAl ) + 26,98 nAl =10,9 d'oý : nAl =0,126 mol soit 0,126*26,98 = 3,41 g et nZn =0,115 mol soit 0,115*65,4 = 7,49 g.
2Fe3+
+Fe = 3Fe2+
si Fe3+en dťfaut 0,05-2xmax = 0 soit xmax =2,5 10-2 mol (retenir la plus petite valeur) [Fe3+]= 2,85 10-2 / 0,5 = 5,7 10-2 mol/L ; [Fe2+] = 6,44 10-2 mol/L masse minimale de poudre de fer ŗ ajouter pour qu'il n'y ait plus d'ion Fe3+ : 0,05-2xmax =0 soit xmax = 0,025 mol n( Fe) = 0,025 mol soit en masse 0,025*55,85 = 1,4 g.
|
||||||||||||||||||||||||
corrigť pH d'une solution d'acide chlorhydrique HCl : pH= - log C = -log 3 10-4 = 3,5 Quant ŗ la solution ŗ 10-7 mol/L, il s'agit d'eau pure et non une solution acide ou de soude. ( pH=7) pH d'une solution de soude : pH= 14 + log C = 14 + log 3 10-4 =10,5. pH d'une solution d'acide fluorrhydrique HF ŗ 0,1 mol/L : pH= Ĺ(pKa-log C) = 0,5(3,2+1) = 2,1.
|
||||||||||||||||||||||||
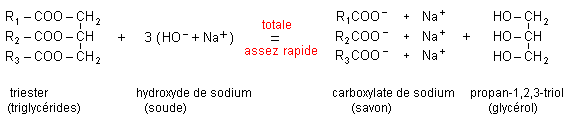
corrigť huile : matiŤres grasses ŗ l'ťtat liquide ŗ tempťrature ambiante, non miscibles ŗ l'eau. graisse : lubrifiant composť d'une ou de plusieurs huiles , corps gras, mťlange d'huiles. Un corps gras renferme une ou plusieurs fonctions ester. un acide gras est un acide carboxylique possťdant une longue chaine carbonťe hydrophobe, saturťe ou insaturťe. un savon ( ou carboxylate de sodium ou de potassium) est une substance solide utilisťe le lavage ou le nettoyage. rťaction de formation du savon ŗ partir d'un corps gras : saponification.
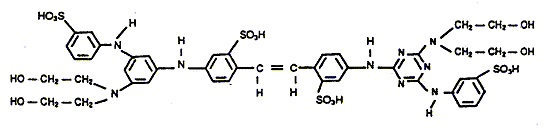
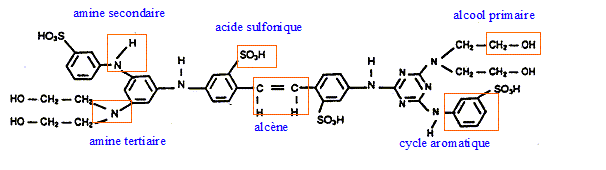
principales fonctions de la chimie organique prťsentes dans la formule du produit suivant :
|
||||||||||||||||||||||||
|
|
||||||||||||||||||||||||
|
La rťaction de l'ammoniac en excŤs sur un hydrocarbure saturť acyclique bromť A conduit ŗ la formation d'une amine B, suivant une rťaction de substitution ťlectrophile. Dans B, le pourcentage massique en azote est ťgal ŗ 1,27 fois le pourcentage massique en hydrogŤne.
corrigť formule brute de B : CnH2n+3 N ; masse molaire de B : M= 12n+2n+3+14 = 14 n+17 g/mol on note :%H = x d'oý : %N = 1,27 x et %C = 100-2,27x. puis 12 n / (100-2,27x) =(2n+3)/x = 14/(1,27x) = (14n+17)/100 14/(1,27x) =11/x ; (2n+3)/x = 11/x soit 2n+3=11 ; n= 4 ; C4H11N. nom et la formule semi-dťveloppťe de B sachant que la chaine hydrocarbonťe est linťaire : CH3-CH2-CH2-CH2-NH2 butylamine ( amine primaire) formule semi-dťveloppťe et le nom des diverses amines isomŤres, de classe diffťrente : CH3-CH2-CHNH2-CH3 1-mťthylpropylamine ( amine primaire) CH3-CH2-CH2-NH-CH3 ( amine secondaire) N-mťthylpropylamine CH3-CH2-N(CH3)2 ( amine tertiaire) N,N- dimťthylťthylamine. formule brute, le nom et la formule semi-dťveloppťe de A : C4H9Br. CH3-CH2-CH2-CH2-Br : 1-bromobutane.
|
||||||||||||||||||||||||
|
|
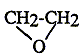 acťtone
; ether ťthylique ; oxyde
d'ťthylŤne ; ťthanol.
acťtone
; ether ťthylique ; oxyde
d'ťthylŤne ; ťthanol.