|
Le piŤge photo, conservateur et parfum , production d'ťnergie nuclťaire d'aprŤs bac S USA 2006 En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
|||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
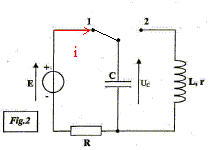
Cet exercice ťtudie le principe de fonctionnement d'un piŤge photo rťalisť par un ornithologue afin d'identifier le prťdateur d'une espŤce d'oiseau en voie de disparition. Un œuf de caille posť sur un commutateur ŗ bascule sert d'app‚t dans un vieux nid. Lorsque le prťdateur prťlŤve l'œuf, le commutateur bascule de la position 0 ŗ la position 2. Le condensateur initialement chargť se dťcharge dans un ťlectroaimant que l'on peut modťliser par une bobine d'inductance L et de rťsistance interne r. L'ťlectroaimant, placť sur un appareil photo dťclenche la prise de vue. Le circuit de charge est constituť d'un condensateur de capacitť C, d'un conducteur ohmique de rťsistance R et d'un gťnťrateur idťal de tension de fem E= 8 V. 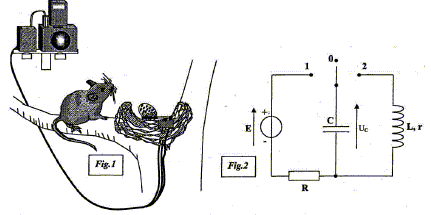 I- Armement du dispositif. Le dispositif s'arme en plaÁant le commutateur en position 1 pendant la durťe nťcessaire ŗ la charge du condensateur. Cette opťration rťalisť, l'œuf est dťposť sur le bras du commutateur ŗ bascule qui est ainsi maintenu en position O.
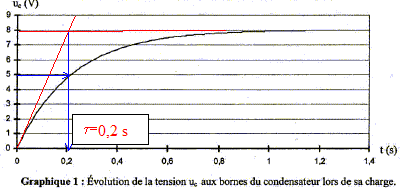
Dťclenchement du piŤge Lorsque l'œuf est prťlevť, le commutateur bascule de la position 0 ŗ la position 2. Un enregistrement de la tension uc(t) aux bornes du condensateur est rťalisť lors de l'ťtude de ce dispositif.
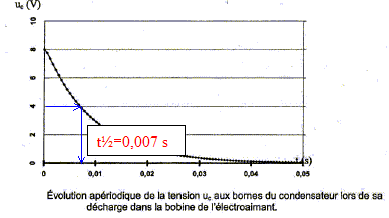
Dťtermination de l'inductance L de la bobine constituant l'ťlectroaimant. On place cette bobine en sťrie avec un condensateur de capacitť C'= 10 nF initialement chargť sous une tension de 6V et une rťsistance R' tel que R'+r= 50 ohms. Le circuit ainsi constituť est reprťsentť ci-dessous : 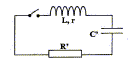 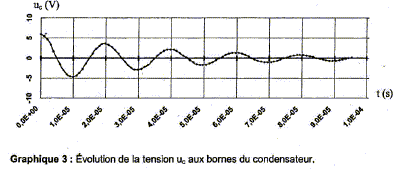 L'ťvolution de la tension aux bornes du condensateur a ťtť enregistrťe ŗ la fermeture de l'interrupteur.
corrigť sens rťel du courant i lors de la charge :
ťquation diffťrentielle vťrifiťe par uc(t) lors de la charge : uc+Ri =E (1) (loi d'additivitť des tensions) de plus i = dq/dt et q=Cuc soit i = Cduc/dt ; repport dans (1) d'oý : uc+RCduc/dt = E On pose t = RC ; par suite : uc+t duc/dt = E analyse dimensionnelle : R rťsistance soit tension / intensitť ; C capacitť soit charge / tension d'oý on dťduit : RC charge / intensitť or une charge est une intensitť fois un temps ; par suite RC a la dimension d'un temps. valeur de uc(t) en rťgime permanent : en rťgime permanent uc(t) est constant : donc duc/dt = 0 ; uc+t duc/dt = E s'ťcrit : Uc=E. solution de l'ťquation diffťrentielle : uc(t) = A(1-exp(-t/t)) ; dťriver par raport au temps ; duc/dt = A/t exp(-t/t) repport dans l'ťquation diffťrentielle : A(1-exp(-t/t)) + A exp(-t/t) = E A- A exp(-t/t)+ A exp(-t/t) = E uc(t) = A(1-exp(-t/t)) est solution de l'ťquation diffťrentielle si A= E. tension aux bornes du condensateur ŗ t=5t : uc(5t) = E(1-exp(-5t/t)) =E(1-exp(-5)) = 0,993 E ŗ 0,7 % prŤs on peut considťrer que la charge du condensateur est terminťe. valeur de t :
abscisse de l'intersection de la tangente ŗ t=0 avec l'asymptote horizontale ou bien abscisse correspondant ŗ uc= 0,63 E= 0,63*8 = 5 V. La charge du condensateur est pratiquement terminťe ŗ t = 5 t soit 1 s. Durťe caractťristique : ŗ tĹ uc = ĹE = 4 V
L'ťnergie initialement stockťe dans le condensateur doit Ítre la plus grande possible : E =ĹCE≤ en fin de charge Cette ťnergie sera d'autant plus grande que E sera plus grand et que la capacitť C sera plus grande. 
Nom du rťgime correspondant au graphe ci-dessus : rťgime pseudo-pťriodique. Inductance de la bobine : pseudo-pťriode T= 2,0 10-5 s (lecture graphe) de plus T= 2p(LC)Ĺ ; T≤ = 4p≤ LC soit L= T≤/(4p≤ C) avec C= 10-8F. L= 4 10-10/(4*3,14≤ 10-8)= 1,0 10-3 H.
|
||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||
|
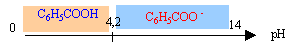
Propriťtťs de l'acide benzoÔque Les conservateurs sont des substances qui prolongent la durťe de conservation des denrťes alimentaires en les protťgeant des altťrations des micro-organismes. L'acide benzoÔque C6H5-COOH ( code E210) et le benzoate de sodium C6H5-COONa ( code E211) sont utilisťs dans l'industrie comme conservateurs alimentaires pour leurs propriťtťs fongicides et antibactťriennes. Acide benzoÔque : solide blanc, masse molaire M= 122 g/mol, solubilitť dans l'eau ( masse maximale que l'on peut dissoudre dans 1 L d'eau) : 2,4 g/L ŗ 25įC. Couple acide base C6H5-COOH / C6H5-COO- pKa1 = 4,2 Rťaction de l'acide benzoÔque avec l'eau : On introduit une masse m0 d'acide benzoÔque dans un volume V0= 100 mL d'eau distillťe. AprŤs dissolution totale, on obtient une solution aqueuse d'acide benzoÔque notťe S0 de concentration C0 = 1,0 10-2 mol/L. Le pH-mŤtre indique 3,1 pour le pH de la solution S0.
Rťaction de l'acide benzoÔque avec la soude. On ajoute ŗ la solution S0 quelques gouttes de soude ( hydroxyde de sodium). Le pH-mŤtre indique alors 6,2.
SynthŤse du benzoate de mťthyle. On le prťpare ŗ partir de la rťaction entre l'acide benzoÔque et le mťthanol de formule CH3OH. On mťlange une masse m1 = 12,2 g d'acide benzoÔque avec un volume V2 = 30 mL de mťthanol, quelques gouttes d'une solution concentrťe d'acide sulfurique et quelques grains de pierre ponce. On chauffe ŗ reflux pendant 60 minutes. AprŤs refroidissement, on verse le contenu du ballon dans une ampoule ŗ dťcanter contenant de l'eau glacťe. On obtient deux phases bien distinctes. AprŤs traitement de la phase contenant l'ester , on isole une masse ťgale ŗ 9,52 g de benzoate de mťthyle.
corrigť masse m0 ŗ peser pour prťparer S0 : quantitť de matiŤre (mol) = concentration (mol/L) * volume de la solution (L) = C0V0 = 0,01*0,1 = 1,0 10-3 mol masse (g) = quantitť de matiŤre (mol) * masse molaire (g/mol) = 10-3*122 = 0,12 g. 0,12 g dans 0,1 L soit 1,2 g/L, valeur infťrieure ŗ la solubilitť dans l'eau ŗ 25įC : la solution n'est pas saturťe. Equation de la rťaction de l'acide benzoÔque avec l'eau : C6H5COOH + H2O = C6H5COO- + H3O+. ŗ pH infťrieur ŗ pKa la forme acide AH prťdomine; ŗ pH supťrieur ŗ pKa la forme base conjuguťe A- prťdomine; ŗ pH=pKa les forme acide et base conjuguťe sont en quantitťs ťgales.
Dans S0 ( pH=3,1, infťrieur au pKa) la forme acide C6H5COOH du couple acide base prťdomine. Tableau
d'avancement :
en grand excŤs taux d'avancement final t = xťq / xmax avec xťq = [H3O+]V0 ; t =[H3O+] / C0 = 10-3,1 / 10-2 = 10-1,1 = 7,9 10-2. La rťaction de l'acide benzoÔque avec l'eau est limitťe ; la forme acide prťdomine ( en accord avec la question prťcťdente) Expreesion du quotient de rťaction ŗ l'ťtat d'ťquilibre : Qr ťq = Ka = [C6H5COO-]ťq[ H3O+ ] ťq / [C6H5COOH]ťq La solution est ťlectriquement neutre ( HO- minoritaire ŗ pH = 3,1) : [C6H5COO-]ťq=[ H3O+ ] ťq conservation de l'ťlťment carbone : [C6H5COOH]ťq +[C6H5COO-]ťq= C0. [C6H5COOH]ťq = C0-[C6H5COO-]ťq. Qr ťq =[ H3O+ ]≤ ťq / (C0-[ H3O+ ] ťq ) = 10-6,2 / (0,01-10-3,1) =6,8 10-5. pKa du couple ( acide benzoÔque/ ion benzoate) : Qr ťq = Ka ; pKa
= -log Ka = - log6,8 10-5
= 4,2.
pH=6,2 , valeur bien supťrieure ŗ pKa ( 4,2) : l'ion benzoate C6H5COO- prťdomine. Equation de la rťaction entre l'acide benzoÔque et la soude : C6H5COOH + HO- =C6H5COO- + H2O constante d'ťquilibre K= [C6H5COO-]/([C6H5COOH][HO-]) (1) or Ka = [C6H5COO-][ H3O+ ] / [C6H5COOH] soit[C6H5COO-] / [C6H5COOH] = Ka / [ H3O+ ] repport
dans (1) : K =Ka / ([ H3O+
] [HO-]) =Ka
/Ke = 10-4,2
/ 10-14 = 109,8 =6,3 109.
n1 =m1/M( acide benzoÔque) = 12,2 / 122 = 0,10 mol masse mťthanol (g = volume (mL) * masse volumique (g/mL) = 30 *0,8 = 24 g ; pui diviser par la masse molaire du mťthanol : n2 = 24/32 = 0,75 mol. facteurs cinťtiques : concentration d'un rťactif : le mťthanol est en large excŤs ; tempťrature : chauffage ŗ reflux ŗ tempťrature modťrťe ; catalyseur : rŰle jouť par l'acide sulfurique. utilitť du chauffage ŗ reflux : accťlŤre la rťaction en permettant de travailler ŗ tempťrature modťrťe ; ťvite les pertes de matiŤre : les vapeurs se condensent dans le rťfrigťrant et retombent dans le ballon. Equation de la rťaction de synthŤse du benzoate de mťthyle : C6H5COOH + CH3OH =C6H5COO-CH3 + H2O. ŗ partir de 0,1 mol d'acide on peut consommer au plus 0,1 mol de mťthanol ; or on dispose de 0,75 mol de mťthanol : ce dernier est en excŤs et l'acide benzoÔque constitue le rťactif limitant. En consťquence on obtiendra au plus 0,1 mol de benzoate de mťthyle. rendement : Qtť rťellement obtenue / Qtť thťorique Qtť rťelle (mol) = masse (g) / masse molaire ester (g/mol ) = 9,52 / 136=7,0 10-2 mol. rendement : 0,07/0,1 = 0,70 (70%) |
|||||||||||||||||||||||||||||||||||||||||||
|
Fission nuclťaire : Une centrale nuclťaire est une usine de production d'ťlectricitť. Actuellement ces centrales utilisent la chaleur produite par des rťactions de fission de l'uranium 235 qui constitue le " combustible nuclťaire ". Cette chaleur transforme de l'eau en vapeur. La pression de la vapeur permet de faire tourner ŗ grande vitesse une turbine qui entraÓne un alternateur produisant de l'ťlectricitť. Certains produits de fission sont des noyaux radioactifs de forte activitť et dont la demi-vie peut Ítre trŤs longue.
Fusion nuclťaire : Le projet ITER s'installera prochainement sur le site de Cadarache en France. L'objectif de ce projet est de dťmontrer la possibilitť scientifique et technologique de la production d'ťnergie par fusion des atomes. La fusion est la source d'ťnergie du soleil et des autres ťtoiles. Pour obtenir une rťaction de fusion il faut rapprocher suffisamment deux noyaux qui se repoussent, puisqu'ils sont tous deux chargťs positivement. Une certaine ťnergie est donc indispensable pour franchir cette barriŤre et d'arriver dans la zone trŤs proche du noyau, oý se manifestent les forces nuclťaires capables de l'emporter sur la rťpulsion ťlectrostatique. La rťaction de fusion la plus accessible est la rťaction impliquant le deutťrium et le tritium. La demi-vie du tritium consommť au cours de cette rťaction n'est que de 15 ans. De plus il y a peu de dťchets radioactifs gťnťrťs par la fusion et l'essentiel est retenu dans les structures de l'installation ; 90% d'entre eux sont de faible ou moyenne activitť.
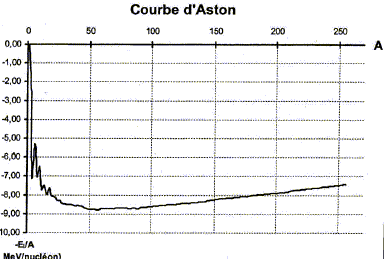
corrigť demi-vie : durťe au bout de laquelle la moitiť des noyaux initiaux se sont dťsintťgrťs. activitť : nombre moyen de dťsintťgrations par seconde ( unitť : bequerel (Bq)) valeurs de A et Z : 23592U + 01n--->94ZSr+ A54Xe + 3 01n conservation de la charge : 92 = Z+54 d'oý Z= 92-54 = 38 conservation du nombre de nuclťons : 235+1=94+A+3 soit A = 139. ťnergie libťrťe par cette rťaction de fission : Dm = 2 m( 01n) + m(A54Xe)+m(94ZSr)- m(23592U) = 2*1,00866+138,8892+93,8945-234,9942 =-0,19318 u soit 0,19318 * 931,5 = 180 MeV ťnergie libťrťe par nuclťon de matiŤre : 180/236 = 0,762 MeV/nuclťon. isotopes : deux noyaux qui ne diffŤrent que par leur nombre de neutrons ; ils ont le mÍme nombre de charge Z le noyau de deutťrium D contient 1 proton et 1 neutron : 21H ; le noyau de tritium T contient 1 proton et 2 neutrons : 31H. D et T sont des isotopes de l'ťlťment chimique hydrogŤne. rťaction de fusion : rťaction au cours de laquelle deux noyaux lťgers s'unissent pour former un noyau plus lourd. La rťaction se fait avec perte de masse et dťgagement d'ťnergie. courbe d'Aston : Le noyau de fer est le plus stable ; les gros noyaux ( uranium 235) situťs sur la partie droite sont instables et conduisent par des rťactions de fission ŗ d'autres noyaux plus stables ; les petits noyaux instables ( deutťrium, tritium), situťs sur la partie gauche, conduisent par des rťactions de fusion ŗ des noyaux plus gros et plus stables. Equation de la rťaction nuclťaire entre un noyau de Deutťrium et un noyaude Tritium au cours de laquelle se forme un noyau d'hťlium 42He : 31H +21H --> 42He + 10n ťnergie DE qui peut Ítre libťrťe par cette rťaction : |Dm |= | m(42He)+m(10n)- m(31H) - m(21H)|=|4,0015+1,00866-2,01355-3,0155|= 1,89 10-2 u puis 1,89 10-2*931,5= 17,6 MeV. ťnergie libťrťe par nuclťon : 17,6 / 5 = 3,52 MeV/nuclťon. avantages de la fusion par rapport ŗ la fission : l'ťnergie libťrťe par nuclťon est plus importante ; Deutťrium abondant et bon marchť ; Tritium assez facile ŗ produire ; dťchets radioactifs moins importants et absence de nuclťides conduisant ŗ la prolifťration des armes nuclťaires.
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||
|
|