|
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
|||
|
|||
|
|
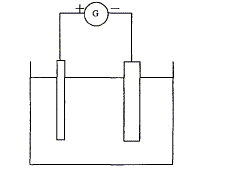
La purification des mťtaux par ťlectrolyse est possible gr‚ce ŗ l'emploi d'une anode soluble. Le mťtal impur constitue l'anode : ce mťtal subit une oxydation et passe ŗ l'ťtat d'ion en solution. Les impuretťs libťrťes tombent au fond de l'ťlectrolyseur ou restent en suspension dans la solution. A la cathode les ions cuivre II en solution subissent une rťduction, le mťtal trŤs pur se dťpose. La solution ťlectrolytique contient des ions cuivre II Cu2+(aq), des ions sulfate et de l'acide sulfurique. Partie 1 :
Partie 2 : A l'aide du montage dťcrit dans la patie 1, on dťsire dťposer par ťlectrolyse une couche de cuivre sur une plaque d'acier. Lors de l'ťectrolyse d'une durťe Dt= 30,0 min, l'intensitť du courant est constante et vaut I= 400 mA. M(Cu) = 63,5 g/mol ; NA=6,02 1023 mol-1 ; e= 1,60 10-19 C.
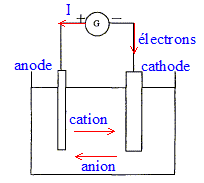
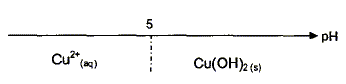
L'ťlectrolyse est une rťaction d'oxydorťduction forcťe ; elle nťcessite un apport d'ťnergie sous forme d'ťnergie ťlectrique. ťquations des transformations aux ťlectrodes : anode positive ( oxydation) : Cu (s) = Cu2+ + 2e-. cathode nťgative ( rťduction) : Cu2+ + 2e- = Cu(s) bilan : Cu (s) + Cu2+ = Cu(s) + Cu2+ . anode soluble : le cuivre de l'ťlectrode s'oxyde en ion Cu2+(aq) ; le mťtal de l'anode disparaÓt. Evolution de la concentration de la solution en ion Cu2+ : lorsqu'un ion cuivre II est rťduit ŗ la cathode, un ion cuivre II apparaÓt lors de l'oxydation ŗ l'anode : en consťquence la concentration en ion cuivre II ne change pas. rŰle de l'acide sulfurique : ŗ pH supťrieur ŗ 5, on observe la prťcipitation de Cu(OH)2 ; le milieu doit avoir un pH infťrieur ŗ 5 : c'est le rŰle de l'acide sulfurique ( d'autre part l'ion sulfate reste spectateur) la plaque d'acier doit se recouvrir de mťtal cuivre : elle joue le rŰle de cathode ; sur cette plaque d'acier les ions cuivre II sont rťduits en cuivre. Quantitť d'ťlectricitť ( C) notťe Q : intensitť ( A) fois durťe ( seconde) Q= I Dt De plus Q= ne NAe avec ne quantitť de matiŤre (mol) d'ťlectron et e : charge ťlťmentaire ou NAe = 1 faraday : en valeur absolue, charge d'une mole d'ťlectrons. or ŗ la cathode : Cu2+ + 2e- = Cu(s) d'oý ne = 2 nCu. par suite : nCu = Ĺne=ĹIt / ( NAe ) masse de cuivre dťposťe sur l'acier : quantitť de matiŤre (mol) de cuivre * masse molaire (g/mol) mCu=nCu M(Cu) = ĹneM(Cu) = ĹIt M(Cu) / ( NAe ) mCu=0,5*0,4*30*60*63,5 / (6,02 1023*1,60 10-19) = 2,37 10-1 g. explication de la variation de masse de la lame de cuivre |Dm|=2,41 10-1 g : Explication nį1 : dans la rťalitť, ŗ la cathode d'autres espŤces prťsentes ( H2O, ion oxonium) peuvent Ítre rťduites et concurence un peu la rťduction des ions cuivre II. Explication nį2 : l'anode ťtant constituťe de cuivre impur, une partie de ces impuretťs se retouvent soit au fond de la cuve, soit dans la solution. En consťquence la masse de cuivre dťposťe est infťrieure ŗ la diminution de masse de l'anode.
|
||
|
|