|
Teneur en CO2 d'un vin d'apr×s bac S Liban 2006 En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitÚs adaptÚs Ó vos centres d’intÚrÛts. |
|||||||||||||||||
|
|||||||||||||||||
|
|
Le vin est obtenu par fermentation du jus de raisin. Lors de la fermentation alcoolique, le glucose prÚsent dans le raisin est dÚgradÚ en Úthanol et en dioxyde de carbone CO2. Lorsque la vinification est terminÚe, on dÚc×le gÚnÚralement dans le vin la prÚsence de CO2 Ó raison de 200 Ó 700 mg par litre. Pour dÚterminer la concentration en CO2 d'un vin, les laboratoires d'œnologie analysent, par spectrophotomÚtrie, les Úchantillons que leur fournissent les viticulteurs. A l'aide d'un spectrophotom×tre, l'absorbance de cet Úchantillon est mesurÚe pour une gamme de longueurs d'onde donnÚes (situÚes de part et d'autre du maximum d'absorption d¹ Ó la prÚsence de CO2). Ces mesures sont ensuite reportÚes sur un graphe constituant le spectre d'absorption de l'Úchantillon pour la gamme de longueurs d'onde choisie. Dans tout cet exercice on consid×rera que dans la gamme de longueurs d'onde choisies, seul le CO2 absorbe. Un Úl×ve cherche Ó dÚterminer la concentration en CO2 d'un Úchantillon de vin. Il dispose pour cela de quatre autres Úchantillons de vin de concentration en CO2 connues : ╔chantillon n░1 C1 = 4,5 mmol.L-1 ╔chantillon n░2 C2 = 10,4 mmol.L-1 ╔chantillon n░3 C3 = 24,3 mmol.L-1 ╔chantillon n░4 C4 = 29,5 mmol.L-1 ╔chantillon n░5 C5 Ó dÚterminer
Il rÚalise le spectre d'absorption de chacun de ces Úchantillons et obtient le graphe de l'absorbance en fonction de l'inverse de la longueur d'onde (le nombre d'onde 1/l) donnÚ ci-dessous : 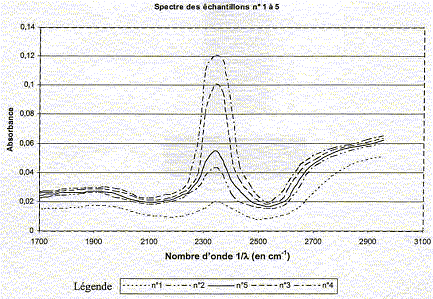
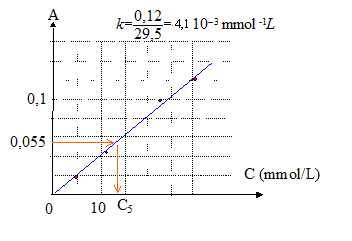
valeur de l'absorbance pour le maximum d'absorption de chaque Úchantillon :
allure de la courbe tracÚe : la courbe est une droite passant par l'origine : donc absorbance et concentration en CO2 sont proportionnelles La courbe obtenue est en accord avec la loi de Beer-Lambert valeur du coefficient e, en unitÚs SI : k = 4,1 10-3 mmol-1 L soit k = 4,1 10-3 mol -1 m3. de plus k = eL soit e = k/L =4,1 10-3/3,5 10-3 =1,2 m▓ mol-1. concentration en CO2 de l'Úchantillon inconnu n░5 : A=kC soit C= A/k = 0,055/4,1 10-3 =13,4 mmol/L masse molaire CO2 : M= 44 g/mol puis 44*13,4 = 590 mg/L, valeur comprise entre 200 et 700 mg/L : le vin contenu dans cet Úchantillon entre dans la catÚgorie des vins citÚs dans le texte. |
||||||||||||||||
| |
|||||||||||||||||
|
|