|
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
|
On se propose de dťterminer les masses en ions chlorure et en acide lactique prťsents dans un lait. I- Dosage par conductimťtrie :
II- Dosage de l'acide lactique : Un lait frais ne contient pas d'acide lactique. En vieillissant, le lactose prťsent dans le lait se transforme en acide lactique, notť par la suite HA. On dose l'acide lactique, considťrť comme le seul acide prťsent dans le lait ťtudiť, par une solution d'hydroxyde de sodium : Na+(aq) + HO-(aq) (soude) de concentration CB = 5,00 10-2 mol.L-1. On prťlŤve un volume VA = 20,0 mL de lait que l'on place dans un bťcher et on suit l'ťvolution du pH en fonction du volume VB de soude versť.
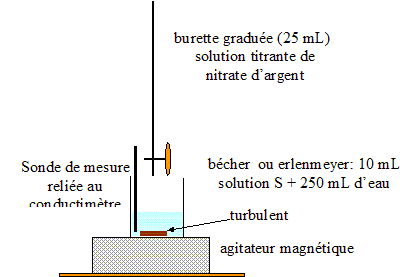
Dosage par conductimťtrie : On prťlŤve un volume V0 = 20,0 mL de lait (solution S0) et on les introduit dans une fiole jaugťe de volume VS = 100,0 mL : le facteur de dilution F est ťgal ŗ : F= VS /V0 = 100/20 = 5. De plus F= C0 /CS d'oý : C0 =5CS. prťlever V1 = 10,0 mL de la solution S : verser un peu de solution S dans un bťcher, prendre une pipette jaugťe de 10,0 mL ( rincťe avec la solution S) surmontťe d'un pipeteur ; utiliser un autre bťcher pour placer ce prťlevement. schťma annotť du dispositif expťrimental de suivi conductimťtrique :
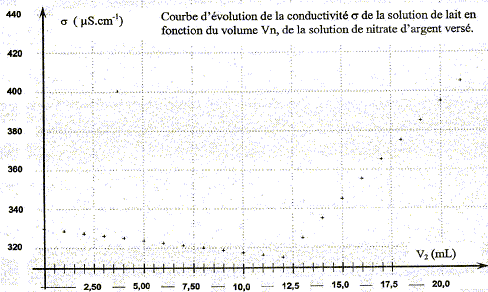
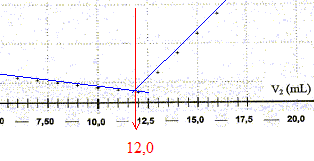
La conductivitť initiale de la solution est due ŗ tous les ions qu'elle contient et en particulier ŗ l'ion chlorure. variation de la valeur de la conductivitť s du milieu rťactionnel au cours du dosage : avant l'ťquivalence, les ions chlorure sont en excŤs, les ions argent ajoutťs sont tous consommťs ; on ajoute des ions nitrate d'oý l'expression de la conductivitť s du milieu rťactionnel : s = lCl- [Cl-] + lNO3- [NO3-]. Du point de vue de la conductivitť, tout se passe comme si on remplaÁait les ions chlorure par les ions nitrate ; de plus le volume de la solution est ŗ peu prŤs constant : or lNO3- <lCl- , en consťquence la conductivitť va diminuer. aprŤs l'ťquivalence, les ions chlorure ont disparu, les ions argent ajoutťs ne sont plus consommťs ; on ajoute des ions nitrate d'oý l'expression de la conductivitť s du milieu rťactionnel : s = lAg+ [Ag+] + lNO3- [NO3-]. Les concentrations de ces deux ions croissent et en consťquence la conductivitť va augmenter. L'abscisse du point particulier, intersection des deux segments de droites, apparaissant sur la courbe s = f(V2) , donne le volume de solution titrante ajoutť ŗ l'ťquivalence. V2E =12,0 mL
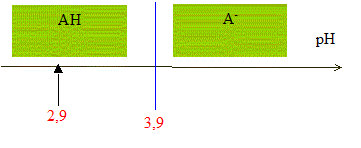
D'aprŤs les coefficients stoechiomťtriques de l'ťquation de rťaction : Ag+(aq) +Cl-(aq) = AgCl(s), ŗ l'ťquivalence la quantitť de matiŤre en ions argent introduits est ťgale ŗ la quantitť de matiŤre en ions chlorure initialement prťsents. C2V2E =V1CS d'oý CS =C2V2E /V1 = 5,00 10-3 * 12,0 / 10,0 = 6,00 10-3 mol/L en tenant compte de la dilution, C0 = 5 CS =3,00 10-2 mol/L. Masse d'ions chlorure prťsents dans 1 L de lait ťtudiť : CS *M(Cl-) = 3,00 10-2 *35,5 =1,07 g/L. La masse d'ions chlorure prťsents dans un litre de lait doit Ítre comprise entre 1,0 g et 2,0 g : ce lait correspond donc ŗ cette norme. Dosage de l'acide lactique : Equation de la rťaction qui se produit lors du mťlange : HA + HO- = A- + H2O Une rťaction adaptťe ŗ un dosage doit Ítre totale et rapide. Expression de la constante de rťaction K correspondante : K= [A- ]/([HA][HO- ]) ( 1) de plus AH + H2O = A- + H3O+ avec Ka3 = [A- ][H3O+]/[AH] soit [A- ] / [AH] = Ka3 /[H3O+] repport dans (1) : K=Ka3 /([H3O+][HO- ]) = Ka3 / Ka1 = 10-3,9 / 10-14 = 1010,1. Je conclus : K ťtant trŤs grand, [HA]ťq , figurant au dťnominateur dans l'expression de K, est trŤs faible : la rťaction est donc bien totale. Utiliser un diagramme de prťdominance :
pH dťbut < pKa3 donc l'espŤce chimique prťdominante au dťbut du dosage est AH. HA(aq) et A-(aq) sont prťsents en quantitťs ťgales lorsque pH = pKa3 c'est ŗ dire ŗ la demi-ťquivalence de ce dosage ( V=ĹVB= 6 mL) quantitť de matiŤre d'acide lactique prťsente dans le volume VA de lait : ŗ l'ťquivalence, les quantitťs de matiŤre de rťactifs mis en prťsence sont en proportions stoechiomŤtriques : VACA= VBCB soit CA= VBCB / VA = 12,0*5,00 10-2 / 20,0 = 3,00 10-2 mol/L. soit 3,00 10-2 / 50 = 6,00 10-4 mol AH dans 20 mL de lait. Masse d'acide lactique prťsente dans un litre de lait : M(HA) CA= 90* 0,0300 = 2,7 g/L. On considŤre qu'un lait frais a une concentration en acide lactique infťrieure ŗ 1,8 g.L-1 ; la valeur trouvťe, 2,7 g/L ťtant supťrieure ŗ 1,8 g/L, ce lait n'est donc pas frais.
|
|||||||||||||||||||||||||||||
| |
||||||||||||||||||||||||||||||
|
|