|
acide acťtique : dilution, dosage, esterification En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
|||
|
|||
|
|
formule brute : C2H4O2 ; autre nom : acide ťthanoÔque ; formule semi dťveloppťe : 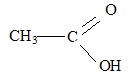
On veut fabriquer 2,0 L d'une solution aqueuse ŗ 1,0 mol/L de cet acide : masse de 1 L de solution commerciale : 1,05 kg = 1050 g n= m/M = 1050/60,05 = 17,5 mol dans 1 L facteur de dilution F= 17,5 / 1 = 17,5 volume de solution mŤre ŗ prťlever pour prťparer 2 L de solution ŗ 1 mol/L : 2 /17,5 = 114,4 mL liste du matťriel : fiole jaugťe 2 L ; burette graduťe ou pipette graduťe + pipeteur consignes de sťcuritť : port de blouse, gants lunettes et travail sous hotte. prťlever 114,4 mL de la solution commerciale ( burette graduťe ou pipette graduťe) ; verser dans la fiole jaugťe de 2 L, contenant un peu d'eau distillťe. complťter avec eau distillťe jusqu'au trait de jauge ; agiter pour rendre homogŤne
prťparer 500,0 mL d'une solution d'acide acťtique de concentration 0,0100 mol/L ŗ partir de la solution prťcťdente : F= 1/0,01 = 100 ; volume pipette jaugťe = 500/100 = 5 mL prťlever 5 mL de la solution mŤre ( pipette jaugťe + pipeteur) ; verser dans la fiole jaugťe de 500 mL. complťter avec eau distillťe jusqu'au trait de jauge ; agiter pour rendre homogŤne.
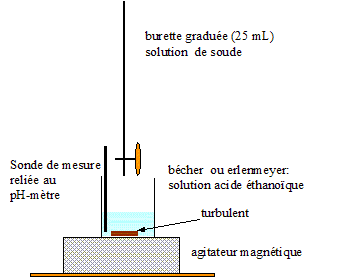
On introduit dans un bťcher 20,0 mL d'une solution d'acide acťtique de concentration Ca= 0,0100 mol/L. On ajoute progressivement une solution d'hydroxyde de sodium de concentration Cb =0,0100 mol/L et on mesure le pH de la solution obtenue. On appelle Vb le volume de solution d'hydroxyde de sodium versť.
schťma du dispositif expťrimental. dťfinition de l'ťquivalence : ŗ l'ťquivalence les quantitťs de matiŤre d'acide et de base mis en prťsence sont en proportions stoechiomŤtriques. Avant l'ťquivalence, dans le bťcher, l'acide est en excŤs ; aprŤs l'ťquivalence la base est en excŤs.
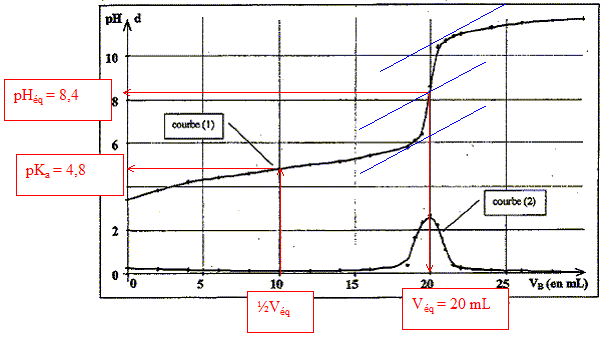
l'acide acťtique est un acide faible : le pH ŗ l'ťquivalence
est diffťrent de 7 ; le pH ŗ la demi-ťquivalence permet de dťterminer
le pKa ( on trouve 4,8 alors que le pKa d'un
acide fort est ťgal ŗ zťro)
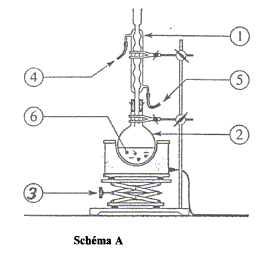
1 : rťfrigťrant ; 2 : ballon ( contenant les rťactifs et les produits) ; 3 : ťlťvateur ŗ croisillons ; 4 : sortie de l'eau ; 5 : entrťe de l'eau : 6 : pierre ponce nom et les caractťristiques de cette rťaction : estťrification, lente athermique, limitťe par l'hydrolyse de l'ester. on chauffe pour accťlťrer la rťaction chimique. nom du composť organique obtenu (ester) : ťthanoate de pentyle. ťquation chimique de la rťaction si on remplace le pentan-1-ol par le propan-1-ol : CH3-CO2H + CH3-(CH2)2-OH= CH3-CO2-(CH2)2-CH3 + H2O.
|
||
|
|