|
d'aprŤs F. Brossard En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
On effectue le suivi cinťtique par spectrophotomťtrie d'une transformation lente mettant en jeu une rťaction entre l'acide oxalique H2C2O4 et les ions permanganate MnO4-. Dans le systŤme ťtudiť, seul l'ion permanganate est colorť en solution. I. Rťglage du spectrophotomŤtre Les mesures sont rťalisťes ŗ une longueur d'onde oý l'absorbance A est la plus grande possible afin d'avoir une meilleure prťcision. Pour choisir cette longueur d'onde, on rťalise le spectre d'absorption de solutions diluťes de permanganate de potassium (K+(aq) + MnO4-(aq) ) qui est reproduit ci-dessous pour diffťrentes concentrations. 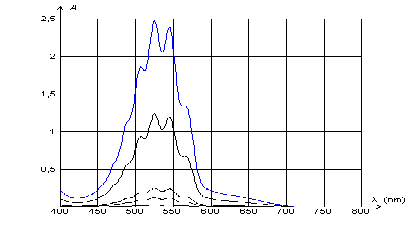 On rappelle que lorsqu'une solution absorbe un rayonnement ťlectromagnťtique visible correspondant ŗ une "couleur", la solution apparaÓt alors de la couleur dite "complťmentaire" ŗ la "couleur absorbťe". Une "ťtoile des couleurs" (sur laquelle le rayonnement absorbť et la couleur complťmentaire sont diamťtralement opposťe) est fournie. 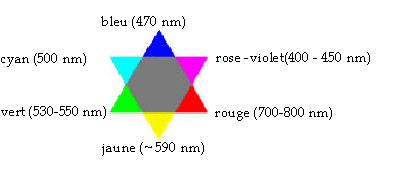
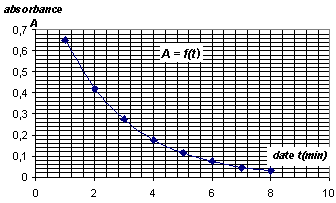
II. Suivi de la transformation Dans un becher de 100 mL, on introduit un volume V1 = 10,0 mL d'une solution de permanganate de potassium acidifiťe de concentration C1 = 1,0 ◊ 10-3 mol. L-1 en ions permanganate. A l'instant t = 0, on ajoute un volume V2 = 10,0 mL d'une solution d'acide oxalique (incolore) de concentration C2 = 1,0 ◊10-2 mol. L-1. On homogťnťise le mťlange et on en verse rapidement une partie dans une cuve de spectrophotomŤtre. On mesure toutes les minutes l'absorbance A de la solution et on note les rťsultats obtenus dans le tableau ci-dessous :
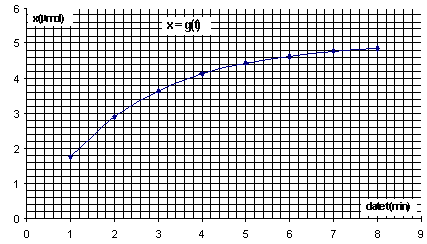
III. Etude de la vitesse
Rose, voire violette ŗ forte concentration La solution absorbe dans le domaine du vert (autour des 550 nm) or d'aprŤs l'ťtoile des couleurs "sa" couleur complťmentaire est le rose. 2 fois { MnO4- + 5e- + 8 H+ = Mn2+ + 4 H2O} rťduction de l'oxydant 5fois { H2C2O4 = 2CO2 + 2 e- + 2H+ } oxydation du rťducteur. On observe une disparition de la coloration violette n(MnO4-)0
= V1C1= 10-5 mol et n(H2C2O4)0
=V2C2= 10- 4 mol
si l'acide oxalique est limitant 10-4-5xmax =0 soit xmax = 2 10-5 mol (la plus petite
valeur "l'emporte"). xmax = 5,0.10-6 mol, et c'est MnO4- le rťactif limitant.
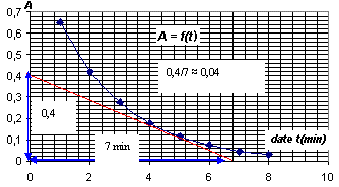
[MnO4-]0 =10-5 / 20 10-3 = 5 10-4 mol/L = ĹC1. ŗ une date t : [MnO4-]= ĹC1- 2x/ V. Or A(t) = k . [MnO4-] d'oý A(t) = k( ĹC1- 2x/ V) A(t) / k = ĹC1- 2x/ V ; ĹC1-A(t) / k= 2x/ V ; x = ĹV(ĹC1-A(t)/k )= VC1- A(t) V/(2k). dťriver par rapport au temps : dx/dt = - V/2k dA/dt v= 1/V dx/dt = -1/(2k) dA/dt La vitesse de rťaction dťcroÓt au cours de temps car la concentration molaire des rťactifs ( facteur cinťtique) diminue.
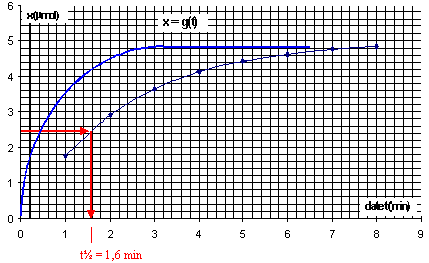
v= - 1/(2k) [dA/dt] t=5 min= 1/4103*0,04 = 10-5 mol L-1 min-1. Le temps de demi rťaction, tĹ, est le temps au bout duquel l'avancement vaut la moitiť de l'avancement final (ici xmax). x(t1/2) =Ĺ xmax = 2,510-6 mol Graphiquement on trouve tĹ = 1,6 min. La tempťrature est un facteur cinťtique dont l'augmentation entraÓne une hausse de la vitesse.
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|