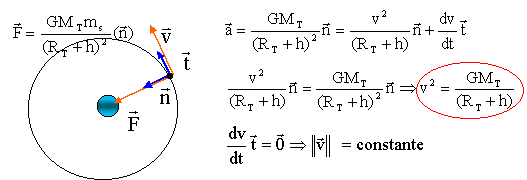|
titrage et indicateurs colorťs d'aprŤs bac France 2005 En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
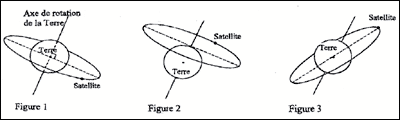
Passionnť d'astronomie, un ťlŤve a collectť sur le rťseau Internet de nombreuses informations concernant les satellites artificiels terrestres. Il met en œuvre ses connaissances de physique pour les vťrifier et les approfondir. Dans tout l'exercice, on notera : Masse de la Terre : MT (rťpartition de masse ŗ symťtrie sphťrique de centre O) ; rayon de la Terre : RT ; masse du satellite ťtudiť : mS ; altitude du satellite ťtudiť : h ; constante de gravitation universelle : G Les questions 2 et 3 sont indťpendantes. 1. Le premier satellite artificiel. Si la possibilitť thťorique de mettre un satellite sur orbite autour de la Terre fut signalťe en 1687 par Isaac Newton, il a fallu attendre le 4 octobre 1957 pour voir le lancement du premier satellite artificiel, Spoutnik 1, par les soviťtiques.
2. Les satellites artificiels ŗ orbites circulaires. Le tťlescope spatial Hubble, qui a permis de nombreuses dťcouvertes en astronomie depuis son lancement en 1990, est en orbite circulaire ŗ 600 km d'altitude et il effectue un tour complet de la Terre en 100 minutes..1. Etude du mouvement du satellite Hubble dans un rťfťrentiel gťocentrique
3. Les satellites artificiels ŗ orbites elliptique. Les satellites peuvent Ítre placťs sur diffťrentes orbites, en fonction de leur mission. Un incident lors de leur satellisation peut modifier l'orbite initialement prťvue. Hipparcos, un satellite d'astromťtrie lancť par la fusťe Ariane le 8 aoŻt 1989, n 'a jamais atteint son orbite prťvue. Un moteur n'ayant pas fonctionnť, il est restť sur une orbite elliptique entre 36 000 km et 500 km d'altitude.
4. Les missions des satellites artificiels. Aujourd'hui plus de 2 600 satellites gravitent autour de la Terre. Ils interviennent dans de nombreux domaines : tťlťphonie, tťlťvision, localisation, gťodťsie, tťlťdťtection, mťtťorologie, astronomie. Leur spectre d'observation est vaste, optique, radar, infrarouge, ultraviolet, ťcoute de signaux radioťlectriques.
corrigť Le satellite est soumis ŗ la seule force de gravitation exercťe par la terre, force centripŤte, dirigťe vers le centre de la terre. Ecrire la seconde loi de Newton suivant l'axe n, pour obtenir l'accťlťration centripŤte, de valeur v≤/(RT+h)
La force centripŤte, perpendiculaire ŗ la vitesse, ne travaille pas ; en consťquence l'ťnergie cinťtique du satellite n'est pas modifiťe et la valeur de la vitesse est constante : le mouvement circulaire est donc uniforme. Le satellite parcourt une circonfťrence 2p(RT+h) ŗ la vitesse v, de valeur constante durant une pťriode T 2p(RT+h) = v T ťlever au carrť puis remplacer v≤ par GMT/(RT+h) 4p2(RT+h)2 = v2 T2 ; 4p2(RT+h)2 = GMT/(RT+h)T2 ; T= 2p((RT+h)3/ GMT) Ĺ. T2 /(RT+h)3 =4p2/ GMT. ( 3Ťme loi de Kepler) un satellite gťostationnaire tourne dans le mÍme sens que la terre, dans le plan ťquatorial ; ce satellite a la mÍme vitesse de rotation que la terre, en consťquence, pour un observateur terrestre il paraÓt fixe. figure 2 : incompatible avec les lois de la mťcanique. Le satellite doit se dťplacer sur une ellipse dont la terre doit Ítre l'un des foyers, ce qui n'est pas le cas sur la figure 2. (ou encore d'aprŤs la premiŤre loi de Kepler le plan de la trajectoire du satellite doit contenir le centre de la Terre) figure 3 : le satellite ne reste pas ŗ la verticale d'un mÍme point de la surface de la terre, lorsque celle-ci tourne autour de son axe. figure 1 : la trajectoire correspond au satellite
gťostationnaire.
loi nį1 : dans le rťfťrentiel gťocentrique ( dans ce cas) la trajectoire du centre d'un satellite est une ellipse dont la terre est l'un des foyers. loi nį3 : tous les satellites en orbite autour d'un astre ( ici la terre) sont tels que le rapport entre le carrť de la pťriode de rťvolution et le cube du demi-grand axede l'ťllipse est constant T2/a3= cte.
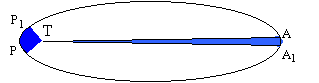
loi des aires : le satellite passe de P ŗ P1 et de A ŗ A1 pendant la mÍme durťe : aire S1= aire S2. Or PT<AT donc arc PP1> arc A A1, en consťquence la vitesse du satellite est plus grande prŤs de P que prŤs de A. La vitesse du satellite varie. en P ( plus proche de la terre que A ) la vitesse est maximale
et en A la vitesse est minimale.
les limites des longueurs d'onde dans le vide de ce spectre : 400 nm : limite entre le visible et les UV ; les longueurs d'onde des UV sont infťrieures ŗ 400 nm. 800 nm : limite entre le visible et l'infrarouge IR ; les longueurs d'onde de l'infrarouge sont supťrieures ŗ 800 nm les limites en frťquence de la lumiŤre visible. f1 = c/l1= 3 108 / 4 10-7 = 7,5 1014 Hz. f2 = c/l2= 3 108 / 8 10-7 = 3,7 1014 Hz. On doit prťciser "dans le vide" pour donner des valeurs de longueur d'onde : la longueur d'onde dťpend du milieu oý l'onde se propage ( seule la frťquence de l'onde est constante lors d'un changement de milieu).
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
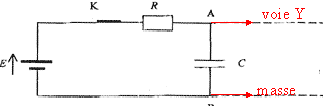
Un ťlŤve, dans le cadre de travaux personnels, souhaite ťtudier un systŤme d'alarme. AprŤs avoir modťlisť la mise sous tension du circuit de commande de la sirŤne (premiŤre partie de l'exercice), il cherche ŗ savoir si des phťnomŤnes inductifs peuvent provoquer le dťclenchement intempestif de la sirŤne (deuxiŤme partie de l'exercice). I. PremiŤre partie : fonctionnement simplifiť d'une alarme d'appartement AprŤs avoir mis sous tension l'alarme d'un appartement, il faut pouvoir disposer d'une durťe suffisante pour sortir sans la dťclencher. Pour cela certains dispositifs utilisent la charge et la dťcharge d'un condensateur. Le circuit est alimentť par une batterie d'accumulateurs de force ťlectromotrice (f.e.m.) E. Le schťma simplifiť de l'alarme est le suivant. 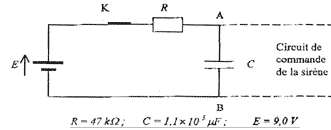 La mise sous tension de l'alarme correspond ŗ la fermeture de l'interrupteur (K). Le circuit de commande de la sirŤne est tel qu'ŗ la fermeture de la porte de l'appartement, le condensateur est mis en court-circuit (ses armatures sont alors reliťes par un fil conducteur non reprťsentť sur le schťma).
DeuxiŤme partie : l'alarme
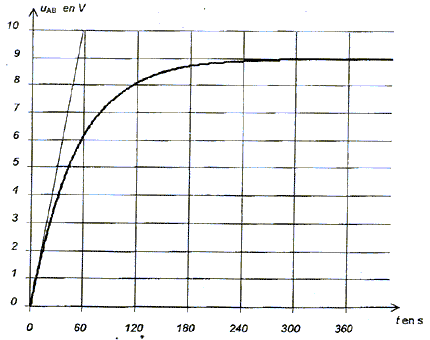
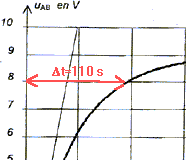
peut-elle se dťclencher de maniŤre intempestive ? 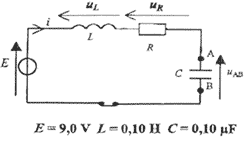 L'ťlŤve enregistre comme dans la premiŤre partie de l'exercice la tension uAB = f(t) aux bornes du condensateur, pour deux valeurs de rťsistance R1 = 160 W et R2 = 2,4 kW . Il obtient les courbes a et b ci-dessous. 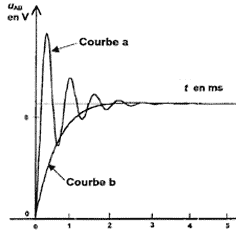
corrigť
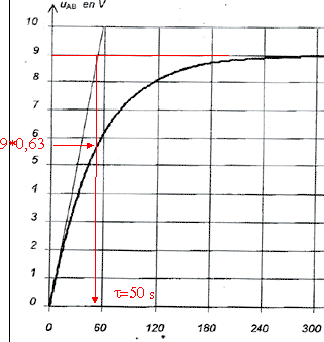
L'intersection de la tangente ŗ l'origine avec l'asymptote donne un point dont l'abscisse est la constante de temps. ou bien tracer une horizontale d'ordonnťe 0,63*9 = 5,7 V ; ŗ partir de l'intersection avec la courbe tracer la verticale.
t= RC = 47 103 * 1,1 10-3 = 52 s.( valeur est compatible avec celle trouvťe graphiquement )
En fermant la
porte, le condensateur est mis en court-circuit : la tension ŗ ses
bornes s'annule. La tension aux bornes du condensateur ne pouvant plus
atteindre 8V ( seuil de dťclenchement de l'alarme), l'alarme ne se
dťclenche pas tant que la porte reste fermťe.
courbe a : rťgime pseudopťriodique ; la rťsistance R n'est pas trŤs ťlevťe (R1 = 160 W). courbe b : rťgime apťriodique ; la rťsistance R n'est ťlevťe (R2 = 2400 W). l'intensitť du courant dans le circuit s'annule ŗ partir de t = 4 ms : la charge q du condensateur est ťagle ŗ : q= C uAB. l'intensitť est ťgale ŗ la dťrivťe de la charge par rapport au temps : i = dq/dt = C duAB/dt duAB/dt correspond au coefficient directeur de la tangente ŗ la courbe uAB=f(t) pour une date donnťe. les courbes a et b se rapprochent de l'horizontale vers t= 4 ms : ŗ partir de cette date, la tangente aux courbes a et b est horizontale ( coefficient directeur nul) et en consťquence l'intensitť s'annule. valeur finale de la tension uAB : uAB+uR+uL=E uR= Ri avec ifin=0 donc uR s'annule. uL= Ldi/dt avec ifin =0 soit difin/dt = 0 et uL=0. en consťquence uAB=E= 9 V au dela de t = 4 ms. Dans le cas de la courbe (a), la tension uAB dťpasse plusieurs fois la valeur limite de dťclenchement de l'alarme : celle-ci se dťclenche par intermittence. calcul de ĹR(C/L)Ĺ>=1 avec C= 1,1 10-3 F ; L= 10-3 H ; R= 4,7 104 W. 0,5*4,7 104 (1,1)Ĺ = 2,5 104, valeur bien supťrieure ŗ 1 : donc il n'y a pas d'oscillations.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
La premiŤre utilisation d'un indicateur colorť pour les titrages acido-basiques remonte ŗ 1767 par W. Lewis. Il employait un extrait de tournesol (...). On utilisait ŗ l'ťpoque des extraits de plantes qui changent de couleur avec l'aciditť du milieu (...). On peut en citer quelques-uns parmi les plus connus et les meilleurs : l'artichaut (...) , la betterave rouge (...) , le chou rouge, de loin l'extrait le plus intťressant car sa couleur change nettement suivant la valeur du pH :
1. Des indicateurs colorťs en cuisine. Le chou rouge est un lťgume riche en fibres et en vitamines, qui se consomme aussi bien en salade que cuit. Mais la cuisson du chou rouge peut rťserver des surprises : chou rouge et eau de cuisson deviennent rapidement bleus. Pour rendre au chou sa couleur violette, on peut ajouter un filet de citron ou du vinaigre. AprŤs avoir ťgouttť le chou, une autre modification de couleur peut surprendre le cuisinier : versťe dans un ťvier contenant un dťtergent, l'eau de cuisson devient verte. En utilisant les textes ci-dessus :
2. Des indicateurs colorťs pour les titrages. De nos jours, les indicateurs colorťs sont toujours largement utilisťs pour les titrages. La pH-mťtrie est une autre technique de titrage acido-basique qui permet en outre de choisir convenablement un indicateur colorť acido-basique pour ces mÍmes titrages. Dans la suite de l'exercice, on s'intťresse au titrage de l'acide ťthanoÔque de formule CH3-CO2H (notť par la suite HA) contenu dans un vinaigre commercial incolore. La base conjuguťe de cet acide sera notťe A-.
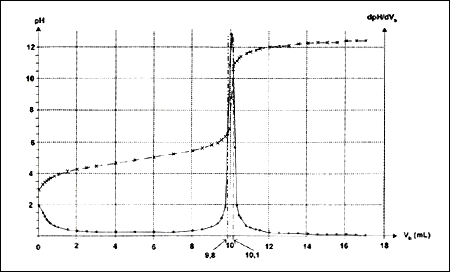
corrigť Un indicateur colorť acido basique est constituť par un couple acide/base dont la forme acide et la forme basique ont des couleurs diffťrentes. Le vinaigre est acide : le chou est violet en prťsence de vinaigre. Le dťtergent est basique : le chou est vert en sa prťsence du dťtergent. Le facteur de dilution vaut 10 : volume fiole jaugťe (mL) / volume pipette jaugťe (mL) = 10. don pipette jaugťe 20,0 mL et fiole jaugťe 200,0 mL. rťaction du titrage : CH3COOH + HO- --> CH3-COO- + H2O, rťaction totale D'aprŤs la
courbe, VBE est proche de 10 mL. Si VB = 6 mL, la
quantitť de matiŤre d'ions HO- versť ŗ la burette est donc
infťrieure ŗ celle de l'acide HA : l'ion HO- est le rťactif
limitant.
d'aprŤs la courbe le pH est voisin de pH=5 aprŤs avoir ajoutť 6 mL de soude. [H3O+]f= 10-pH = 10-5 mol/L. [HO-] f = 10-14 / [H3O+]f= 10-14 /10-5 = 10-9 mol/L le volume du mťlange est : 10+60 +6 = 76 mL= 7,6 10-2 L Qtť de matiŤre ion hydroxyde : (mol) = volume solution (L) * concentration (mol/L) n(OH-)f =7,6 10-2 *10-9=7,6 10-11 mol. xf = n(OH-)0 - n(OH-)f = 6 10-4 - 7,6 10-11 = 6 10-4 mol taux d'avancement
final : t = xf / xmax
= 1; la rťaction est totale.
On peut aussi utiliser la mťthode des tangentes. A l'ťquivalence, n(HA)0 = n(HO-) versť ŗ l'ťquivalence : Ca Va = Cb VBE Ca = Cb VBE / Va = 0,1* 10 / 10 = 1,0.10-1 mol / L en tenant compte
de la dilution : C0 = 10 Ca = 1,0 mol.L-1.
logKi = log[A-ind]ťq/[HAind]ťq+ log[H3O+]ťq log[A-ind]ťq/[HAind]ťq=logKi-log[H3O+]ťq=pH-pKi. [A-ind]ťq/[HAind]ťq= 10pH-pKi. Pour l'artichaut : VB = 9,8 mL, [A-ind]ťq/[HAind]ťq = 106,5 – 7,5 =0,1 VB = 10,1 mL, [A-ind]ťq/[HAind]ťq = 1010,5 – 7,5 =103.
L'artichaut est l'indicateur adaptť. Si le vinaigre est colorť, alors il masque le virage de l'incolore au jaune de l'indicateur.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||