Physico-chimie
du corps humain : la digestion, synthèse d'un médicament
antispasmodique. Concours général physique 2024.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
.
| . |
.
.
|
|
.
.
|
..
..
......
...
|
Synthèse d'un médicament antispasmodique, l'hymécromone.
Protocole.
Etape 1. Dans un erlenmeyer n° 1 on introduit 1,0 g de résine Dowex, une masse m1 = 0,805 g de résorcinol et V0
= 1,00 mL de 3-oxobutanoate d'éthyle. L'erlenmeyer est placé 30 minutes
au bain marie à 80°C. On observe un léger dégagement gazeux qui cesse
en fin de réaction. A la fin de la réaction, le milieu réactionnel est
solide.
Etape 2.
On ajoute 3 mL d'éthanol pour dissoudre le solide ( la résine reste
insoluble). On transfert le liquide surnageant dans un erlenmeyer n°2.
La résine est rincée avec 2 mL d'éthanol puis celui-ci est transféré
dans l'erlenmeyer 2.
Etape 3. La
solution de l'erlenmeyer 2 est chauffée au bain-marie puis de l'eau
chaude est ajoutée jusqu'à ce que la solution devienne trouble. On
laisse refroidir à température ambiante puis dans un bain de glace
pendant 15 min.
Etape 4. Les
cristaux blancs obtenus sont filtrés sur Büchner, rincés avec 5 mL
d'eau froide. Le produit est séché et placé à l'étuve durant 15 min. On
obtient une masse m2 = 907 mg de produit.
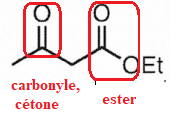
16. Recopier la formule de l'acétoacétate d'éthyle, entourer les groupes caractéristiques, nommer les familles fonctionnelles.
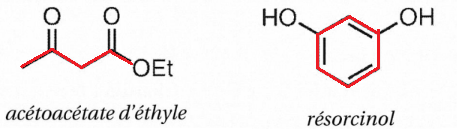
17. Recopier la formule de l'hymécromone et entourer les chaînes carbonées de chacun des deux réactifs.
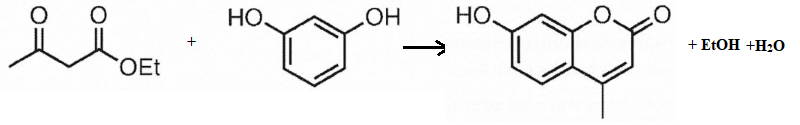
18. Ecrire l'équation de la réaction qui modélise la formation de l'hymécromone.
19. Expliquer le léger dégagement gazeux ( étape 1).
Température d'ébullition de l'éthano = 78°C. L'éthanol se dégage.
20. Expliquer le trouble lors de l'ajout d'eau chaude dans l'étape 3..
L'hymécromone est insoluble dans l'eau froide, très peu soluble dans l'eau chaude..
21. Expliquer l'intérêt du lavage à l'eau froide ( étape 4).
On élimine le réactif en excès.
22. Calculer la quantité de matière de chaque réactif. Identifier le réactif limitant.
Acétoacétate d'éthyle : M = 130,14 ; n1=1,03 / 130,14 =7,91 10-3 mol.
Résorcinol M = 110,11 g/mol ; n2 =0,805 / 110,11 =7,31 10-3 mol.
Les coefficient stoéchiométriques étant identiques, le résorcinol est en défaut.
23. Calculer le rendement de la synthèse.
M(hymécromone) =176,17 g / mol ; nthéorique = 7,31 10-3 mol.
Masse théorique : 7,31 10-3 x176,17 =1,29 g.
Rendement : masse réelle / masse théorique = 0,907 / 1,29 ~0,70 (70 %).
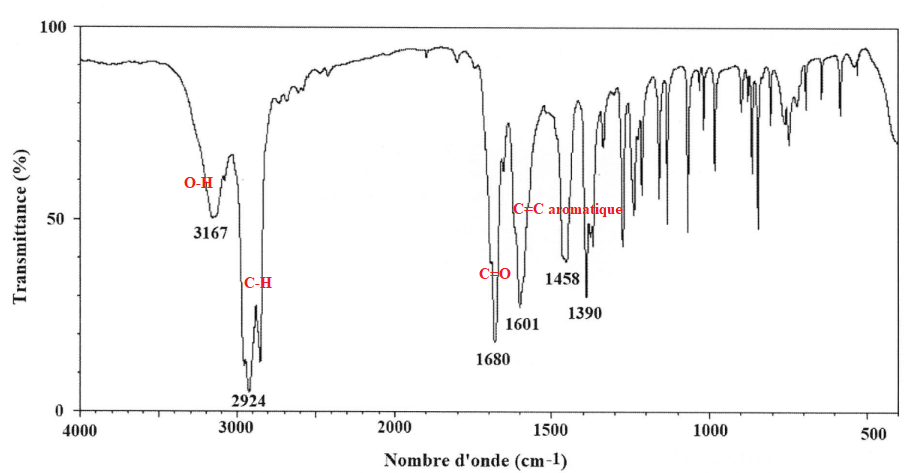
24. Analyser le spectre IR de l'hymécromone.
Etude du mécanisme réactionnel.
25. Le résorcinol est noté Ar-OH ; le groupement CH3-CO-CH2 est noté R. Représenter les flèches courbes ; indiquer le type de réaction mis en jeu à chaque étape.
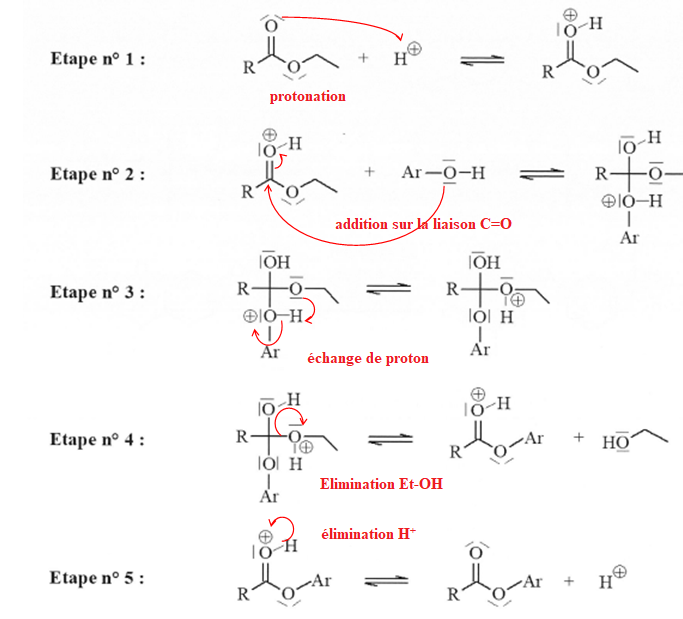
26. Indiquer le rôle des protons H+ fournis par la résine. Justifier.
Catalyseur ; H+ est consommé à la première étape puis régénéré à la dernlère étape.
|
...
|
....
|
Etude de l'impact environnemental de la synthèse.
La synthèse classique de l'hymécromone se fait dans le toluène au reflux en présence de trixhlorure de phosphoryle.
Expliquer pourquoi la synthèse présentée ici peut-être qualifiée de synthèse "verte".
Travail dans des conditions plus sûres : les substances utilisées sont faiblement ou non toxiques.
Utilisation de solvants non toxiques.
Préférer des procédés catalytiques aux procédés classiques.
|




