Une
batterie comestible,
bac Amérique du
nord 2024
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
.
| . |
.
.
|
|
.
. |
..
..
......
...
|
1. Composition et fonctionnement de la pile.
Le prototype réalisé par des chercheurs italiens est constitué de deux
electrodes :
- la premiere notée CA/ R est en or, recouverte de charbon actif et de
0, 75 mg de riboflavine ou vitamine B2;
- la seconde notée CA/ Q est en or, recouverte de charbon actif et de
0,60 mg de quercétine
(pigment
végétal présent dans les capres ou l'oignon rouge).
L'ensemble est séparé par un film d'algue Nori immergé dans une
solution électrolytique d'hydrogénosulfate de sodium (Na+(aq)
; HSO4·(aq)) puis encapsule dans de la cire
d'abeille
Lors de son tonctionnement, la pile permet d'obtenir une tension de
0,65 V et de delivrer un courant d'intensitée constante de 48 μA
pendant une durée Dt
=12 minutes. Ce courant permet selon les scientifiques itallens
d'alimenter de petits dispositifs médicaux.
Q.1. Ecrire
l'équation de la réaction électrochimique modélisant la transformation
de la riboflavine lors du fonctionnement de la pile.
Q.2. En
déduire si la riboflavine subit une oxydation ou une réduction.
Justifier.
C17H20N4O6
(s) --> C17H18N4O6
(s)+2H++2e-.
Le réducteur riboflavine s'oxyde en libérant des électrons ( borne
négative).
La pile comestible est utilisée pour alimenter une résistance.
Q.3. Compléter le
schéma de fonctionnement de la pile en mentionnant :
- la borne positive
- la borne négative
- le sens du courant dans le circuit
le sens des électrons dans le circuit.
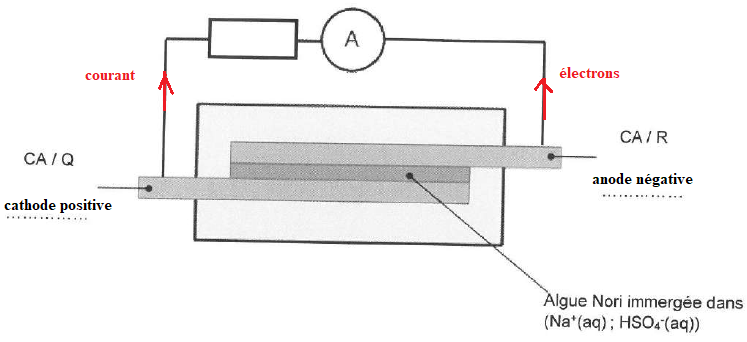
Q.4. lndiquer le
rôle jouée par le film d'algue Nori immergé dans la solution
électrolytique d'hydrogénosulfate de sodium.
Comme un pont salin, elle ferme le circuit électrique et maintient
l'électroneutralité des électrolytes dans chaque compartiment.
La réaction électrochimique modéelisant la transformation mise en jeu
sur l'electrode recouverte de quercetine est :
C15H10O7(s) +2H+aq +2e-
--> C15H12O7(s).
Q.5. Déterminer la
charge eélectrique Q délivrée par la pile pendant les 12 min de
fonctionnement.
Q=I Dt =48 10-6
x12 x60 =3,5 10-2 C.
Q.6. En déduire que
la quantité de matière d'électrons n(e) consommée par l'électrode
recouverte de quercétine pendant cette durée vaut n(e) = 3,6x 10-7
mol.
Q = n(e) F ; n(e) = 3,5 10-2 / 96500 = 3,6x 10-7
mol.
Q.7.
lndiquer si, au bout de 12 min, la demi-pile est déchargée en calculant
le pourcentage de quercétine qui a été consommée pendant cette durée.
n(quercétine) = 0,5 n(e)=1,8 10-7 mol.
M(quercétine) = 302,24 g / mol.
m = 1,8 10-7 x302,24 =5,4 10-5 g = 54 µg=0,054 mg.
0,054 / 0,60 x100 =9 %. La demi-pile n'est pas déchargée.
|
...
|
....
|
2. Recharge de la pile
Une deuxième possibilité d'application de cette
batterie comestible est son utilisation pour remplacer les piles
Lithium-Ion ou Nickel Metal Hybride utilisées dans les jouets. En
effet, ces dernières présentent un danger d'intoxication en cas
d'ingestion par un jeune enfant.
Les scientifiques italiens ont étudié le comportement de leur prototype
après plusieurs charges sous une tension comprise entre 0,60 et 0,80 V
pour un courant de 48 μA.
Q.8. lndiquer la
courbe qui représente la charge de la batterie comestible en analysant
le graphe. Expliquer.
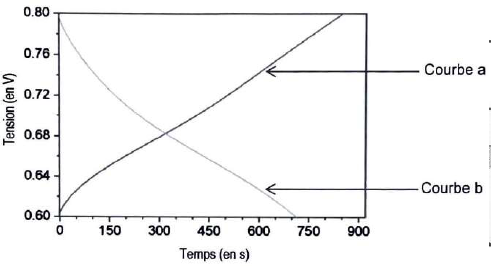
Lors de la charge, la tension aux bornes de la pile augmente : courbe a.
Lors de la décharge, la tension aux bornes de la pile diminue : courbe
b.
On cherche à comparer la capacité d'une pile comestible à celle d'une
pile classique Nickel Metal Hybride.
Q.9. Calculer, avec
les données fournies (1,2 V ; 0,048 Wh ; 40 h), la
capacité en A.h de la pile Nickel Metal Hybride. Discuter de la
possibilité d'une réelle application de la batterie comestible dans la
vie courante.
Pile Nickel Metal Hybride : énergie : 0,048 Wh ;
Puissance (W)= énergie ( Wh) / durée (h) = 0,048 / 40 =1,2 10-3
W.
Intensité = puissance (W) / tension (V) = 1,2 10-3 /1,2 =1,0
10-3 A.
Capacité (Wh) = intensité (A) x durée (h) = 1,0 10-3 x40
=0,040 Ah.
Capacité de la batterie comestible : 10 µAh = 1,0 10-5 Ah.
0,040 / (1,0 10-5)=4000.
La capacité de la batterie comestible est 4000 fois plus petite que la
capacité d'une pile Nickel Metal Hybride. La batterie comestible ne
peut pas remplacer la pile Nickel metal Hybride.
|
ane.
|
|
|