Le
gallate de propyle, bac Amérique du
nord 2024
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
.
| . |
.
.
|
|
.
. |
..
..
......
...
|
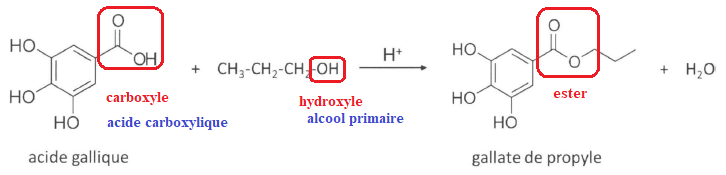
Le gallate de propyle (E310) peut être synthétisé à partir d'acide gallique et de propan-1-ol, en présence d'ions H+, selon une transformation chimique modélisée par la réaction dont l'équation est donnée ci-dessous.
D'après la réglementation NGAA (Norme Générale pour les Additifs
Alimentaires), la teneur maximale autorisée de ce conservateur est de
200 mg par kilogramme d'aliment.
Q.1. Recopier sur
la copie les formules de l'acide gallique et du gallate de propyle.
Entourer les groupes caractéristiques modifiés lors de la
transformation de l'acide gallique en gallate de propyle et nommer les
familles fonctionnelles correspondantes.
Le mécanisme réactionnel de la synthèse comporte cinq étapes, dont les
étapes 3 et 4 sont représentées sur le document fourni en Annexe à
rendre avec la copie.
Q.2. Représenter les flèches courbes de l'acte élémentaire correspondant à l'étape 3 du mécanisme, en justifiant leur sens.
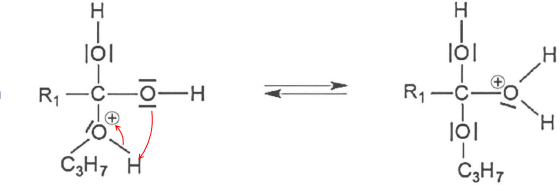
Attaque du doublet de l'oxygène de l'alcool vers le site électrophile O +H.
Q.3. Représenter le
schéma de Lewis de l'espèce chimique obtenue lors de l'étape 4.
Justifier le qualificatif d'intermédiaire réactionnel donné à cette
entité.
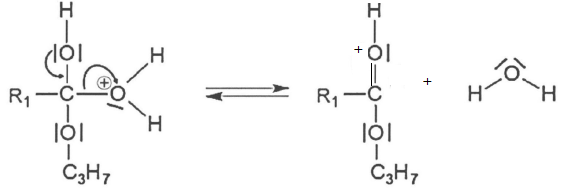
Espèce chimique participant àun mécanisme réactionnel et qui n'est ni un réactif, ni un produit dans l'équation bilan.
Q.4. Indiquer le rle joué par les ions hydrogène H +lors de cette transformation.
H + joue le rôle de catalyseur.
|
...
|
....
|
On
utilise le gallate de propyle comme conservateur dans de l'huile
d'olive alimentaire. On le synthétise en faisant réagir l'acide
gallique avec un excès de propan-1-ol dans des conditions
expérimentales où le rendement de la synthèse est de 60 %.
Q.5. Indiquer l'intérêt d'introduire en excès le propan-1-ol.
En utilisant un réactif en excès ( le moins couteux ) on déplace l'équilibre dans le sens direct. Le rendement augmente.
Q.6. Déterminer la
masse d'acide gallique nécessaire pour obtenir 500 litres d'huile
possédant la teneur maximale en conservateur autorisée par la
réglementation. Commenter le résultat.
Données:
- masse molaire de l'acide gallique : M1 = 170,1 g-mol-1;
- masse molaire du gallate de propyle : M2 = 212,2 g-mol-1;
- masse volumique de l'huile d'olive : r = 0,91kg-L-1.
Masse d'huile d'olive : 500 x0,91 =455 kg.
La masse maximale autorisée de ce conservateur est de 200 mg par kilogramme d'aliment.
Masse maximale de conservateur : 0,2 x 455=91 g.
Quantité de matière correspondante : 91 / 212,2=0,429 mol.
Quantité de matière d'acide gallique : 0,429 / 0,60 =0,715 mol.
Masse d'acide gallique : 0,715 x 170,1 =121,6 g..
|
ane.
|
|
|