L'acide
butyrique,
bac général La Réunion
2023.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
.
| .. |
.
.
|
|
.
.
|
..
..
......
...
|
PARTIE A : Étude d’une solution aqueuse d’acide butyrique.
On notera dans cette partie, pour simplifier, l’acide butyrique AH(aq) et sa base conjuguée A(aq)
−
.
On considère un volume V = 100 mL d’une solution d’acide butyrique de concentration en
quantité de matière C = 1,0 × 10−4 mol ⋅ L
−1
. La mesure du pH de la solution donne pH = 4,5.
L’acide butyrique réagit avec l’eau selon l’équation de réaction suivante :
AH(aq) + H2O(l) ⇄ A
−(aq) + H3O
+(aq)
A.1. Donner l’expression du taux d’avancement final t de la réaction étudiée en fonction de
l’avancement final xf et de l’avancement maximal xmax.
t = xf / xmax.
A.2. Exprimer l’avancement maximal xmax en fonction de C et V.
xmax = CV.
A.3. Exprimer la valeur de l’avancement final xf en fonction du pH et de V.
xf = [H3O
+(aq)] V = 10-pH V.
A.4. Calculer le taux d’avancement final t et justifier que l’acide butyrique est un acide faible.
xf / xmax =10-pH / C =10-4,5 / (1,0 10-4)~0,32.
Le taux d'avancement final étant inférieur à 1, l'acide butyrique est un acide faible.
On montre que les concentrations en quantité de matière à l’équilibre peuvent s’exprimer de la
manière suivante :
[AH(aq) ]eq = C × (1 − t) pour l’acide butyrique,
[A
−(aq)]eq = C t pour sa base conjuguée.
A.5.1. Exprimer la constante d’acidité Ka de la réaction en fonction de t et C.
Ka =
[A
−(aq)]eq [H3O
+(aq)] / [AH(aq) ]eq =(Ct)2 /(C × (1 − t)) = C t2 /(1-t).
A.5.2. En déduire la valeur du pKa de l’acide butyrique.
Ka = 1,0 10-4 x0,322 /(1-0,32)=1,5 10-5 ; pKa = - log (1,5 10-5)=4,8.
PARTIE B : Synthèse d’un ester à l’odeur de pomme à partir de l’acide butyrique.
Même si l’acide butyrique possède une odeur désagréable, certains esters issus de cet acide ont
une odeur agréable souvent fruitée. C’est le cas du butanoate de méthyle qui a une odeur de
pomme.
La synthèse du butanoate de méthyle est réalisée selon le protocole suivant :
- verser dans un ballon à fond rond 20 mL de méthanol, 20 mL d’acide butyrique et 4 mL
d’acide sulfurique concentré ;
- ajouter quelques grains de pierre ponce ;
- chauffer à reflux pendant 15 min ;
- laisser refroidir en enlevant le chauffe-ballon ;
- verser le contenu du ballon dans un bécher contenant 40 mL de solution saturée en
NaCl(s) ;
- transvaser ensuite dans l’ampoule à décanter et laisser décanter ;
- séparer les deux phases ;
- recueillir la phase organique et la sécher sur du sulfate de magnésium anhydre ;
- purifier l’ester obtenu par distillation.
L’équation de réaction de la synthèse est la suivante :
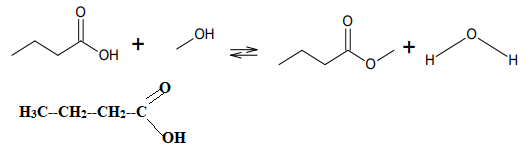
B.1. Donner la formule semi-développée de l’acide butyrique.
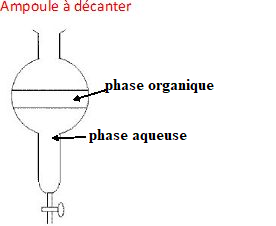
B.2. Préciser la phase dans laquelle se trouve le butanoate de méthyle.
La solubilité de l'ester est très faible dans l'eau salée. L'ester est
dans la phase organique de densité inférieure à celle de l'eau salée.
B.3. Schématiser l’ampoule à décanter après décantation. Justifier la position des deux phases.
 Le spectre du produit synthétisé est fourni.
Le spectre du produit synthétisé est fourni.
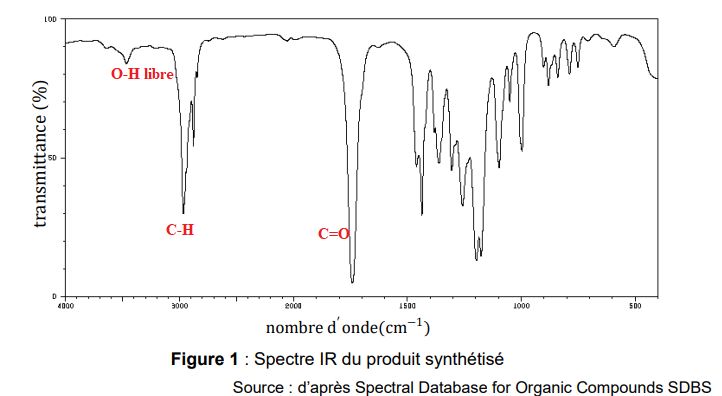
B.4. Attribuer un groupe d’atomes à chacun des pics entre les valeurs de nombre d’onde
comprises entre 1600 cm−1 et 4000 cm−1
. Indiquer si ce spectre IR est compatible avec le
produit de réaction attendu.
Ce spectre est compatible avec l'ester.
|