Le fluor 18, un traceur radioactif
.
Le fluor 18, notť
18F, est un isotope du fluor. Il est utilisť en mťdecine nuclťaire comme
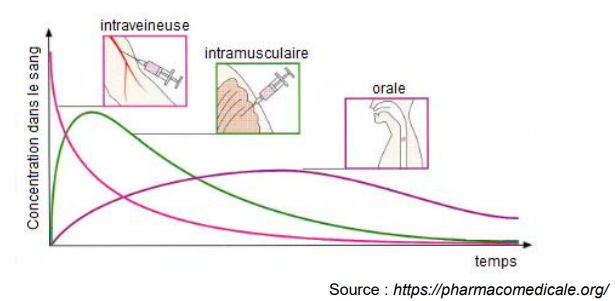
radio-traceur intťgrť dans des molťcules de glucose modifiťes. La solution de glucose
marquť au fluor 18 est injectťe au patient pour l’examen.
La pťriode radioactive (ou demi-vie) du fluor 18 vaut TĹ = 110 min.
Il est le siŤge d’une dťsintťgration radioactive de type β
+
.
On admet que la radioactivitť de l’ťchantillon injectť devient inactive au bout de 20 pťriodes
radioactives (ou demi-vies) ťcoulťes.
1. Dťfinir l’expression ę noyaux isotopes Ľ.
Des noyaux isotopes ne diffŤrent que par leur nombre de neutrons ; ils ont le mÍme numťro atomique Z.
2. Donner la composition du noyau
189F d’un atome de fluor 18.
9 protons ; 18-9 = 9 neutrons.
L’ťquation de la rťaction de dťsintťgration nuclťaire du fluor 18 s’ťcrit :
189F →
AZ X +
01e
+ γ
3. Donner le nom de la particule
01e ťmise par le fluor 18 lors de sa dťsintťgration β
+
.
Positon.
4. Identifier parmi les noyaux suivants le noyau fils
AZ X
ťmis lors de la dťsintťgration du
fluor
89F
. Justifier ce choix.
188O ;
198O ; 1910Ne ; 2010Ne.
Conservation du nombre de nuclťons : 18 = A ;
conservation de la charge : 9 = Z+1 soit Z = 8. Donc
188O.
5. Donner la dťfinition de la pťriode radioactive (ou demi-vie) T
1/2 d’un radio-traceur.
Durťe au bout de laquelle l'activitť initiale est divisťe par 2.
6. Dťterminer le temps au bout duquel l’activitť d’un ťchantillon de fluor 18 est divisťe
par 8 par rapport ŗ sa valeur initiale.
8 = 2
3 soit trois demi vie ou 3 x110 = 330 min.
7. L’activitť initiale du produit injectť est de 400 MBq. Dťterminer une valeur approchťe de
l’activitť rťsiduelle 12 heures et 50 minutes aprŤs l’injection, c’est-ŗ-dire aprŤs 7 pťriodes
radioactives du fluor 18.
L'activitť initiale est divisťe par 2
7 =128.
400 / 128 ~3,1 MBq = 3,1 106 Bq.
8. L’activitť radioactive naturelle du corps humain est de l’ordre de 120 Bq par kilogramme de
masse corporelle. Elle est due ŗ l’ingestion d’aliments contenant naturellement des
ťlťments radioactifs. Justifier pourquoi il est conseillť au patient ayant subi l’examen
d’imagerie mťdicale d’ťviter un contact ťtroit (de moins de 1 m) et prolongť (de plus de 30
minutes) avec toute personne pendant le reste de la journťe.
Pour un patient de 60 kg : 120 x 60 =7200 Bq <
3,1 106 Bq due au fluor.
L'activitť radioactive du patient est trop ťlevťe.
Diagnostiquer des maladies avec un produit de contraste.
Un produit de contraste est une substance injectable ou ingťrable utilisť en imagerie mťdicale
pour augmenter artificiellement le faible contraste naturel de certains tissus afin de
mieux visualiser les organes explorťs. Pour certains types d’imagerie mťdicale, un produit de
contraste ŗ base d’iode peut Ítre utilisť.
La Gastrografine est un produit de contraste iodť dont le principe actif, l’ion amidotrizoate, est
la base du couple acide amidotrizoÔque / ion amidotrizoate. La formule brute de l’acide
amidotrizoÔque est C
11H
9
I
3N
2O
4
.
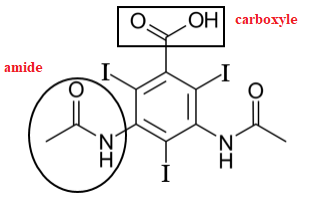
Sa formule topologique est donnťe ci-dessous.
Dans un flacon de produit de contraste Gastrografine, la concentration en masse d’iode vaut
C
m = 370 g∙L
-1
. Ce produit de contraste est spťcifique aux explorations gastro-intestinales.
La masse de produit de contraste ŗ absorber dťpend de la masse corporelle du patient.
La masse d’iode ŗ absorber est de 500 milligrammes par kilogramme de masse corporelle du
patient.
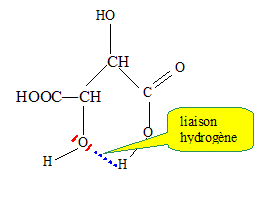
1. Nommer les deux groupes caractťristiques entourťs sur la formule de l’acide
amidotrizoÔque.
 2.
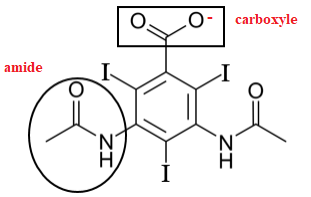
2. Justifier le caractŤre acide de l’acide amidotrizoÔque et ťcrire la formule brute de la base
associťe.
La molťcule possŤde une fonction acide carboxylique.
 3.
3. Un patient de masse corporelle m = 73 kg doit rťaliser un scanner nťcessitant l’absorption
de Gastrografine.
3.1. Calculer la masse d’iode ŗ donner au patient.
0,500 x 73 = 36,5 g d'iode.
3.2. En dťduire le volume de Gastrografine ŗ administrer et prťciser si un flacon
commercial de 100 mL est suffisant.
Cm = 370 g∙L-1 soit 37 g dans 100 mL.
37 > 36,5 : un flacon commercial est suffisant.