Chimie
analytique, concours interne technicien principal police technique et
scientifique 2019.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
..
..
|
.
.
|
..
..
......
...
|
Partie A.
1.a. Selon quelle norme internationnale, qui spécifie les
exigences de qualité et de compétence des labortoires d'essais, est
accréditée la section Toxicologie du LPS de Paris ?
Norme ISO/CEI 17125.
1.b Quel est l"organisme qui accrédite les laboratoires en France ?
Le COFRA (COmité FRanèais d'ACcréditation).
2. Quels sont les facteurs d'influence ( les "5M") vérifiés lors de la validation de cette méthode d'analyse ?
La méthode des 5 M est une méthode d'analyse qui permet d'identifier les causes/otigines possibles d'un problème.
Matière : matière et matériaux utilisés ( entrées du processus).
Matériel : l'équipement des machines.
Méthode : le mode opératoire.
Main-d'oeuvre : les interentions humaines.
Milieu : l'environnement, le contexte.
3. Donner le nom IUPAC et la formule semi-développée de l'isopropanol.
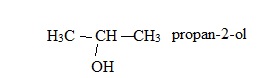 4.
Que signifie le pictogramme suivant visible sur un flacon d'acide
formique ? Quelles précautions prendre lors de la manipulation ?
4.
Que signifie le pictogramme suivant visible sur un flacon d'acide
formique ? Quelles précautions prendre lors de la manipulation ?

Port de blouse, gants et lunettes de protection.
5. Quel est l'intérêt d'utiliser une combinaison de solvants pour l'extraction ?
Cela permet de modifier, d'ajuster au mieux, la polarité de la phase liquide.
6. Préciser le rôle de chaque maillon de la chaine d'analyse LC-MS-MS.
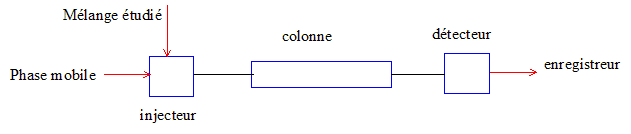 L'échantillon
à analyser est entraîné par la phase liquide mobile dans une
colonne remplie d'une phase stationnaire constituée de grains de petite
taille. Un débit élevé de la phase mobile et cette fine granulométrie
permet une bonne séparation des composants.
7. Que signifient les indications 100 mm x 2,1 mm x 2,6 µm portées sur la colonne utilisée ?
L'échantillon
à analyser est entraîné par la phase liquide mobile dans une
colonne remplie d'une phase stationnaire constituée de grains de petite
taille. Un débit élevé de la phase mobile et cette fine granulométrie
permet une bonne séparation des composants.
7. Que signifient les indications 100 mm x 2,1 mm x 2,6 µm portées sur la colonne utilisée ?
Longueur : 100 mm , diamètre intérieur 2,1 mm, granulométrie, taille des grains : 2,6 µm.
8. Expliquer le principe d'une source ESI.
On applique un fort champ électrique sur un liquide traversant un
capillaire. A la sortie il se forme des goutellettes hautement chargées.
9. Quelles sont les
quatre grandes familles de stupéfiants rechercher dans un prélèvement
salivaire ? Donner un exemple de substances pour chaque famille.
Perturbateurs / hallucinogènes : cannabis, chanvre.
Dépresseurs, opiacés : morphine, héroïne.
Stimulants : cocaïne et crack.
Stimulants : amphétamines et dérivées, ecstasy.
10. Qu'est-ce q'un métabolite ? Quelles indications peut fournir leur présence ?
Un métabolite est un composé organique intermédiaire ou issu du
métabolisme. Ce terme est réservé aux petites molécules ( monomère) par
opposition aux macromolécules. Par exemple le glucose est un
métabolite, contrairement au glycogène.
La présence des molécules mères retrouvées dans la salive, révèlent la consommation des 24 dernières heures.
11. Le conducteur est-il en infraction ? Si oui, s'agit-il d'une contravention, d'un délit ou d'un crime ?
Le taux relevé pour la cocaïne est de 15 ng / mL de salive. Ce conducteur est en infraction.
Il s'agit d'un délit : jusqu'à 2 ans emprisonnement et 4500 € d'amende.
Partie B.
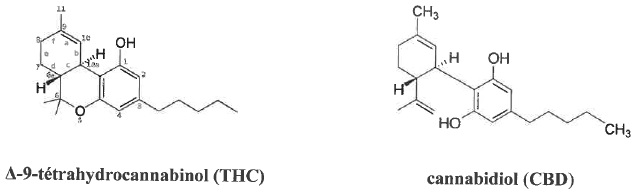
1. Représenter le D-8-tétrahydroxycannabinol, isomère du D-9-THC.
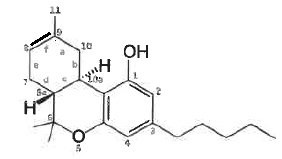
2. Calculer la masse molaire de chacune de ces molécules. En quoi les molécules de THC et de CBD diffèrent-elles ?
M = 314 g / mol.
THC : présence d'un cycle suplémentaire par rapport au CBD.
Fonction alcool supplémentaire et liaison double C=C supplémentaire dans le CBD.
3. Pourquoi l'échantillon est-il broyé minutieusement ?
Il est plus facile de dissoudre une poudre fine qu'un solide constitué de grosses particules.
4. Expliquer à l'aide d'un schéma annoté le principe de la chromatographie en phase gazeuse.
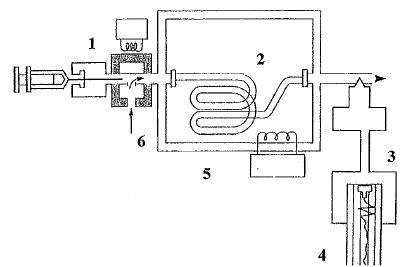
1 : injecteur ; 2 : colonne ; 3 : détecteur ; 4 : intégrateur ou
ordinateur ; 5 : thermostat de colonne ; 6 : gaz vecteur.
5. Quel gaz vecteur sont couramment employés en CPG ?
Hydrogène, hélium, azote.
6. Que signifie les modes "split" et "splitless". Pourquoi l'échantillon A est-il injecté en mode "splitless ?
Les injecteurs peuvent fonctionner suivant
deux modes, avec ou sans division (encore appelés split ou splitless).
En
mode split, le gaz vecteur pénètre avec un grand débit dans la chambre
de vaporisation ; une vanne de fuite sépare le courant gazeux en deux
parties : seule la plus petite pénétre dans la colonne.
Ce mode est utilisé dans les colonnes capillaires à faible débit. Le
mode splitless est utilisé dans le cas d'échantillons très dilués.
7. Quelle grandeur
est représentée en ordonnées sur les chromatogrammes ? Donner le temps
de rétention du CBD et celui du THC en mode split.
L'intensité du signal ( ansorbance, luminescence, conductivité, m / z) est portée en ordonnée
Temps de rétention CBD : 7 min ; temps de rétention THC :7,4 min.
8.a. A quoi correspondent les pics des spectres 314 et 315 ?
Il s'agit des pics moléculaires M et M+1 ( carbone 13 : 1 % du pic de base).
b. Comment le CBD et le THC sont-ils identifiés ?
Le pic de base du CBD se situe à m/z = 231 ; le pic de base du THC se
situe à m / z =299. Pour le THC, on observe également un pic très
important à m / z = 231.
c. Pour chacun de ces composés, quel pic choisir pour une quantification ?
On choisit le pic de base, le plus important.
Le dosage des traces de THC s'effectue par GC-MS, en mode SIM, en utilisant la méthode de l'étalon interne.
9. Qu'est ce qu'un mode SIM ? Quel est son intérêt ? Citer un autre mode d'acquisition.
Un ion cible de rapport m / z donné est recherché. l'analyseur est
configuré pour permettre uniquement aux ions d'un rapport m / z donné
de passer dans le détecteur.
Mode : full scan. L'analyseur est scanné de manière séquentielle et
passe chaque m / z dans la gamme sélectionnée vers le détecteur.
Spectromètre de masse MSMS : sélection de l'ion à fragmenter ;
fragmentation de cet ion ; analyse des ions issus de la fragmentation.
10. Donner les avantages de la méthode de dosage par étalonnage interne.
Cette technique permet de s'affranchir complètement des volumes injectés.
Elle
est relativement longue à mettre en oeuvre. L'étalon interne n'est pas
facile à trouver : il doit avoir une structure chimique proche des
solutés analysés, ne pas interférer avec les solutés, ne pas réagir
chimiquement avec d'autres constituants présents et doit être
compatible avec le système de détection.
Unr prise d'essai de 10 mg est effectuée à laquelle on ajoute 1 mL de
solvant. Après extraction et centrigugation, l'extrait est repris avec
une solution de THC-d3 à 10 µg / mL.
11. Que signifie THC-d3 ? Quel est son rôle dans le protocole ?
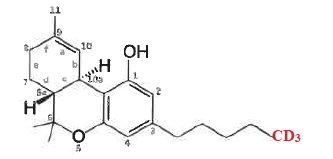 Il sert d'étallon interne. Il sert d'étallon interne.
12. Les temps de
rétention du THC et du THC-d3 sont très proches. Cela pose t-il un
problème pour effectuer le dosage de traces de THC dans ces conditions
? Justifier.
Réponse non. L'étalon interne THC-d3 doit avoir un temps de rétention
proche du temps de rétention du THC. De plus l'aire du pic de l'étalon
interne doit être du même ordre de grandeur que l'aire du pic
correspondant au THC.
13. Pourquoi la séquence analytique est-elle encadrée par deux témoins ?
Cela permet d'avoir une calibration en deux points, car la réponse du détecteur n'est pas tout à fait linéaire.
14. Calculer la concentration de THC dans l'échantillon A en µg / mL, puis exprimer cette valeur en pourcentage massique.
Masse pesée de l'échantillon A : 9,378 mg ; aire THC : 6041 ; aire THC-d3 : 7340.
6041 / 7640 =0,79.
Concentration du THC-d3 : 10 µg / mL ; concentration du THC : 10 x0,79 = 7,9 µg / mL.
Masse dans 10 mL : 7,9 10-2 mg.
Pourcentage massique : 7,9 10-2 / 9,378 =0,0084 ( 0,84 %).
L'échantillon A est un produit brut non autorisé, sa teneur en THC est supérieure à 0,2 %.
|
...
|
....
|
L'eau oxygénée.
Le titre volumique d'une solution d'eau oxygénée est le volume de
dioxygène se dégageant lors de la décomposition d'un litre de solution
dans les conditions normales de température et de pression.
1. Montrer
que : titre volumique = 11,2 x concentration en mol / L. Quelle
est la concentration en peroxyde d'hydrogène d'une eau oxygénée à 30
volumes.
H2O2(l) --> H2O(l) + ½O2(g).
Quantité de matière de H2O2 dans 1 L de concentration C mol / L : C.
Quantité de matière de dioxygène libérée ½C mol.
Volume molaire des gaz dans ces conditions : 22,4 L / mol.
Volume de dioxygène : 22,4 x ½C = 11,2 C.
Concentration d'une eau oxygénée à 30 volumes : C = 30 / 11,2 ~2,7 mol / L.
Le permanganate de potassium réagit avec l'eau oxygénée selon une réaction d'oxydo-réduction très exothermique.
2. Ecrire l'équation de cette réaction. Quels sont les effets produits par cette réaction ?
2 fois { MnO4- + 8H+ + 5e- = Mn2+ + 4H2O } réduction
5 fois {H2O2 = O2 + 2H+ + 2e- } oxydation
2 MnO4- + 5 H2O2 + 6H+ --> 5 O2 + 2 Mn2+ + 8H2O.
Réaction très exothermique, l'eau se vaporise et forme un brouillard.
3. Quel explosif très instable peut être synthétisé artisanalement à partir de l'eau oxygénée ?
Le peroxyde d'acétone ( eau oxygénée + acétone).
Essence.
La nouvelle dénomination Sans plomb 95 ou 98 est E5, ce qui signifie que ce carburant peut contenir jusqu'à 5 % d'éthanol.
1. Que désigne 95 ou 98 ?
Il s'agit de l'indice d'octane.
2. Donner la formule brute d'un alcane linéaire et celle d'un alcène.
Alcane : CnH2n+2 ; alcène : CnH2n.
3. Donner la formule semi-développée de l'o-xylène ( 1,2-diméthylbenzène ).
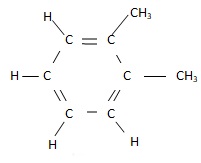
4. Ecrire la réaction de combustion de l'éthanol. Quel est le volume de CO2 formé si on brûle 1 L d'étahnol ?
C2H6O + 3O2 ---> 2CO2+3H2O.
M(éthanol ) =46 g/mol.
Densité éthanol : 0,789.
Masse éthanol dans 1 L : 0,789 kg = 789 g.
Quantité de matière éthanol : 789 / 46 = 17,15 mol.
Quantité de matière dixoyde de carbone : 2 x17,15 =34,3 mol.
Volume molaire des gaz : 24 L / mol.
Volume dioxyde de carbone : 24 x34,3 ~823 L.
|
|
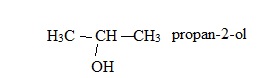





 Il sert d'étallon interne.
Il sert d'étallon interne.